På hydratiseringsreaksjoner i alkadiene de er tilleggsreaksjoner, det vil si at komponentene (hydronium og hydroksyd) i vannmolekylet blir tilsatt til et alkadien.
Du alkadiene er hydrokarboner som har en åpen kjede og to dobbeltbindinger (dannet av en sigma og et pi) mellom karbon, som vi kan se i følgende struktur:

Strukturformel av en alkadien
for hydratiseringsreaksjon i alkadiener er utført, er det viktig at pi-bindingen, som er tilstede i dobbeltbindingen, brytes av påvirkning av varme og svovelsyre (H2KUN4). Når pi-bindingen brytes, vises to bindingssteder, hver på en av karbonene som er involvert i dobbeltbindingen.

Fremkomst av bindingssteder med forstyrrelse av pi-binding
Utseendet til bindingssteder på alkadienmolekylet er nødvendig for ionene (H+ og oh-) fra vannet tilsettes alkadien og danner for eksempel en dialkohol (alkohol med to hydroksyler).
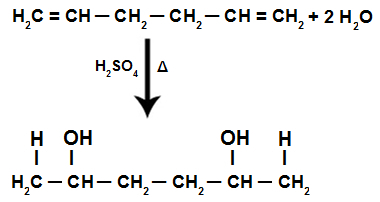
Tillegg av H+ og oh- i strukturen til en alkadien
MERK: Tilsetningen av H+ og oh- i alkadienstrukturen følger Markovnikovs styre, dvs. H+ binder seg til det mest hydrogenerte karbonet, og OH- binder seg til mindre hydrogenert karbon.

Eksempel på anvendelse av Markovnikov-regelen i hydrering av alkadiene
Da det er forskjellige typer alkadiene med hensyn til posisjonen til dobbeltbindinger, kan det være at hydratiseringen av en alkadien danner forskjellige forbindelser. Se følgende tilfeller:
→ Akkumulert eller kondensert alkadien
Det er en alkadien som har to dobbeltbindinger samtidig som tre atomer på karbon, det vil si at det ikke er noen enkeltbinding som skiller karbonene som er involvert i bindingene dobler.

Strukturformel for akkumulert alkadien
Under hydratiseringsreaksjonen til en vekslende alkadien brytes pi-bindingene, idet de er H+ tilsatt til de mer hydrogenerte karbonene og OH- tilsatt mindre hydrogenerte karbonatomer:
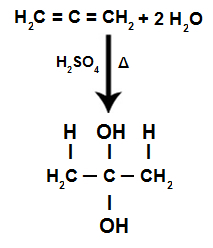
Akkumulert ligning av alkadienhydreringsreaksjon
Vi har at i hydrering av en akkumulert alkadien mottar det samme karbonatomet de to hydroksylene, og danner en tvillingalkohol, som er en ustabil struktur.

Strukturen til tvillingformet alkohol
Ettersom tvillingalkoholen er ustabil, har vi dannelsen av et vannmolekyl med komponentene i de to hydroksylene og dannelsen av en pi-binding mellom karbon og oksygen.

Dannelse av et keton fra en tvillingalkohol
Derfor vil hydratiseringsreaksjonen av akkumulerte alkadiene resultere i dannelsen av a keton.
→ Konjugert eller alternativ alkadien
Det er en alkadien som har to dobbeltbindinger samtidig som involverer fire karbonatomer, det vil si at det er en enkeltbinding som skiller karbonene involvert i bindingene dobler.
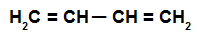
Strukturformel for en alternerende alkadien
I alternerende alkadiene oppstår resonansen til deres dobbeltbindinger. Dermed endrer elektronene til pi-bindingen posisjon (røde piler), som i følgende diagram:
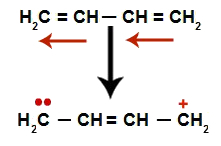
Skjematisk skildring av resonansen i en alternerende alkadien
Vi har generelt utseendet til en dobbeltbinding nøyaktig mellom karbonene der de to doblene var tidligere og etableringen av to bindingssteder, ett på hvert karbon som ikke lenger lager dobbeltbindingen (i eksemplet karbon 1 og 4). Kull 1 og 4 i kjedet mottar H+ og oh- fra vannet.

Delvis hydrering i alternerende alkadien
Etter resonans brytes pi-bindingen til den nye dobbeltbindingen, og en H+ og en oh- tilsettes alkadienmolekylet. OH tilsettes karbonet nærmest den første tilsatte OH-gruppen fordi den gjennomgår den elektroniske tiltrekningen av gruppen, som er mer elektronegativ.

Terminering av hydrering i en alternerende alkadien
På grunn av resonansen sier vi at den alternerende alkadien gjennomgikk en 1,4 hydratisering og dannet en dialkohol.
→ Alkadiene isolert
Det er en alkadien som har to dobbeltbindinger som involverer minst fem atomer samtidig. av karbon, det vil si at det er minst to enkeltbindinger som skiller karbonene som er involvert i bindingene dobler.

Strukturell formel for en isolert alkadien
Under hydratiseringsreaksjonen til en isolert alkadien brytes pi-bindingene, H+ tilsatt til de mer hydrogenerte karbonene og OH- tilsatt de mindre hydrogenerte karbonene.

Isolert alkadienhydreringsreaksjonsligning
Derfor, i tillegg til en isolert alkadien, har vi bare dannelsen av en diaalalkohol.
Av meg. Diogo Lopes Dias
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm
