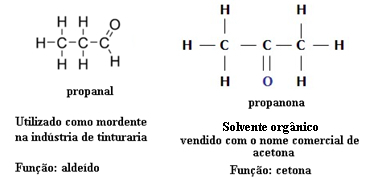
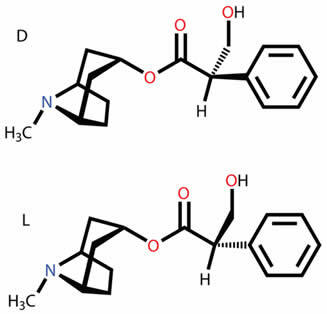
DE Periodiske tabell er en modell som grupperer alle kjente kjemiske elementer og deres egenskaper. De er ordnet i stigende rekkefølge av atomnummer (antall protoner).
Totalt har det nye periodiske systemet 118 kjemiske elementer (92 naturlige og 26 kunstige).
Hver firkant spesifiserer navnet på det kjemiske elementet, dets symbol og atomnummer.
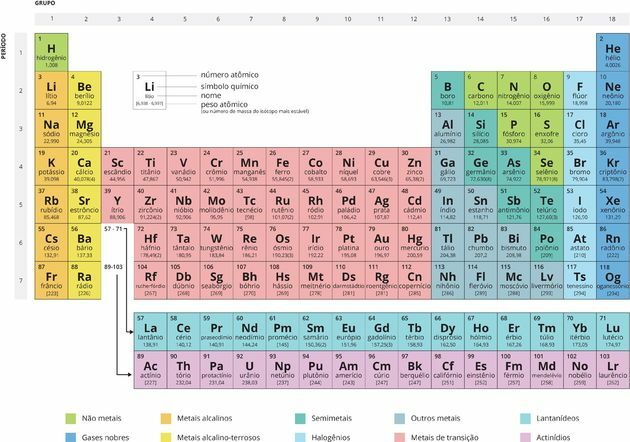
Organisering av periodiske tabeller
samtalene Perioder de er nummererte horisontale linjer, som har elementer som har samme antall elektroniske lag, til sammen sju perioder.
- 1. periode: 2 elementer
- 2. periode: 8 elementer
- 3. periode: 8 elementer
- 4. periode: 18 elementer
- 5. periode: 18 elementer
- 6. periode: 32 elementer
- 7. periode: 32 elementer
Med organisering av periodene i tabellen vil noen horisontale linjer bli veldig lange, så det er vanlig å representere lantanidserien og aktinidserien bortsett fra de andre.
På Familier eller grupper er de vertikale kolonnene, der elementene har samme antall elektroner i det ytterste skallet, det vil si i valenssjikt. Mange elementer i disse gruppene er relatert i henhold til deres kjemiske egenskaper.
Det er atten grupper (A og B), og de mest kjente familiene er fra gruppe A, også kalt representative elementer:
- 1A familie: Alkaliske metaller (litium, natrium, kalium, rubidium, cesium og francium).
- 2A familie: Jordalkalimetaller (beryllium, magnesium, kalsium, strontium, barium og radium).
- 3A familie: Borfamilie (bor, aluminium, gallium, indium, tallium og nihonium).
- 4A familie: Karbonfamilie (karbon, silisium, germanium, tinn, bly og flerovium).
- 5A familie: Nitrogenfamilie (nitrogen, fosfor, arsen, antimon, vismut og muskovium).
- 6A familie: Kalkogener (oksygen, svovel, selen, tellur, polonium, livermorium).
- 7A familie: Halogener (fluor, klor, brom, jod, astatin og tenessin).
- 8A familie: Edle gasser (Helium, Neon, Argon, Krypton, Xenon, Radon og Oganessonium).
Du overgangselementer, også kalt overgangsmetaller, representerer de 8 familiene i gruppe B:
- 1B familie: kobber, sølv, gull og roentgen.
- 2B familie: sink, kadmium, kvikksølv og copernicus.
- 3B familie: skandium, yttrium og alvorlig av lantanider (15 grunnstoffer) og aktinider (15 grunnstoffer).
- 4B familie: titan, zirkonium, hafnium og rutherfordium.
- 5B familie: vanadium, niob, tantal og dubnium.
- Familie 6B: krom, molybden, wolfram og seaborgium.
- 7B familie: mangan, teknetium, rhenium og bohrium.
- 8B familie: jern, ruthenium, osmium, kalium, kobolt, rodium, iridium, meitnerium, nikkel, palladium, platina, darmstadium.
Ved å bestemme International Union of Pure and Applied Chemistry (IUPAC) begynte gruppene å bli organisert etter tall fra 1 til 18, selv om det fremdeles er vanlig å finne familier som blir beskrevet med bokstaver og tall som vist ovenfor.
En viktig forskjell som det nye systemet som ble presentert av IUPAC genererte, er at 8B-familien tilsvarer gruppene 8, 9 og 10 i det periodiske systemet.
Periodesystem i svart-hvitt
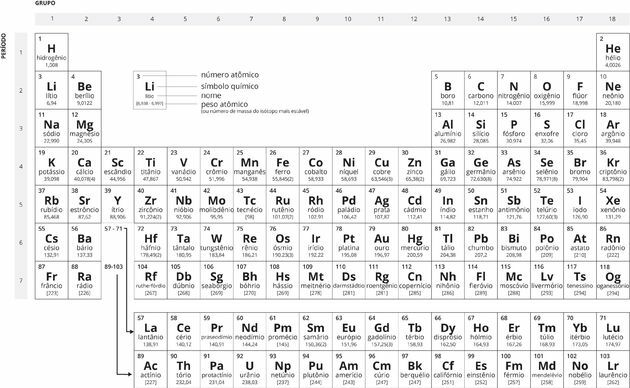
Historien til det periodiske systemet
Det grunnleggende formålet med å lage en tabell var å legge til rette for klassifisering, organisering og gruppering av elementer i henhold til deres egenskaper.
Inntil de nådde den nåværende modellen, skapte mange forskere tabeller som kunne demonstrere en måte å organisere de kjemiske elementene på.
Det mest komplette periodiske systemet ble tegnet av den russiske kjemikeren Dmitri Mendeleev (1834-1907), i året 1869 på grunn av atommasse av elementene.
Mendeleev ordnet grupper av elementer i henhold til lignende egenskaper og etterlot tomme rom for elementer han trodde ville blitt oppdaget.
Det periodiske systemet slik vi kjenner det i dag ble organisert av Henry Moseley, i 1913, etter ordre fra atomnummer kjemiske elementer, omorganisering av tabellen foreslått av Mendeleev.
William Ramsay oppdaget elementene neon, argon, krypton og xenon. Disse elementene sammen med helium og radon inkluderte edelgassfamilien i det periodiske systemet.
Glenn Seaborg oppdaget de transuraniske elementene (nummer 94 til 102) og i 1944 foreslo rekonfigurering av det periodiske systemet, og plasserte serien av aktinider under serien av lantanider.
I 2019 fyller det periodiske systemet 150 år, og det ble opprettet en FN-og UNESCO-resolusjon for å gjøre dette til året Internasjonalt periodisk system for kjemiske elementer som en måte å gjenkjenne en av de mest innflytelsesrike og viktige kreasjonene på av vitenskap.
Nysgjerrigheter i det periodiske systemet
- Den internasjonale foreningen for ren og anvendt kjemi International Union of Pure and Applied Chemistry - IUPAC) er en NGO (ikke-statlig organisasjon) dedikert til studier og fremskritt i Kjemi. Verdensomspennende anbefales standarden som er etablert for det periodiske systemet av organisasjonen.
- For 350 år siden var det første kjemiske elementet som ble isolert i laboratoriet fosfor av den tyske alkymisten Henning Brand.
- Plutonium-elementet ble oppdaget på 1940-tallet av den amerikanske kjemikeren Glenn Seaborg. Han oppdaget alle transuranske elementer og vant Nobelprisen i 1951. Element 106 ble kåret til Seaborgium til hans ære.
- I 2016 ble nye kjemiske elementer i bordet offisiell: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) og Oganesson (Ununóctio).
- De nye kjemiske elementene som er syntetisert kalles supertunge fordi de inneholder et høyt antall protoner, som viser seg å være langt bedre enn de kjemiske elementene som finnes i naturen.
Periodisk oversikt
Sjekk opptakseksamen med en kommentert oppløsning i Øvelser på det periodiske systemet og upubliserte spørsmål i Øvelser i å organisere det periodiske systemet.