Amines er nitrogenholdige organiske forbindelser som er avledet fra stoffet ammoniakk (NH3) ved å erstatte ett eller flere hydrogener med organiske radikaler. I henhold til mengden av substituerte hydrogener, er aminer kan klassifiseres i:
Primær amin: dannet ved å erstatte et hydrogen i ammoniakk med et organisk radikal;
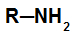
Generell struktur av et primært amin
Sekundær amin: dannet ved erstatning av to ammoniakkhydrogener med to organiske radikaler.

Generell struktur av et sekundært amin
Tertiær amin: dannet ved å erstatte de tre hydrogenene av ammoniakk med tre organiske radikaler.

Generell struktur av et tertiært amin
Amines fysiske egenskaper
De er polare forbindelser;
Primære og sekundære aminer er i stand til å utføre hydrogenbindinger;
Tertiære aminer utfører interaksjon permanent dipol;
Aminer med opptil fem karbon er løselige i vann og etanol. Aminer med seks eller flere karbonatomer er praktisk talt uoppløselig i vann, men oppløselige i organiske løsningsmidler;
Aminer som har en aromatisk struktur er tettere enn vann;
Aminer med ett til tre karbonatomer er gassformede ved romtemperatur. De med fire til tolv karbon er flytende ved romtemperatur;
Generelt har aminer høyere smelte- og kokepunkter bare i forhold til enhver ikke-polær organisk forbindelse.
Kjemiske kjennetegn ved aminer
De regnes som organiske baser, ifølge Bronsted-Lowry-teorien;
Aromatiske aminer har lavere grunnleggende karakter på grunn av fenomenet resonans;
Jo større grunnleggende karakteren til aminet er, desto mer sannsynlig er det å reagere med et bestemt stoff;
I nærvær av en syre utføres aminer nøytraliseringsreaksjon, siden de har en grunnleggende karakter.
regel av aminnomenklatur
For å navngi et amin, følg bare regelen etablert av International Union of Pure and Applied Chemistry (IUPAC), beskrevet nedenfor:
Navnet på radikal eller radikal + amin
MERK: Hvis aminet har forskjellige radikaler, må vi følge alfabetisk rekkefølge.
Følg noen eksempler:
Eksempel 1: primær amin

I det primære aminet i dette eksemplet har vi nærvær av et propylradikal, så navnet er propylamin.
Eksempel 2: sekundær amin

I det sekundære aminet i dette eksemplet har vi tilstedeværelsen av metylradikalen (til venstre for nitrogen) og etylradikalen (til høyre for nitrogenet). Navnet er i alfabetisk rekkefølge etylmetylamin.
Eksempel 3: tertiær amin
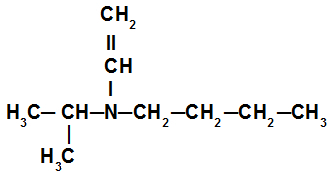
I det sekundære aminet i dette eksemplet har vi isopropylradikalen (til venstre for nitrogen), butylradikalen (til høyre for nitrogenet) og vinylradikalen (under nitrogenet). Navnet er derfor butyl-isopropyl-vinylamin.
Amine-applikasjoner
Mye brukt i produksjonen av forskjellige organiske forbindelser;
Brukes til fremstilling av såper;
Brukes i gummivulkaniseringsprosessen;
Brukes til fremstilling av fargestoffer.
Av meg. Diogo Lopes Dias
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-aminas.htm
