Sublimering er endringen fra fast tilstand til gassform og omvendt, uten å gå gjennom flytende tilstand.
For at et stoff skal gjennomgå sublimeringsprosessen, må det utsettes for visse temperatur- og trykkverdier.
Mothballs og CO2 fast (tørris) er eksempler på stoffer som gjennomgår sublimering under omgivelsesforhold.

Fasediagram
Vi kan oppdage den fysiske tilstanden til et stoff ved å kjenne til verdiene for temperatur og trykk det er utsatt for.
For dette bruker vi diagrammer bygget for hvert stoff, fra verdier funnet eksperimentelt.
Kalt "Fasediagram", er den delt inn i tre regioner som representerer de faste, flytende og gassformede tilstandene. Linjene som avgrenser disse regionene signaliserer punktene der stoffet endrer fase.
Trippelpunktet i diagrammet indikerer temperaturen og trykket som stoffet kan eksistere sammen i de tre fasene. Under dette punktet er sublimeringskurven.
Punktene på denne kurven bestemmer trykk- og temperaturverdiene der sublimering vil forekomme.
Når et fast stoff utsettes for et trykk som er mindre enn trippelpunktet, vil det, hvis det blir oppvarmet, passere direkte i gassform.
Endringen fra direkte fast tilstand til gassform kan også skje ved å senke trykket når temperaturen er lavere enn trippelpunktet.
Lær mer på: Endringer i fysisk tilstand.
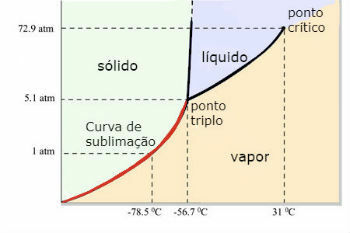
Fasediagram for karbondioksid (CO)2 )
CO-trippelpunktet2 oppstår når trykket er 5 atm. Dette faktum rettferdiggjør at det er vanlig å se forekomsten av sublimering i tørris, siden omgivelsestrykket er 1 atmosfære.
Av denne grunn oppnås ikke flytende karbondioksid under omgivelsesforhold. Under disse forholdene er den enten i fast tilstand eller i damptilstand.
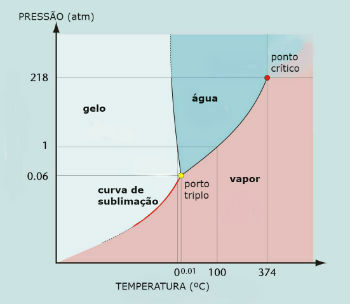
Vannfasediagram (H2O)
Trippelpunktet for vann oppstår når trykket bare er 0,06 atm. Under omgivelsesbetingelser er sublimering av vann således ikke vanlig.
For å lære mer, les også:
- Fysiske tilstander av vann
- Materielle fysiske tilstander
- Væske eller kondens
- Materieegenskaper
- Størking
- Fusjon
- Fordampning
- Kokende
- Fordampning