Grafen er et nanomateriale som bare består av karbon, der atomer binder seg sammen for å danne sekskantede strukturer.
Det er den fineste krystall som er kjent, og dens egenskaper gjør den svært ønskelig. Dette materialet er lett, elektrisk ledende, stivt og vanntett.
Anvendeligheten av grafen er på flere områder. De mest kjente er: sivil konstruksjon, energi, telekommunikasjon, medisin og elektronikk.
Siden det ble oppdaget, har grafen vært sentrum for forskningsinteresse. Studien av søknader om dette materialet mobiliserer institusjoner og investeringer på millioner av euro. Så forskere over hele verden prøver å utvikle en billigere måte å produsere den i stor skala på.
Forstå hva grafen er
Grafen er en allotropisk form for karbon, hvor arrangementet av atomene til dette elementet danner et tynt lag.
Denne allotropen er todimensjonal, det vil si at den bare har to målinger: bredde og høyde.
For å få et inntrykk av størrelsen på dette materialet, tilsvarer tykkelsen på et papir et overlag av 3 millioner lag med grafen.
Selv om det er det tynneste materialet som er isolert og identifisert av mennesker, er dets dimensjon i størrelsesorden nanometer. Den er lett og sterk, i stand til å lede elektrisitet bedre enn metaller som kobber og silisium.
Ordningen som karbonatomene antar i strukturen til grafen, gjør at det er veldig interessante og ønskelige egenskaper i den.
Grafenapplikasjoner
Mange selskaper og forskningsgrupper rundt om i verden publiserer resultater av arbeid som involverer søknader om grafen. Se nedenfor de viktigste.
| Drikkevann | Grafenformede membraner er i stand til å avsalte og rense sjøvann. |
|---|---|
| CO-utslipp2 | Grafenfiltre er i stand til å redusere CO-utslipp2 ved å skille gasser generert av næringer og virksomheter som vil bli avvist. |
| sykdomsdeteksjon | Mye raskere biomedisinske sensorer er basert på grafen og kan oppdage sykdommer, virus og andre giftstoffer. |
| Konstruksjon | Byggematerialer som betong og aluminium blir lettere og sterkere med tilsetning av grafen. |
| Skjønnhet | Hårfarging ved å spraye grafen, hvis varighet vil være rundt 30 vasker. |
| Mikroenheter | Flisene blir enda mindre og sterkere på grunn av erstatning av silisium med grafen. |
| Energi | Solceller har bedre fleksibilitet, mer gjennomsiktighet og lavere produksjonskostnader ved bruk av grafen. |
| Elektronikk | Batterier med bedre og raskere energilagring kan lade seg på opptil 15 minutter. |
| Mobilitet | Sykler kan ha fastere dekk og rammer som veier 350 gram ved hjelp av grafen. |
Grafenstruktur
Strukturen av grafen består av et nettverk av karbon koblet i sekskanter.
Karbonkjernen består av 6 protoner og 6 nøytroner. Atomets 6 elektroner er fordelt i to lag.
På valenssjikt det er 4 elektroner, med dette skallet som holder opptil 8. Derfor, for at karbon skal få stabilitet, må det koble til 4 forbindelser og nå den elektroniske konfigurasjonen av edelgass, som angitt i oktettregelen.
Atomer i grafen binder seg av kovalente bindingerdet vil si deling av elektroner.

Karbon-karbonbindinger er de sterkeste bindingene som finnes i naturen, og hvert karbon forbinder de andre 3 i strukturen. Derfor er hybridiseringen av atomet sp2, som tilsvarer 2 enkelt- og en dobbeltbinding.
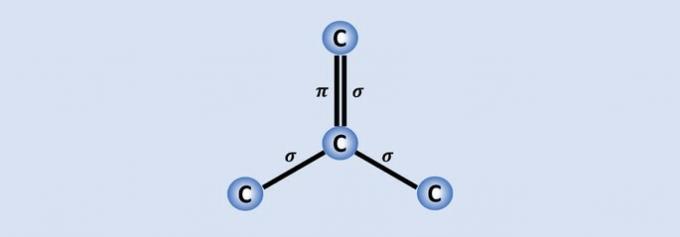
Av de 4 karbonelektronene deles tre med naboatomene og ett som utgjør bindingen. , hjelper for eksempel grafen til å være en god leder av elektrisitet fordi den har mer "frihet" i materialet.
Grafenegenskaper

| Lys | En kvadratmeter veier bare 0,77 milligram. En grafen aerogel er omtrent 12 ganger lettere enn luft. |
|---|---|
| Fleksibel | Den kan utvide opptil 25% av lengden. |
| Dirigent | Dens nåværende tetthet er høyere enn kobber. |
| Varig | Den utvides i kulde og krymper i varmen. De fleste stoffer virker på motsatt måte. |
| Vanntett | Nettverket dannet av karbon tillater ikke engang passering av et heliumatom. |
| Motstandsdyktig | Omtrent 200 ganger sterkere enn stål. |
| Gjennomsiktig | Absorberer bare 2,3% av lyset. |
| Tynn | En million ganger tynnere enn et menneskehår. Tykkelsen er bare ett atom. |
| Hard | Hardest kjent materiale, enda mer enn diamant. |
Historie og oppdagelse av grafen
Begrepet grafen ble først brukt i 1987, men ble først offisielt anerkjent i 1994 av União de Química Pure and Applied.
Denne betegnelsen oppsto fra krysset til grafitt med suffikset -ene, med henvisning til stoffets dobbeltbinding.
Siden 1950-tallet snakket Linus Pauling i klassene sine om eksistensen av et tynt lag karbon, bestående av sekskantede ringer. Philip Russell Wallace beskrev også noen viktige egenskaper ved denne strukturen år tidligere.
Imidlertid, nylig, i 2004, ble grafen isolert av fysikerne Andre Geim og Konstantin Novoselov ved University of Manchester, og kan være dypt kjent.
De studerte grafitt og ved hjelp av teknikken for mekanisk peeling klarte de å isolere et lag med materiale ved hjelp av klebebånd. Denne prestasjonen tildelte Nobelprisen til paret i 2010.
Viktigheten av grafen for Brasil
Brasil har en av de største reservene av naturlig grafitt, et materiale som inneholder grafen. Grafitt naturreservater når 45% av verdens totale.
Selv om forekomsten av grafitt blir observert over hele det brasilianske territoriet, finnes de utnyttede reservene i Minas Gerais, Ceará og Bahia.
Med rikelig med råvarer investerer Brasil også i forskning i området. Det første laboratoriet i Latin-Amerika dedikert til forskning med grafen ligger i Brasil, ved Universidade Presbiteriana Mackenzie i São Paulo, kalt MackGraphe.
Grafenproduksjon
Grafen kan fremstilles av karbid, hydrokarbon, karbonnanorør og grafitt. Sistnevnte er det mest brukte som utgangsmateriale.
De viktigste metodene for produksjon av grafen er:
- Mekanisk mikroeksfoliering: En grafittkrystall har lag av grafen fjernet ved hjelp av et bånd som er avsatt på underlag som inneholder silisiumoksid.
- Kjemisk mikroeksfoliering: karbonbindinger svekkes ved tilsetning av reagenser, noe som delvis bryter nettverket.
- Kjemisk dampavsetning: dannelse av grafenlag avsatt på faste bærere, for eksempel metallisk nikkeloverflate.
Grafenpris
Vanskeligheten med å syntetisere grafen i industriell skala betyr at verdien av dette materialet fortsatt er veldig høyt.
Sammenlignet med grafitt er prisen tusenvis av ganger høyere. Mens 1 kg grafitt selges for 1 dollar, gjøres salget av 150 g grafen for 15 000 dollar.
Nysgjerrigheter om Graphene
- EU-prosjektet, kalt Grafen Flaggskip, øremerket rundt 1,3 milliarder euro til forskning relatert til grafen, applikasjoner og produksjonsutvikling i industriell skala. Rundt 150 institusjoner i 23 land deltar i dette prosjektet.
- Den første kofferten utviklet for romfart har grafen i sammensetningen. Lanseringen er planlagt til 2033, da NASA planlegger å gjennomføre ekspedisjoner til Mars.
- Borophene er grafens nye konkurrent. Dette materialet ble oppdaget i 2015 og regnes som en forbedret versjon av grafen, som er enda mer fleksibelt, motstandsdyktig og ledende.
Grafen i Enem
I Enem 2018-testen, et av spørsmålene til Naturvitenskap og dets teknologier handlet om grafen. Sjekk nedenfor den kommenterte løsningen på dette problemet.
Grafen er en allotropisk form for karbon som består av et plant ark (todimensjonalt utvalg) av komprimerte karbonatomer som bare er ett atom tykt. Dens struktur er sekskantet, som vist på figuren.
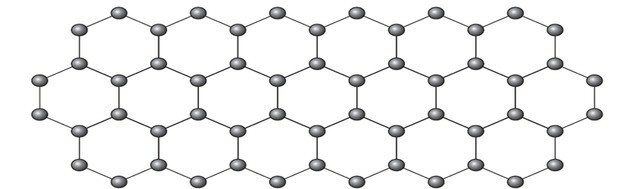
I denne ordningen har karbonatomer hybridisering
a) sp av lineær geometri.
b) sp2 av plan trigonal geometri.
c) sp3 vekslet med sp-hybridiserte karbonatomer med lineær geometri.
d) sp3d av plan geometri.
e) sp3d2 med sekskantet plan geometri.
riktig alternativ: b) sp2 av plan trigonal geometri.
Karbonallotropi oppstår på grunn av dets evne til å danne forskjellige enkle stoffer.
Fordi den har 4 elektroner i valensskallet, er karbon tetravalent, det vil si at det har en tendens til å lage 4 kovalente bindinger. Disse obligasjonene kan være enkle, doble eller tredoble.
Avhengig av bindingene som karbon lager, endres den romlige strukturen til molekylet til det arrangementet som passer best til atomene.
Hybridisering skjer når det er en kombinasjon av orbitaler, og for karbon kan det være: sp, sp2 og sp3, avhengig av typen samtaler.
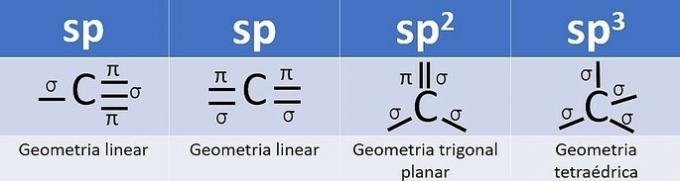
Antallet hybridorbitaler er summen av sigma (σ) bindingene som karbonet lager, da bindingen ikke hybridiserer.
- sp: 2 sigma lenker
- sp2: 3 sigma lenker
- sp3: 4 sigma lenker
Representasjonen av grafen allotrope i kuler og pinner, som vist i figuren i spørsmålet, viser ikke stoffets virkelige bindinger.
Men hvis vi ser på en del av bildet, ser vi at det er ett karbon, som representerer en ball, som kobles til tre andre karbonatomer som danner en struktur som en trekant.
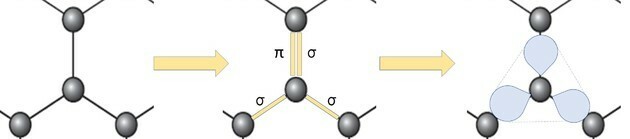
Hvis karbon trenger 4 bindinger og er bundet til 3 andre karbonatomer, er en av disse bindingene dobbelt.
Fordi den har en dobbel og to enkeltbindinger, har grafen sp-hybridisering2 og følgelig trigonal plan geometri.
De andre kjente allotropiske karbonformene er: grafitt, diamant, fulleren og nanorør. Selv om de alle er laget av karbon, har allotroper forskjellige egenskaper, som stammer fra deres forskjellige strukturer.
Les også: Kjemi i fiende og Kjemispørsmål i fiende.



