Teksten Titrering viste hvordan denne volumetriske analyseteknikken utføres, hvis hovedmål er identifisere konsentrasjonen av en løsning gjennom reaksjonen med en annen løsning med kjent konsentrasjon.
Nå skal vi se hvordan vi bruker dataene som er oppnådd i titreringen for å komme til ønsket konsentrasjon, som kan være en syre eller en base i løsning. For å gjøre det, er det i utgangspunktet tre trinn:
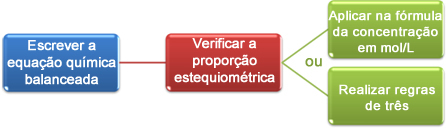
La oss se på et eksempel:
La oss si at en kjemiker hadde en løsning av eddiksyre (eddik (CH3COOH(her))) og ønsket å finne ut konsentrasjonen i mol / l. Deretter plasserte han 20,0 ml eddik (titrert) i en Erlenmeyer-kolbe og tilsatte fenolftaleinindikatoren. Deretter fylte han en 100 ml burette med natriumhydroksid (NaOH) med kjent konsentrasjon (titrerende) lik 1,0 mol / l. Til slutt utførte kjemikeren titreringen og la merke til at fargeforandringen (vendepunkt - da han stoppet titreringen) skjedde da 24 ml NaOH ble konsumert.

Basert på dette eksperimentet fikk han følgende data:
MCH3COOH= ?
VCH3COOH = 20 ml = 0,02 liter
MNaOH = 24 ml = 0,024 l
VNaOH = 1,0 mol / l
Hvor M = konsentrasjon i mol / L og V = volum i L.
For å finne ut konsentrasjonen av eddiksyre, må vi først vite hvordan vi skal skrive den kjemiske ligningen som representerer den riktig balanserte nøytraliseringsreaksjonen som skjedde. I dette tilfellet er reaksjonen som følger:
1 CH3COOH(her) + 1 NaOH(her) → 1 NaC2H3O2 (aq) + 1 time2O(ℓ)
Denne delen er viktig for å se det støkiometriske forholdet hvor reaktantene reagerer. Vær oppmerksom på at forholdet er 1: 1, det vil si for hvert mol eddiksyre, 1 mol natriumhydroksid er nødvendig.
Nå kan vi fortsette med beregningene på to måter:
(1.) Gjennom formelen: M1. V1 = M2. V2
Siden det støkiometriske forholdet er 1: 1, må vi: NeiCH3COOH = nNaOH .
Å være M = n / V. → n = M. V. Dermed kommer vi til listen ovenfor, som i dette tilfellet kan skrives slik: MCH3COOH. CH3COOH = MNaOH. VNaOH
Så bare erstatt verdiene til denne formelen:
MCH3COOH. V CH3COOH = MNaOH. VNaOH
MCH3COOH. 0,02 L = 1,0 mol / L. 0,024 L.
MCH3COOH = 0,024 mol
0,02 l
MCH3COOH = 1,2 mol / l
Derfor var den opprinnelige konsentrasjonen av eddiksyreoppløsningen, vår tittel 1,2 mol / l.
Viktig notat: Hvis det støkiometriske forholdet ikke var 1: 1, ville det være nok å multiplisere konsentrasjonen i mol / L (M) av stoffene med deres respektive koeffisienter. For eksempel, hvis forholdet var 1: 2, ville vi ha følgende:
M1. V1 = 2. M2. V2
Men her er en annen måte å utføre disse beregningene på:
(2.) Gjennom regler på tre:
1 CH3COOH(her) + 1 NaOH(her) → 1 CH3COONa(her) + 1 time2O(ℓ)
1 mol 1 mol 1 mol 1 mol
1. 60g 1. 40 g 1. 82 g 1. 18 g
Disse massene er de beregnede molekylmassene for hvert stoff.
* Å vite at det brukte volumet av 1,0 mol / L NaOH-løsning(her) var 24 ml, kan vi først finne ut mengden materie (mol) NaOH som reagerte:
1 mol NaOH → 1,0 L
1 mol NaOH 1000 ml
x 24 ml
x = 0,024 mol NaOH
* Siden forholdet er 1: 1, bør mengden materie (mol) eddiksyre være den samme som NaOH: 0,024 mol.
Observasjon: Hvis det støkiometriske forholdet var forskjellig, ville vi ta hensyn til det i denne delen. For eksempel, hvis det var 1: 3 og mengden materie av en kjemisk reaktiv art var lik 0,024 mol, ville den for det andre stoffet være tredobbelt: 0,072.
* Nå beregner vi:
20 ml eddik 0,024 mol eddiksyre
1000 ml eddik og
y = 1,2 mol
Det vil si at det er 1,2 mol / l, som er den samme verdien vi fikk i forrige metode.
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/calculos-envolvidos-na-titulacao.htm
