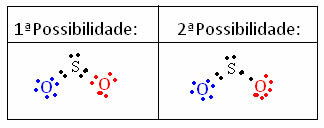
Du nitroforbindelser er preget av tilstedeværelsen av følgende funksjonelle gruppe:
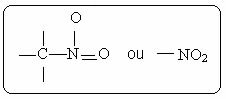
Blant dets derivater er det mest kjente nitrobenzen, som er en gul væske, giftig, uoppløselig i vann, tett og brukt som løsningsmiddel for organiske stoffer.
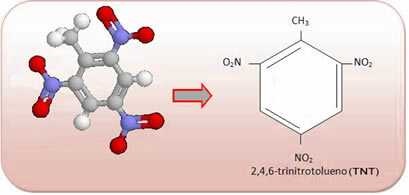
Disse forbindelsene er veldig reaktive, så de blir mye brukt som eksplosiver. Noen velkjente eksempler er 2-metyl-1,3,5 - trinitrobenzen eller 2,4,6-trinitrotoluen (TNT), eller 2,4,6 - dinitrotoluen (DNG) og trinitroglyserin (TNG), som i tillegg til å være et eksplosivt stoff også brukes som en koronar vasodilator i tilfelle fare for infarkt.
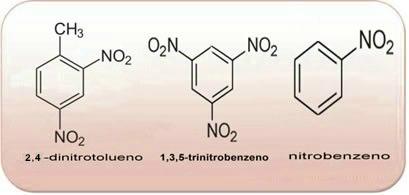
Ovennevnte forbindelser er alle aromatiske, jo større er mengden NO2 i molekylene, jo mer eksplosivt vil det være. Deres preparater og egenskaper er veldig forskjellige fra alifatiske nitroforbindelser. Nitroalkaner er fargeløse, polære væsker, også uoppløselige i vann og brukes i organiske synteser, som mellomprodukter og som løsningsmidler.
Ikke stopp nå... Det er mer etter annonseringen;)
Nomenklaturen for nitrocompounds følger regelen nedenfor, etablert av International Union of Pure and Applied Chemistry (IUPAC):

Dermed har vi følgende navn på nitrocompound strukturer nedenfor:
H3Ç__PÅ2: nitrometan
H3Ç__CH2__PÅ2: nitroetan
H3Ç__CH2__ CH2__PÅ2: 1- nitropropan
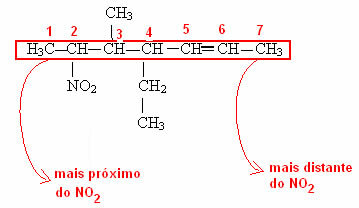
Legg merke til i det siste eksemplet at det var nødvendig å nummerere hvor den funksjonelle gruppen i karbonkjeden kommer fra. Denne nummereringen gjøres alltid fra den nærmeste enden av den funksjonelle gruppen. Se hvordan dette gjøres i eksemplet nedenfor:
Av Jennifer Fogaça
Uteksamen i kjemi
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Nitrocompounds"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/nitrocompostos.htm. Tilgang 27. juni 2021.