O varme og Termisk energi, motivert av forskjellen på temperatur, som flyter fra kroppen med høyere temperatur til kroppen med lavere temperatur. Energistrømmen mellom kropper med forskjellige temperaturer finner sted til den når termisk balanse, når temperaturen til kroppene som byttet varme blir lik.

Selv om Internasjonalt system for enheter (SI) bestemme at enheten for energi er joule (J), den mest brukte enheten for varme er kalori (cal). En kalori tilsvarer mengden varme som er nødvendig for at 1 g vann skal gjennomgå en temperaturvariasjon fra 14,5 ° C til 15,5 ° C.
Korrespondansen mellom kalorier og joule er at 1 kal tilsvarer omtrent 4,18 J.
fornuftig varme
Når en kropp mottar eller gir en viss mengde varme, bare i stand til å generere temperaturvariasjoner, uten å forekomme endring i aggregeringstilstand for molekyler, heter varmen følsom.
Gjennom følgende ligning kan mengden fornuftig varme mottatt eller tapt av en kropp bestemmes.
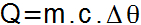
I denne ligningen er de tilsvarende elementene og måleenhetene:
Q = Mengde fornuftig varme (kalk);
m = Stoffmasse (g);
c =spesifikk varme (cal / g ° C);
Δθ = Temperaturvariasjon (° C eller K).
To observasjoner er viktige:
O spesifikk varme det er en karakteristisk mengde av hver type stoff som bestemmer hvor mye varme som trengs for 1 g av elementet for å øke temperaturen med 1 ° C.
Temperaturvariasjoner kan uttrykkes både i ° C hvor mye i K, fordi disse to vekter har 100 intervaller, og presenterer dermed samme variasjoner.
Eksempel
Bestem mengden fornuftig varme som trengs for å varme opp, fra 40 ° C til 50 ° C, en prøve på 4 kg av et gitt stoff med en spesifikk varme på 0,5 cal / g ° C.
Spørsmålsdata:
Masse m: m = 4 kg = 4000 g
Temperaturområde: Δθ = 50 - 40 = 10 ° C
Spesifikk varme: c = 0,5 cal / g ° C
Q = m.c.Δθ
Q = 4000. 0,5. 10
Q = 20.000 cal = 20 kcal
Denne stoffmengden vil variere med 10 ° C når den får 20.000 kalk varme.
Av Joab Silas
Uteksamen i fysikk
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-calor-sensivel.htm
