O Thomson atommodell ble foreslått i år 1898 av den engelske fysikeren Joseph John Thomson eller ganske enkelt J.J. Thomson. Etter å ha flere eksperimentelle bevis for eksistensen av elektronet, velte han teorien om udelbarheten av atomet som ble foreslått av John Dalton.
Thomson, basert på sin modell, bekreftet og beviste eksistensen av elektroner (partikler med negativ elektrisk ladning) i atomet, det vil si atomet har subatomære partikler.
Tankekart: Thomson Atomic Model
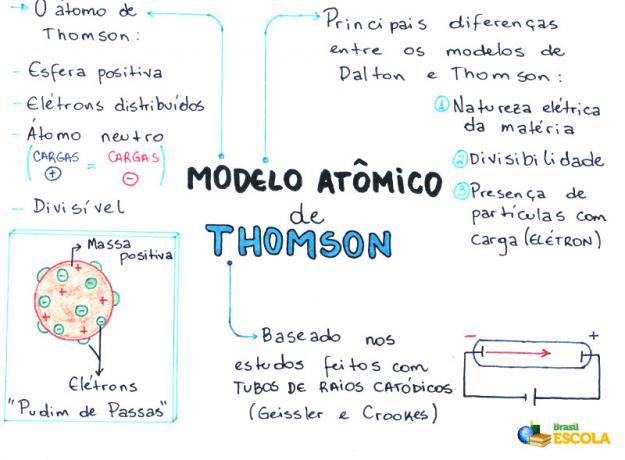
* For å laste ned tankekartet i PDF, Klikk her!
Thomson foreslo sin atommodell basert på funn relatert til radioaktivitet og eksperimenter utført med katodestrålerøret bygget av forskerne Geissler og Crookes. Se en fremstilling av dette røret:
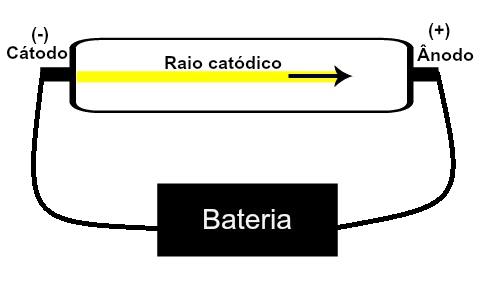
Når en sjelden lavtrykksgass utsettes for høy elektrisk spenning (f.eks. 15000 V), produserer den en lysstråle (sammensatt av elektriske ladninger) fra katoden (negativ pol) mot anoden (pol positivt).
Med dette eksperimentet kom Thomson til den konklusjonen at når atomene til det gassformige materialet inne av røret ble utsatt for en høy spenning, deres elektroner ble revet ut og ledet til platen positivt.
Hensyn som er foreslått av atomsmodellen Thomson
Med eksperimentene som ble utført med katodestrålerøret, foreslo Thomson sin tolkning av hvordan atomet og dets konstitusjon ville være. Så ifølge ham:
- Atomet er en kule, men ikke massiv som foreslått av John Dalton atommodell;
- Atomet er nøytralt, siden all materie er nøytral;
- Ettersom atomet har elektroner som har negative ladninger, må det derfor ha positive partikler slik at den endelige ladningen er null;
- Elektroner er ikke faste eller fanget i atomet, de kan overføres til et annet atom under visse forhold;
- Atomet kan betraktes som en kontinuerlig væske med positive ladninger der elektroner, som har en negativ ladning, vil bli fordelt;
- tilknyttet din modell til en rosinpudding (som representerer elektronene);
- Ettersom elektronene som er spredt har samme ladning, er det en gjensidig frastøting mellom dem, noe som gjør dem jevnt fordelt i sfæren.
Nyheter foreslått for atomet etter Thomson-modellen
Thomsons atommodell var den andre som ble foreslått for atomet. Den første modellen ble formulert av John Dalton.
Ikke stopp nå... Det er mer etter annonseringen;)
Thomsons modell handlet om ny kunnskap om atomet som til da ikke hadde blitt foreslått på grunn av mangel på vitenskapelig grunnlag, for eksempel:
- Materiellets elektriske natur;
- Atom splittbarhet;
- Tilstedeværelse av små, ladede partikler i atomet.
Problemer påpekt Thomson-atomet
Flere fysikere på tidspunktet for forslaget til Thomson atommodell, basert på teoriene om klassisk fysikk, påpekte noen inkonsekvenser i denne modellen:
- Thomson foreslo at atomet hadde en stabilitet i forhold til den jevne fordeling av elektroner, som kunne modifiseres av påvirkning av energi. Imidlertid, Klassisk fysikk, basert på elektromagnetisme, tillater ikke eksistensen av et stabilt system basert bare på frastøting mellom partikler med samme ladning;
- For Thomson er elektroner jevnt fordelt i atomet, men de har evnen til å skifte på en akselerert måte og må derfor avgi elektromagnetisk stråling ved bestemte frekvenser spesifikk. Dette ble imidlertid ikke observert.
- Thomsons modell var ofte ineffektiv i å forklare atomegenskaper som deres sammensetning og organisering.
* Mind Map av Victor Ricardo Ferreira
Kjemi lærer
Av meg. Diogo Lopes Dias
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
DAGER, Diogo Lopes. "Thomsons Atomic Model"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/o-atomo-thomson.htm. Tilgang 27. juni 2021.
Kjemi

Niels Bohr, Bohrs atom, atomfysikk, stabilt atom, atommodell, planetariske system, lag av elektrosfæren, energinivåer, elektronskjell, elektronenergi, Rutherford atommodell, opphisset tilstandsatom.
Kjemi
Atomer og konstruksjonen av universet, atomteori, at alt er laget, materie består av atomer, teori om de fire elementene, gamle alkymister, atomteori, grunnleggende partikkel.