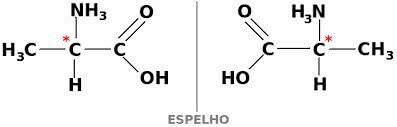
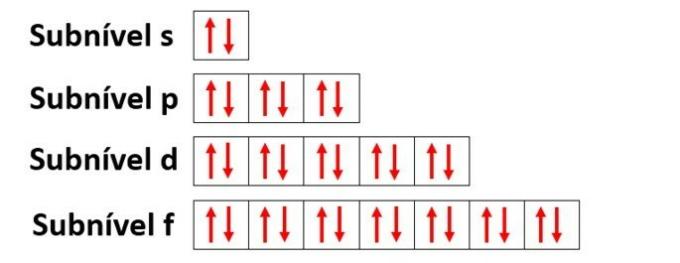
een energetische oxidatiereactie in alkenen treedt op wanneer er een breuk van het molecuul is, dat wil zeggen, het gelijktijdig verbreken van de twee dubbele bindingen en de zuurstof inlaat in het organische molecuul.
Het is mogelijk om dit type reactie uit te voeren met alkenen bij gebruik van kaliumpermanganaat (KMnO4) of kaliumdichromaat (K2Cr2O7) geconcentreerd, in een zuur medium, terwijl het heet is.
In het zure medium zijn er H-ionen3O+ waardoor KMnO ontbindt4 en het vrijgeven van 5 atomen van ontluikende zuurstof [O] voor elke 2 KMnO4. Noteer deze ontleding hieronder:

Deze reactie wordt "energetisch" genoemd omdat het de twee bindingen van het dubbel verbreekt (bij milde oxidatie wordt alleen de binding verbroken pi), een andere factor is dat deze reductie van mangaan in een zuur medium veel intenser is dan in een basisch medium, zoals in milde oxidatie.
De ontluikende zuurstof die vrijkomt, reageert dan met een alkeen, maar het eindproduct hangt af van wat de soorten koolstof die de dubbele binding aangaan, dwz of ze primair, secundair of. zijn tertiair. Kijk wat er in elk geval gebeurt:
Niet stoppen nu... Er is meer na de reclame ;)
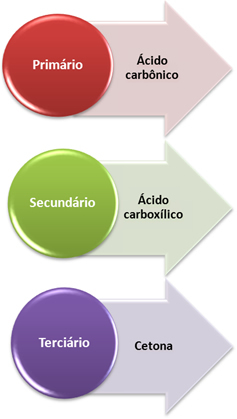
- Primaire koolstof: Als de onverzadiging tussen twee primaire koolstoffen ligt, zijn de gevormde producten twee koolzuur (H2CO3). Als slechts één van de koolstofatomen in de dubbele binding primair is, zal slechts één van de gevormde moleculen koolzuur zijn. Deze verbinding is echter onstabiel en is nooit geïsoleerd, het valt uiteen in: water en koolstofdioxide.
- Secundaire koolstof: Als de onverzadiging tussen twee secundaire koolstoffen ligt, zullen de twee gevormde producten zijn carbonzuren. Als slechts één van de koolstoffen secundair is, zal dit aanleiding geven tot een carbonzuurmolecuul, terwijl de andere afhankelijk is van de andere koolstof.
- Tertiaire koolstof: Ontstaat keton.
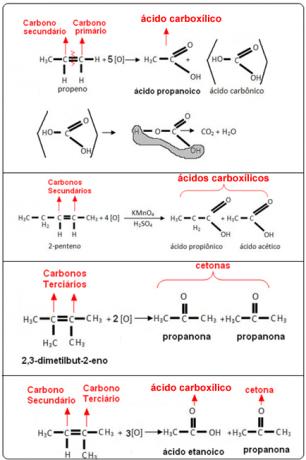
Zie de voorbeelden hieronder:
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijken:
FOGAÇA, Jennifer Rocha Vargas. "Energie-oxidatie van alkenen"; Brazilië School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcenos.htm. Betreden op 28 juni 2021.