Gastransformaties zijn processen waarbij a gas- kan een of meer van zijn parameters hebben van druk, volume en temperatuur-veranderd. Er zijn speciale gastransformaties waarbij ten minste één van deze grootheden constant wordt gehouden.
De soorten gastransformaties zijn:
isobare transformatie;
isotherme transformatie;
isovolumetrische transformatie;
adiabatische transformatie.
Zie ook:Thermologie - de studie van verschijnselen die verband houden met warmte en temperatuur
isotherme transformatie
De isotherme transformatie is er een waarbij de temperatuur van een gas constant blijft. Bij dit soort transformatie druk en volume zijnomgekeerdproportioneel, zodat door het verhogen van de druk, wordt het volume verlaagd en omgekeerd.
Isotherme transformaties worden beschreven door Lhey boyle-mariotte. Volgens deze wet is het product tussen druk en volume van een ideaal gas constant:

VOORl en VOORF – begin- en einddruk
Vl en VF – begin- en eindsnelheid
K – constante
isobare transformatie
De isobare transformatie wordt gekenmerkt door a
volume variatie en temperatuur-, waardoor de druk constant blijft. Dit type transformatie wordt wiskundig beschreven door de wet van Charles en Gay-Lussac. Tijdens een isobare transformatie zijn temperatuur en volume recht evenredig, dat wil zeggen, houden constant de druk van een gas, zal het volume dat het inneemt toenemen met de toename van de temperatuur van het gas. gas.Zie de formule die wordt gebruikt door Wet Gay-Lussac:
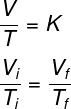
tl en tF – begin- en eindtemperatuur
Volgens de Wet van Gay-Lussac, is de verhouding tussen het volume en de druk van een gas, tijdens een isobare transformatie, gelijk aan een constante.
Niet stoppen nu... Er is meer na de reclame ;)
isovolumetrische transformatie
Isovolumetrische, isometrische of isochorische transformatie is de naam van het proces waarbij een ideaal gas veranderingen in druk en temperatuur ondergaat en zichzelf behoudt constante jouw volume. Dit type gastransformatie, dat plaatsvindt in containers met stijve wanden, wordt wiskundig gedefinieerd door de De wet van Charles.
Volgens deze wet is de verhouding tussen druk en temperatuur van een ideaal gas altijd constant. Bovendien zijn bij dit type transformatie druk en temperatuur rechtevenredig: verdubbeling van de druk, verdubbelen wij de temperatuur en vice versa.
De formule die het gedrag van ideale gassen beschrijft tijdens isovolumetrische transformaties is als volgt:
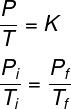
Lees ook: Thermodynamica - een gebied van de natuurkunde dat verschijnselen bestudeert waarin warmte-uitwisseling plaatsvindt
adiabatische transformatie
Adiabatische transformatie is de naam van het proces dat een a gas dat niet verandert warmte met de externe omgeving of met de wanden van zijn container. De formule die wiskundig het gedrag verklaart van een ideaal gas dat een adiabatische transformatie ondergaat, stelt dat het product tussen druk en volume verhoogd tot een constante γ constant is.

De constante γ hangt af van de gradeninvrijheid van het gas, dat wil zeggen, het aantal richtingen waarin de gasmoleculen kunnen bewegen. Het kan ook worden berekend door de verhouding tussen de specifieke hitte in drukconstante en warmtespecifiek in volumeconstante.
Voorbeelden van gastransformaties
isotherme transformatie – elke langzame uitzetting of samentrekking van een gas dat optreedt bij een constante temperatuur.
isobare transformatie – het koelen van het gas in een blaas die in een koelkast is geplaatst om af te koelen.
isovolumetrische transformatie – het volledig verwarmen van de waterdamp in een snelkookpan.
adiabatische transformatie – gas dat wordt verdreven door een spuitbus.

Zie ook: Calorimetrie – formules, concepten en opgeloste oefeningen
Opgeloste oefeningen over gastransformaties
Vraag 1 - Bekijk de onderstaande alternatieven en vink het antwoord aan dat alleen echte alternatieven bevat.
I - Isotherme transformaties zijn die waarbij de gastemperatuur constant wordt gehouden.
II - Adiabatische transformaties omvatten warmte-uitwisseling tussen het gas en de externe omgeving.
III - Isochoortransformatie is er een waarbij de gasdruk constant wordt gehouden.
IV - Isobare transformaties gebeuren met constante druk.
Zijn correct:
a) I en II.
b) I, II en III.
c) II en III.
d) I en IV.
Oplossing:
Alternatieven II en III zijn verkeerd, aangezien adiabatische transformaties geen warmte-uitwisseling met zich meebrengen, en isochore transformaties die plaatsvinden in constante volumes. Het juiste alternatief is dus de letter D.
Vraag 2 -Een ideaal gas ondergaat een snelle transformatie, waardoor temperatuur, druk en volume in korte tijd plotselinge veranderingen ondergaan. Volgens zijn kennis van gastransformaties was de transformatie die het gas onderging:
a) isotherm.
b) isobaar.
c) adiabatisch.
d) isovolumetrisch.
Oplossing:
Adiabatische transformaties vinden snel plaats, dus er is geen tijd voor het gas om warmte uit te wisselen met de externe omgeving. Bij dit type transformatie veranderen de parameters voor druk, volume en temperatuur abrupt. Het juiste alternatief is dus de letter C.
Door Rafael Hellerbrock
Natuurkunde leraar
Wil je naar deze tekst verwijzen in een school- of academisch werk? Kijk:
HELERBROCK, Rafael. "Gastransformaties"; Braziliaanse School. Beschikbaar in: https://brasilescola.uol.com.br/quimica/transformacoes-gasosas.htm. Betreden op 27 juli 2021.