Het is al lang bekend dat wanneer zonlicht door een prisma gaat, vergelijkbaar met dat in de bovenstaande figuur, verstrooiing van de lichtcomponenten optreedt. Deze reeks kleuren, variërend van rood tot violet, staat bekend als continu spectrum, omdat de overgang van de ene kleur naar de andere praktisch onmerkbaar is.
Deze kleuren vormen wat we noemen de zichtbaar licht of zichtbare straling, die zijn samengesteld uit elektromagnetische golven. D.w.z, golven gevormd door oscillaties in het elektrische veld en het magnetische veld die gelijktijdig optreden en loodrecht op elkaar staan.
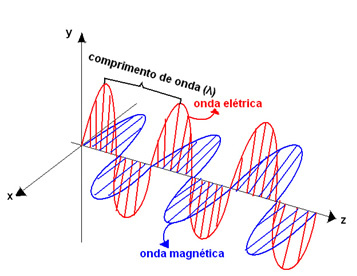
Deze golven hebben frequenties (f) – aantal trillingen van deze golf per seconde – en golflengte – de afstand van de top van de ene golf tot de andere, weergegeven door de Griekse letter lambda (λ). Het verschil tussen de ene kleur en de andere is dus de frequentie en golflengte van elke elektromagnetische golf waaruit de kleuren bestaan.
Dit fenomeen van het waarnemen van het spectrum wordt echter niet alleen verkregen met zonlicht. We kunnen ook andere lichten door een prisma laten gaan. We krijgen dus andere spectra. Echter, deze
spectrum zal zijn discontinu, met afstand tussen kleuren, die we in het spectrum noemen als strepen of bands.Laten we bijvoorbeeld zeggen dat we het licht van een gasontladingsbuis gevuld met waterstofgas door een prisma laten gaan. Het verkregen spectrum zou vergelijkbaar zijn met het hieronder getoonde.

Als het het gas van een ander element zou zijn, zou het spectrum ook discontinu zijn, maar het zou er anders uitzien. Op deze manier dient elk spectrum als een "digitaal" voor de identificatie van chemische elementen; want elk heeft een ander spectrum; herhaalt nooit.
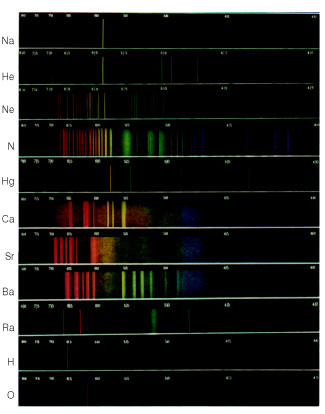
Tegenwoordig is het mogelijk om de spectra van de elementen te verkrijgen en te visualiseren via een apparaat genaamd device spectroscoop.
Door Jennifer Fogaça
Afgestudeerd in scheikunde
Bron: Brazilië School - https://brasilescola.uol.com.br/quimica/espectro-eletromagnetico-dos-elementos-quimicos.htm