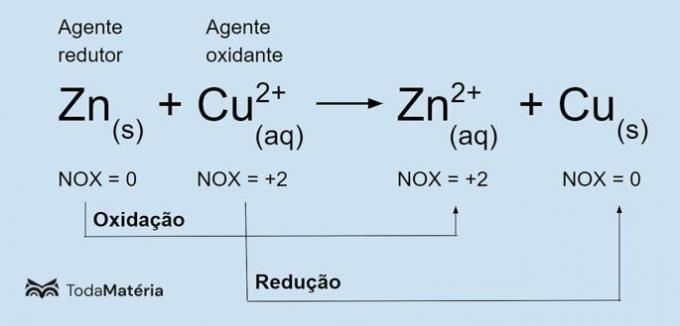
Atoma elektronu elektronisko izplatīšanu neitrālā vai fundamentālā stāvoklī parasti veic ar Paulinga diagramma, parādīts zemāk:
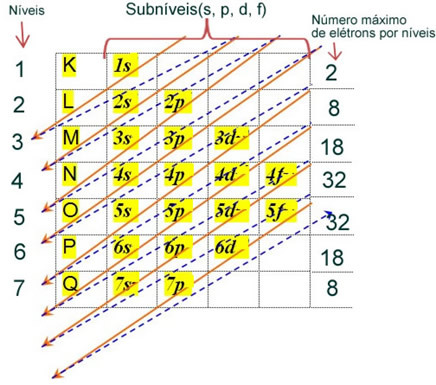
Detalizēti šī izplatīšanas noteikumi ir atrodami šādos divos mūsu vietnes tekstos: “Elektronu elektronu sadalījums" un "Elektroniskās izplatīšanas noteikumi”.
Jonu elektroniskā izplatīšana sākotnēji darbojas tāpat kā neitrālā stāvoklī esošie atomi; tikai ar vienu atšķirību. Tā kā jons ir atoms, kas ieguvis vai zaudējis elektronus, mums tas jāņem vērā un jādara šādi:

Svarīgs novērojums ir: izmaiņas tiek veiktas visattālākajā apakšlīmenī, nevis visenerģiskākās.
ja jons ir a katijons, mums vajadzētu noņemiet elektronus ka viņš zaudēja. Apskatīsim piemēru:
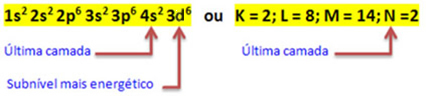
Dzelzs atomam (atomu skaitam = 26) ir šāds elektroniskais sadalījums apakšlīmeņos enerģētiskā secībā: 1.s2 2s2 2. lpp6 3s2 3p6 4s2 3d6. Kas attiecas uz elektroniskajiem slāņiem, mums ir: K =2; L = 8; M = 14; N = 2.
Šis sadalījums ir parādīts Paulinga diagrammā zemāk:
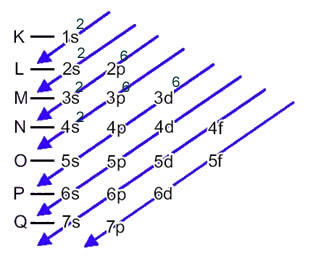
Kad dzelzs atoms zaudē 2 elektronus, tas pārvēršas Fe katjonā.
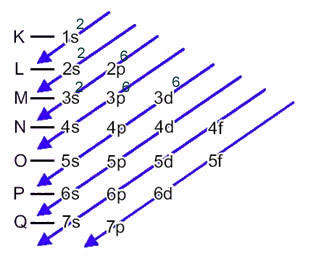
2+. Tātad, veicot elektronisko izplatīšanu, mums tas ir jādara noņemiet 2 elektronus no pēdējās čaulas(N) un nav visenerģētiskākais apakšlīmenis, kā parādīts zemāk:Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)
Tādējādi Fe katjona elektroniskā izplatīšana2+ dod:
1.s2 2s2 2. lpp6 3s2 3p6 3d6 vai K = 2; L = 8; M = 14
Tagad, ja mums jāveic elektroniska izplatīšana a anjons, mums vajadzētu pievienojiet saņemtos elektronus.Skatiet, kā tas tiek darīts, šajā piemērā:
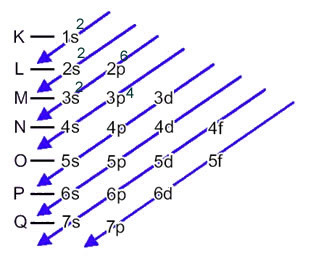
Sēra anjons (16s2-) veidojas no sēra atoma (16S) ar 2 elektronu pieaugumu, kā norādīts ar lādiņu 2-. Tās pamatstāvokļa elektronisko izplatīšanu nodrošina:
1.s2 2s2 2. lpp6 3s2 3p4 vai K = 2; L = 8; M = 6
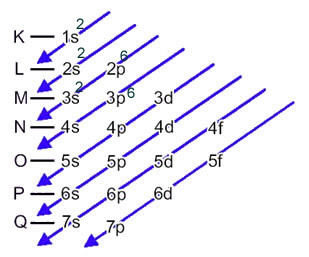
Šajā gadījumā pēdējais apakšlīmenis ir tāds pats kā enerģijas apakšlīmenis 3p. Tātad, mēs tam pievienojam divus sēra anjona elektronus:
1.s2 2s2 2. lpp6 3s2 3p6 vai K = 2; L = 8; M = 8
Autore Jennifer Fogaça
Beidzis ķīmiju
Vai vēlaties atsaukties uz šo tekstu skolas vai akadēmiskajā darbā? Skaties:
FOGAÇA, Jennifer Rocha Vargas. "Elektroniskā jonu sadale"; Brazīlijas skola. Pieejams: https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm. Piekļuve 2021. gada 27. jūnijam.