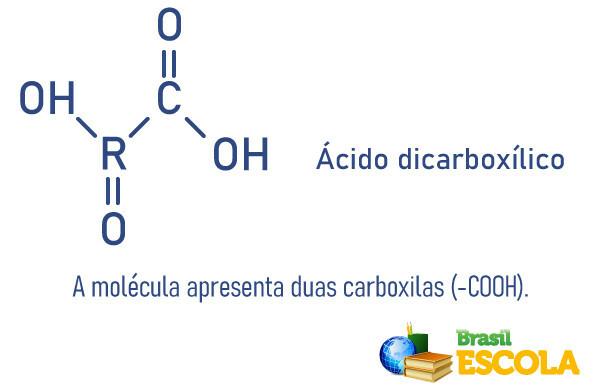
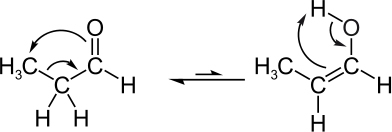
Kondensācijas polimēri, saukti arī par eliminācijas polimēriem, ir tie, kuros to monomēri ir vienādi vai atšķirīgi. apvienoties, vienlaicīgi likvidējot ūdens molekulas vai citas mazas savienojumu molekulas, kas neietilpst polimērs.
Vienīgais izņēmums ir poliuretāns: kondensācijas reakcijā, caur kuru tas tiek iegūts, molekulas neizdalās.
Galvenie savienojumi, kas izdalās papildus ūdenim, ir: hlorūdeņradis (HCl), amonjaks (NH3) un ūdeņraža cianīds (HCN).
Kondensācijas polimēriem vienmēr būs regulāra, vienmērīga struktūra, tas ir, polimēri vienmēr būs pārmaiņus, nevis nejauši. Kopolimērus (kuru struktūra ir neregulāra) var veidot tikai tad, kad vairāk nekā divi monomēri apvienojas, veidojot kondensācijas polimēru.
Ņemot vērā ūdeni kā eliminējamo molekulu, mums ir šāda vispārējās kondensācijas reakcijas shēma šo polimēru veidošanai:
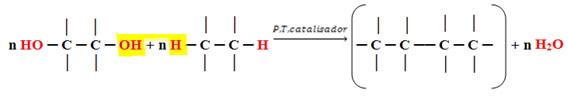
Kondensācijas polimēru veidošanās vispārējā reakcija.
Svarīgākie un visbiežāk izmantotie kondensācijas polimēri mūsu sabiedrībā ir:
• Poliuretāns: ko iegūst, kondensējot parafenilēna diizocianātu ar 1,2-etāndiolu. To lieto izolācijā, raķešu degvielas saistvielās, apģērba oderējumos, polsterējuma putās, sērfošanas dēļos utt .;

Izstrādājumi no poliuretāna.
• Bakelīts: vielas, kas izraisa bakelītu, ir benzols un metanols. To lieto tādos pārklājumos kā krāsas un lakas, koka līmes, trauku rokturi, gaismas slēdži, kontaktligzdas, kontaktdakšas, pārsegi utt .;
• Poliesteris: tie ir polimēri, ko veido vairāki esteri, un to veidošanai ir nepieciešama skābe un spirts. Galvenais poliesteris ir PET (polietilēna tereflāts), kas veidojas, savienojot tereftalskābi ar etāndiolu. To izmanto tekstilšķiedru, piemēram, tergal auduma, ražošanai bezalkoholisko dzērienu pudeļu un citu dzērienu, videolentes, sirds trauki un vārsti kā aizsargs organisko audu, kas cietuši no apdegumiem, atjaunošanai, cita starpā;
• Neilons vai poliamīds: parastie neilona monomēri (neilons 66) ir heksandioīnskābe un 1,6-heksāndiamīns. Tās pielietojumu var redzēt bez eļļošanas gultņos, zobratos, iepakojumos, tekstilšķiedrās, velcros, suku saros, makšķerēšanas vados un elektriskajos piederumos;
Nepārtrauciet tūlīt... Pēc reklāmas ir vairāk;)

zeķes no neilona
• Kevlar®: to veido savienojums starp tereftalskābi un p-benzenediamīnu. To galvenokārt lieto bruņu vestēs, kā arī sacīkšu automašīnu šasijās, sacīkšu automašīnu vadītāju apģērbos, ugunsdzēsības apģērbos un lidmašīnu daļās;

Lodīšu necaurlaidīgas vestes karavīru un policijas aizsardzībai ir izgatavotas no Kevlar® polimēra
• Polikarbonāts: Fosgēna un p-izopropilēndifenola veidots polikarbonāts tiek plaši izmantots ložu necaurlaidīgā stiklā, saulesbrilles lēcās, CD un DVD, rentgena iekārtas, drošības logi un struktūras, kas aptver noteiktas zonas (piemēram, attēlā redzamais) zemāk);

Struktūra, kas izgatavota, pamatojoties uz polikarbonātu.
• Silikoni: ko veido silīcijs kā galvenais elements, kur tā atomi tiek mainīti ar skābekļa elementiem un silīcijs saistās ar organiskajiem radikāļiem. Visizplatītākais silikons ir dihidrimetil-silāns. Šo savienojumu pielietojums ir: plastiskās ķirurģijas ceļā ievietotas protēzes, eļļošana veidnes, logu blīves, iekapsulēti sveķi, kosmētika, piemēram, eļļas un ādas krēmi citi.
Autore Jennifer Fogaça
Beidzis ķīmiju