Periodiskā tabula ir svarīgs mācību līdzeklis, kas apkopo informāciju par visiem zināmiem ķīmiskajiem elementiem.
Pārbaudiet savas zināšanas, izmantojot šo sarakstu 17 jautājumi ar dažādām pieejām par šo tēmu un atrisiniet savas šaubas ar rezolūcijām, kas komentētas pēc atsauksmēm.
Lai palīdzētu saprast jautājumus, izmantojiet periodiskā tabula pilnīgs un atjaunināts.
Periodisko tabulu organizācija
jautājums 1
(UFU) Deviņpadsmitā gadsimta sākumā, atklājot un izolējot dažādus ķīmiskos elementus, radās nepieciešamība tos racionāli klasificēt, lai veiktu sistemātiskus pētījumus. Daudzi sasniegumi tika pievienoti līdz pašreizējās ķīmisko elementu periodiskās klasifikācijas sasniegšanai. Attiecībā uz pašreizējo periodisko klasifikāciju atbildiet:
a) Kā periodiskajā tabulā secīgi uzskaitīti elementi?
Periodiskā tabula ir sakārtota ķīmisko elementu secībās augošā secībā atomu skaitlis. Šis skaitlis atbilst protonu skaitam atoma kodolā.
Šo organizācijas metodi ierosināja Henrijs Moselijs, pārkonfigurējot Dmitrija Mendeļejeva piedāvāto tabulu.
Elementu tabulā var atrast pēc ģimenes un perioda, kurā tas ir ievietots. Šis sadalījums notiek šādi:
| grupas vai ģimenes | 18 vertikālas secības |
| Elementu grupas, kurām ir līdzīgas īpašības. |
| Periodi | 7 horizontālas secības |
| Elementa elektronisko slāņu skaits. |
b) Kuras periodiskās tabulas grupas var atrast: halogēnu, sārmu metālu, sārmu zemes metālu, halogēnu un cēlgāzi?
Elementu klasifikācija grupās tiek veikta pēc īpašībām. Elementiem, kas ietilpst vienā grupā, ir līdzīgas īpašības, un attiecībā uz norādīto klasifikāciju mums:
| Klasifikācija | Grupa | Ģimene | Elementi |
| halogēns | 17 | 7A | F, Cl, Br, I, At un Ts |
| sārmu metāls | 1 | 1A | Li, Na, K, Rb, Cs un Fr |
| sārmu zemes metāls | 2 | 2A | Esiet, Mg, Ca, Sr, Ba un Ra |
| halkogēns | 16 | 6A | O, S, Se, Te, Po un Lv |
| cēlgāze | 18 | 8A | Viņš, Ne, Ar, Kr, Xe, Rn un Og |
2. jautājums
(SPRK-SP) Atrisiniet problēmu, pamatojoties uz tālāk minēto apgalvojumu analīzi.
I - Pašreizējā mūsdienu periodiskā tabula ir sakārtota atomu masas augošā secībā.
II - visi elementi, kuru valences apvalkā ir 1 elektrons un 2 elektroni, ir attiecīgi sārmu metālus un sārmu zemes metālus ar nosacījumu, ka galvenais kvantu skaitlis šī slāņa (n 1).
III - Tajā pašā periodā elementiem ir vienāds skaits līmeņu (slāņu).
IV - Tajā pašā grupā (ģimenē) elementiem ir vienāds līmeņu (slāņu) skaits.
Tiek secināts, ka attiecībā uz pašreizējo periodisko ķīmisko elementu tabulu tie ir pareizi:
a) I un IV (tikai).
b) I un II (tikai).
c) II un III (tikai).
d) II un IV (tikai).
e) III un IV (tikai).
Pareiza alternatīva: c) II un III (tikai).
Analizējot katru alternatīvu, mums:
Es - nepareizi. Elementi ir sakārtoti augošā secībā pēc atomu skaita.
II - PAREIZI. Elektroni valences apvalkā nosaka grupu, kurā atrodas elements.
| sārmu metāli | 1 elektrons valences apvalkā |
| 3lasīt | 2-1 |
| 11Plkst | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Fr | 2-8-18-32-18-8-1 |
| sārmu zemes metāli | 2 elektroni valences apvalkā |
| 4būt | 2-2 |
| 12mg | 2-8-2 |
| 20Šeit | 2-8-8-2 |
| 38Mr | 2-8-18-8-2 |
| 56Ba | 2-8-18-18-8-2 |
| 88Varde | 2-8-18-32-18-8-2 |
Galvenais kvantu skaitlis atbilst apvalkam, kurā atrodas elektrons, atšķiroties no 1, jo izmantojot elektronisko izplatīšanu, mēs pamanām, ka elektrona atrašanās vieta ir no otrā apvalka vai n = 2.
III - PAREIZI. Elementa atrašanās vieta noteiktā periodā ir saistīta ar slāņu skaitu, veicot elektronisko izplatīšanu.
| Periodi | 7 horizontālas secības |
| 1. periods | 1 slānis: K |
| 2. periods | 2 slāņi: K, L |
| 3. periods | 3 slāņi: K, L, M |
| 4. periods | 4 slāņi: K, L, M, N |
| 5. periods | 5 slāņi: K, L, M, N, O |
| 6. periods | 6 slāņi: K, L, M, N, O, P |
| 7. periods | 7 slāņi: K, L, M, N, O, P, Q |
Piemērs: ķīmiskais elements, kas atrodas otrajā periodā.
IV - nepareizi. Elementiem, kas pieder tai pašai grupai, ir līdzīgas īpašības, un tas ir saistīts ar faktu, ka tiem valences apvalkā ir vienāds elektronu skaits.
Piemērs:
| Berilijs | Magnijs |
|
2 elektroni iekšā valences slānis. |
2 elektroni iekšā valences slānis. |
Tāpēc berils un magnijs ir periodiskās tabulas 2. grupas daļa.
3. jautājums
(Unitins) Attiecībā uz mūsdienu periodisko elementu klasifikāciju identificējiet patieso apgalvojumu:
a) ģimenē elementiem pēdējā apvalkā parasti ir vienāds elektronu skaits.
b) periodiskajā tabulā ķīmiskos elementus novieto atomu masu dilstošā secībā.
c) ģimenē elementiem ir ļoti dažādas ķīmiskās īpašības.
d) vienā periodā elementiem ir līdzīgas ķīmiskās īpašības.
e) visi reprezentatīvie elementi pieder periodiskās tabulas B grupai.
Pareiza alternatīva: a) ģimenē elementiem pēdējā čaulā parasti ir vienāds elektronu skaits.
a) PAREIZI. Vienas ģimenes ķīmiskajiem elementiem pēdējā čaulā ir vienāds elektronu skaits, un tas viņiem padara līdzīgas īpašības.
b) nepareizi. Atomu masas palielinās, palielinoties elementa atomu skaitam.
c) nepareizi. Elementu ķīmiskās īpašības ir līdzīgas, tāpēc tās ir sagrupētas vienā ģimenē.
d) nepareizi. Vienā laikā elementiem to elektroni ir sadalīti vienā un tajā pašā čaulu skaitā.
e) nepareizi. Reprezentatīvie elementi pieder A grupai, kas atbilst ģimenēm: 1A, 2A, 3A, 4A, 5A, 6A, 7A un 8A. B grupai piederošie elementi ir pārejas elementi.
4. jautājums
(Vunesp) Ņemot vērā ķīmisko elementu īpašības un periodisko tabulu, nav pareizi apgalvot:
a) metāls ir viela, kas vada elektrisko strāvu, ir elastīga un kaļama.
b) nemetāls ir viela, kas nevada elektrisko strāvu, nav kaļama un kaļama.
c) semimetālam ir metāla fiziskais izskats, bet ķīmiskais raksturojums ir līdzīgs nemetāla raksturīgajam.
d) lielāko daļu ķīmisko elementu veido nemetāli.
e) cēlās gāzes ir monoatomiskas.
Nepareiza alternatīva: d) lielākā daļa ķīmisko elementu ir nemetāli.
Ievērojiet periodisko tabulu ķīmisko elementu klasifikāciju metālos, nemetālos un pusmetālos.

Kā redzam, lielākā daļa elementu ir metāli.
a) PAREIZI. Metāli elektrību vada to struktūrai raksturīgo elektronu mākoņu dēļ, ko veido brīvie elektroni. Tie ir elastīgi, jo tie var pārvērsties par vadiem vai loksnēm atkarībā no reģiona, kurā tiek izdarīts spiediens. Tie ir arī kaļami, jo ar šāda veida materiālu var izgatavot ļoti plānas loksnes.
b) PAREIZI. Nemetāliem ir pretējas metālu īpašības. Vadītāju vietā tie ir labi siltumizolatori, un, tā kā tie ir trausli, tie nav veidoti vados vai loksnēs, jo tiem nav laba elastība un kaļamība.
c) PAREIZI. Semimetāliem ir raksturīgas pazīmes starp metāliem un nemetāliem. Būdami elektrības pusvadītāji, tiem ir metāla spīdums, bet tie ir trausli kā nemetāli.
d) nepareizi. Lielākā daļa elementu tiek klasificēti kā metāli. Metālu klases, kas atrodas periodiskajā tabulā, ir: sārmains, sārmains, iekšējais un ārējais pārejas posms.
e) PAREIZI. Cēlās gāzes ir monoatomiskas, tāpēc tās attēlo tikai to iniciāļi.
Piemērs:
| cēlgāze | halkogēns |
| Hēlijs (viņš) | Skābeklis (O2) |
| monoatomisks: veido atoms | diatomisks: veido divi atomi |
Cēlgāzu stabilitātes dēļ šīs saimes elementiem ir zema reaktivitāte, un tos sauc arī par inertiem.
5. jautājums
Atbildiet par pašreizējās periodiskās tabulas organizāciju:
a) Kas ir kolonnas?
b) Kādas ir līnijas?
c) Kādu metodi izmanto ķīmisko elementu organizēšanai?
Atbildes:
a) kolonnas ir periodiskās tabulas grupas, kuras agrāk sauca par ģimenēm, kurās apvienoti ķīmiskie elementi ar līdzīgām īpašībām.
b) Līnijas ir periodiskās tabulas periodi, un tie norāda atoma elektronisko slāņu skaitu pamatstāvoklī.
c) Ķīmiskie elementi pašreizējā periodiskajā tabulā ir sakārtoti augošā secībā pēc atomu skaita, kas norāda protonu skaitu atoma kodolā.
Periodiskās tabulas ģimenes
jautājums 1
(CESGRANRIO) Veicot asociāciju starp zemāk esošajām kolonnām, kas atbilst elementu grupām saskaņā ar periodisko tabulu, skaitliskā secība būs šāda:
| 1. cēlās gāzes | • 1.A grupa |
| 2. sārmu metāli | • 2.A grupa |
| 3. sārmu zemes metāli | • 6.A grupa |
| 4. Halkogēni | • 7.A grupa |
| 5. Halogēni | • 0 grupa |
a) 1, 2, 3, 4, 5.
b) 2, 3, 4, 5, 1.
c) 3, 2, 5, 4, 1.
d) 3, 2, 4, 5, 1.
e) 5, 2, 4, 3, 1.
Pareiza alternatīva: b) 2, 3, 4, 5, 1.
| grupas | elektroniskā konfigurācija |
| • 1.A grupa: 2. sārmu metāli | mums1 (ar n |
| • 2.A grupa: 3. sārmu zemes metāli | mums2 (ar n |
| • 6.A grupa: 4. Halkogēni | mums2np4 |
| • 7.A grupa: 5. Halogēni | mums2np5 |
| • 0 grupa: 1. cēlās gāzes | 1.s2 (Viņš) vai mēs2np6 (ja n> 1) |
2. jautājums
(UECE) Ķīmiskā elementa ar Z = 54 valences slānī ir 5s konfigurācija2 5.lpp6. Elementi ar Z = 52 un ar Z = 56 pieder pie:
a) halogēnus un sārma zemi
b) halogēni un sārmi
c) halogēni un sārma zeme
d) halogēni un sārmi
Pareiza alternatīva: a) halogēni un sārmu zemes.
Ņemot vērā atomu skaitļus, mēs veicām elektronisko izplatīšanu un atradām šādus rezultātus:
| 54X un | 52Jūs | 56Ba |
|
8 elektroni iekšā valences slānis |
6 elektroni iekšā valences slānis |
2 elektroni iekšā valences slānis |
| Cēlās gāzes: 8A ģimene | Halkogēni: 6A ģimene | Sārma zeme: 2A ģimene |
3. jautājums
(F. Ibero-Americana-SP) Periodisko tabulu grupa, kurai raksturīga mākslīgo elementu pārsvars, ir šāda:
a) lantanīdi
b) cēlgāzes
c) pārejas metāli
d) sārmu zemes metāli
e) aktinīdi
Pareiza alternatīva: e) aktinīdi.
Mākslīgie elementi ir tie, kuru dabā nav un kuri laboratorijā ir sintezēti kodolreakciju ceļā.
Tos sauc arī par transurāna elementiem, jo šo radioaktīvo elementu atomu skaits ir lielāks par 92, kas atbilst urānam.
Parasti šie elementi ir īslaicīgi, un tie ilgst līdz sekundes daļām.
Saskaņā ar šo informāciju mums:
Dabā sastopamie elementi ir: lantanīdi, cēlgāzes, pārejas metāli un sārmu zemes metāli. Izņemot tehnēciju un prometiju, kas ir mākslīgi.
Mākslīgo elementu pārsvars ir aktinīdi, kas klasificēti kā iekšējie pārejas metāli un ievietoti periodiskajā tabulā zem lantanīdiem. No šīs sērijas dabiski ir tikai aktīnijs, torijs, protaktīnijs un urāns.
4. jautājums
(U. Salvadoras katoļu baznīca-BA) X suga2- ar 8 elektroniem visattālākajā apvalkā (valences apvalkā) tas var būt no elementa X, kas periodiskajā tabulā pieder grupai:
a) 7A
b) 6A
c) 2A
d) 1A
e) 8A
Pareiza alternatīva: b) 6A.
Saskaņā ar okteta likumu, lai elements iegūtu stabilitāti, tas pieņem cēlgāzes elektronisko konfigurāciju, kuras valences apvalkā ir 8 elektroni.
Uzlādējiet 2- par X sugu2- norāda, ka elements ir ieguvis 2 elektronus.
To sugu elektronu konfigurācija, kuru vistālākajā apvalkā ir 8 elektroni, ir ns2np6.
Zaudējot divus elektronus, elements atgriežas pamatstāvoklī ar ns elektronu konfigurāciju2np4.
Valences apvalkā esošie 6 elektroni ir raksturīgi halogēniem, 6A ģimenes elementiem.
Piemēram:
| Elements: skābeklis | elektroniskā konfigurācija |
| 8O | 1.s22s22. lpp4 |
| O suga2- | 1.s22s22. lpp6 |
Uzziniet vairāk par Periodiskās tabulas ģimenes.
Ķīmiskie elementi
jautājums 1
(CESGRANRIO) Ņemot vērā atomu skaitļu 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 un 75 elementus, iespēja, kas satur tikai sārmu metālus, ir:
a) 3, 11, 37 un 55
b) 3, 9, 37 un 55
c) 9, 11, 38 un 55
d) 12, 20, 38 un 56
e) 12, 37, 47 un 75
Pareiza alternatīva: a) 3, 11, 37 un 55
Sārmu metāli atbilst ķīmiskajiem elementiem, kas elektronisko izplatīšanu beidz ar elektronu s apakšlīmenī.
Elektroniski sadalot dotos atomu numurus, mums ir šādi sārmu metāli:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| Litijs | Nātrijs | Rubīdijs | Cēzijs |
Pārējie atomu skaitļi atbilst šādu grupu elementiem:
Sārmu zemes metāli: pārtrauc elektronisko izplatīšanu apakšlīmenī s2.
| Z = 12 | Z = 38 | Z = 56 |
| Magnijs | Stroncijs | Bārijs |
Pārejas metāli: pārtrauc elektronisko izplatīšanu d apakšlīmenī.
| Z = 30 | Z = 47 | Z = 75 |
| Cinks | Sudrabs | Renijs |
Halogēni: pārtrauc elektronisko izplatīšanu apakšlīmenī p5.
| Z = 9 |
2. jautājums
(Unirio) “Eloi ievietoto mākslīgo sirdi sāka attīstīt pirms četriem gadiem Amerikas Savienotajās Valstīs, un to jau izmanto aptuveni 500 cilvēku. Komplektu, ko sauc par Sirdsbiedru, veido trīs galvenie gabali. Vissvarīgākais ir četru mārciņu apaļa soma, kuras diametrs ir 12 centimetri un biezums ir 3 centimetri un kas izgatavota no titāna - sudraba-balta metāla, viegla un izturīga. ” Žurnāls Veja, 1999. gada jūlijs.
Starp zemāk esošajiem metāliem tas, kura pēdējā slānī elektronu skaits ir vienāds ar titānu, ir:
a) C
b) In
c) Ga
d) Mg
e) Xe
Pareiza alternatīva: d) Mg.
| Titāns | elektroniskā konfigurācija | Slāņu sadalījums |
| 22Jūs | 1.s2 2s2 2. lpp6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
No titāna elektroniskās izplatīšanas mēs redzam, ka šī elementa pēdējā apvalkā ir 2 elektroni.
| Elements | elektroniskā konfigurācija | Slāņu sadalījums |
| 6Ç | 1.s2 2s2 2. lpp2 | 2, 4 |
| 11Plkst | 1.s2 2s2 2. lpp6 3s1 | 2, 8, 1 |
| 31Ga | 1.s2 2s2 2. lpp6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12mg | 1.s2 2s2 2. lpp6 3s2 | 2, 8, 2 |
| 54X un | 1.s2 2s2 2. lpp6 3s2 3p6 3d10 4s2 4p6 4.d10 5s2 5.lpp6 | 2, 8, 18, 18, 8 |
Elements, kura pēdējā apvalkā ir arī 2 elektroni, ir magnijs.
3. jautājums
(UFPA) Apsveriet noteiktu ķīmisko elementu, kura enerģētiskākais apakšlīmenis ir 5s2. Tās atomu skaits un grupa, kurā tas atrodas, ir:
a) 20; 1A
b) 20; 2A
c) 38; 2A
d) 38; 1A
e) 39; 2A
Pareiza alternatīva: c) 38; 2A
Veicot elektronisko izplatīšanu, mēs noskaidrojām, ka:
- Ķīmiskais elements atrodas ģimenē 2A, jo tam ir visenerģiskākais apakšlīmenis s2
- Ir atomu skaitlis 38, kas atbilst kopējam izplatīto elektronu skaitam.
- Tas atrodas piektajā periodā, jo elektroniskā izplatīšana tika veikta līdz piektajam slānim.
Pārbaudot šo informāciju periodiskajā tabulā, mēs varam apstiprināt, ka tas ir stroncija elements.
4. jautājums
(UFC) x atomam ir vēl viens protons nekā y atomam. Pamatojoties uz šo informāciju, nosakiet pareizo paziņojumu.
a) Ja y ir sārma zeme, x ir sārma metāls.
b) Ja y ir cēlgāze, x ir halogēns.
c) Ja y ir pārejas metāls, x ir cēlgāze.
d) Ja y ir cēlmetāla gāze, x ir sārma metāls.
e) x atrodas tajā pašā periodā pirms atoma y periodiskajā tabulā.
Pareiza alternatīva: d) Ja y ir cēlmetāla gāze, x ir sārma metāls.
Periodiskā tabula ir sakārtota atomu skaita augošā secībā.
Ja Y ir atomu skaitlis z un X ir vēl viens protons nekā tas, tas nozīmē, ka šie divi elementi atrodas vienā periodā un X ir pēc Y.
Piemērs:
| Elements | nākamais elements |
| zJā | z + 1X |
| 11Plkst | 12mg |
Abi elementi atrodas 3. periodā, un magnijā ir vēl viens protons nekā nātrijā.
Saskaņā ar šo pamatojumu mums:
a) nepareizi. Sārmu metāls atrodas periodiskās tabulas sārma metāla priekšā. Pareizais apgalvojums būtu šāds: Ja y ir sārma metāls, x ir sārma zeme.
b) nepareizi. Halogēns nāk pirms periodiskās tabulas cēlgāzes. Pareizais apgalvojums būtu šāds: Ja y ir halogēns, x ir cēlgāze.
c) nepareizi. Pārejas metālus un cēlās gāzes atdala citi ķīmiskie elementi, tāpēc tie nav secīgi.
d) PAREIZI. Cēlās gāzes ir periodiskās tabulas pēdējā grupa, bet sārmu metāli - pirmā, tāpēc tās ir secīgas.
Piemērs:
| cēlgāze | sārmu metāls |
| zJā | z + 1X |
| 2viņš | 3lasīt |
Litijā, sārmu metālā, ir vēl viens protons nekā hēlijā, kas ir cēlmetāla gāze.
e) nepareizi. X atrodas tajā pašā periodā kā Y tikai pēc tā, nevis iepriekš, kā norāda alternatīvā.
5. jautājums
Pēc ķīmiskā elementa atomu skaita var uzzināt:
a) neitronu skaits kodolā
b) elektronu skaits elektrosfērā
c) serdes masa
Atbilde: b) elektronu skaits elektrosfērā
Atoms pamatstāvoklī ir elektriski neitrāls. Tātad, zinot atomu skaitli, kas atbilst protonu (pozitīvi lādētu daļiņu) skaitam, mēs zinām elektronu (negatīvi lādētu daļiņu) skaitu elektrosfērā.
Piemēram, dzelzs atoma skaitlis ir 26, tāpēc pamatstāvoklī tam ir 26 elektroni ap kodolu.
Uzziniet vairāk par ķīmiskie elementi tas ir atomu skaitlis.
Periodiskās un aperiodiskās īpašības
jautājums 1
Spriediet, vai apgalvojumi, kas saistīti ar elementu periodiskajām īpašībām, ir patiesi (T) vai nepatiesi (F).
() Atkarīgs no elementu atomu masām.
() Tie tiek atkārtoti vairāk vai mazāk regulāri intervālos attiecībā pret atomu skaita pieaugumu.
() Ir līdzīgi tajā pašā elementu grupā.
() Ir līdzīgi tajā pašā elementu periodā.
() Tajā pašā grupā periodisko īpašību skaitliskās vērtības vienmēr palielinās, kad palielinās elementu atomu skaits.
Pareizā secība ir:
a) V - F - V - F - F
b) V - F - F - V - V
c) F - V - V - F - F
d) F - V - F - V - V
e) V - F - F - V - F
Pareiza alternatīva: c) F - V - V - F - F
(FALSE) Atkarīgs no elementu atomu masas.
Saskaņā ar Moseley periodiskuma likumu daudzas ķīmisko elementu fizikālās un ķīmiskās īpašības atšķiras atkarībā no atomu skaita.
(PATIESA) Tie tiek atkārtoti vairāk vai mazāk regulāros intervālos attiecībā pret atomu skaita pieaugumu.
Tādas īpašības kā atomu rādiuss, atomu tilpums, blīvums, kušanas temperatūra un vārīšanās ir tādu īpašību piemēri, kuras periodiskajā tabulā regulāri atkārtojas.
(PATIESA) Ir līdzīgi tajā pašā elementu grupā.
Periodisko tabulu grupas ir sakārtotas ar elementiem, kuriem ir līdzīgas īpašības.
(FALSE) Ir līdzīgi tajā pašā elementu periodā.
Īpašības ir līdzīgas ģimenēs, nevis periodos. Periodos elementi tiek sadalīti pēc elektronisko slāņu skaita.
(FALSE) Tajā pašā grupā periodisko īpašību skaitliskās vērtības vienmēr palielinās, kad palielinās elementu atomu skaits.
Īpašības var palielināties vai samazināties atkarībā no atomu skaita. Piemērs tam ir elektronegativitāte, kas samazinās, palielinoties atomu skaitam attiecīgajā grupā.
Lasiet arī: Periodiskās īpašības
2. jautājums
(FAESP) Elementu aperiodiskās īpašības ir:
a) blīvums, atomu tilpums un atomu masa.
b) kušanas temperatūra, elektronegativitāte un īpatnējais siltums.
c) atomu tilpums, atomu masa un kušanas temperatūra.
d) atomu masa, īpatnējais siltums un kušanas temperatūra.
e) atomu masa un īpatnējais siltums.
Pareiza alternatīva: e) atoma masa un īpatnējais siltums.
Aperiodiskās īpašības tiek atkārtotas regulāri.
Atomu masa ir atoma svara mēra atoma masas vienībās, kas atbilst oglekļa-12 masas.
Īpatnējais siltums nosaka siltuma daudzumu, kas nepieciešams, lai 1 g elementa temperatūru paaugstinātu par 1 ° C.
Šīs divas īpašības nav saistītas ar elementa pozīciju periodiskajā tabulā.
Pārējās īpašības tiek klasificētas kā periodiskas, jo tās palielinās vai samazinās līdz ar atomu skaitu. Vai viņi:
- Blīvums: norāda koeficientu starp elementa masu un tilpumu.
- Atomu tilpums: attēlo atomu kopas tilpumu un ietekmē attālumu starp tiem.
- Kušanas temperatūra: temperatūra, kurā notiek pāreja no cietas uz šķidrumu.
- Elektronegativitāte: atoma spēja piesaistīt sev elektronisko pāri, kuru tas kopīgi saista.
Lasiet arī: elektronegativitāte un Elektroniskā interese
3. jautājums
Kuras no šīm diagrammām, kas saistītas ar periodisko tabulu, ir pareizas?
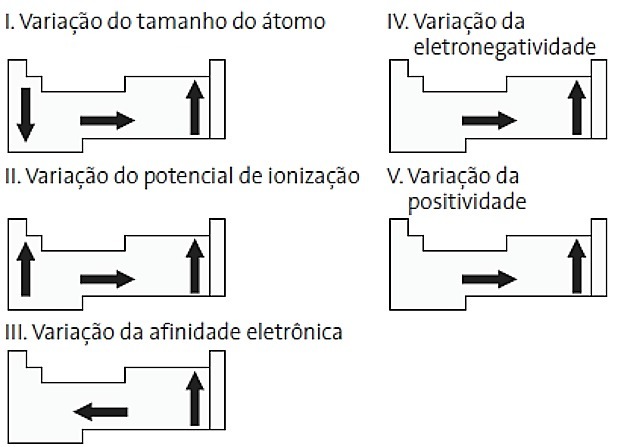
a) II un V
b) II un III
c) es un V
d) II un IV
e) III un IV
Pareiza alternatīva: d) II un IV.
Es Nepareizi. Atoma lieluma variāciju mēra pēc vidējā attāluma no kodola līdz visattālākajam elektronam. Lielākie atomi atrodas tabulas apakšā, tāpēc pieaugums notiek atbilstoši atomu skaitam, un pareizais attēlojums ir:
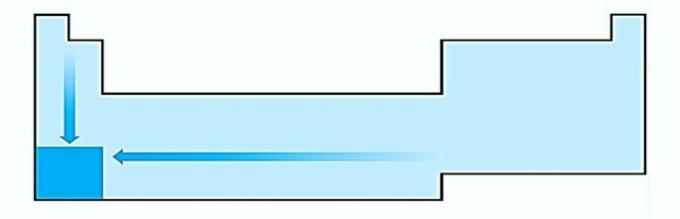
II. PAREIZI Enerģiju, kas nepieciešama, lai gāzveida stāvoklī noplēstu elektronu no izolēta atoma, sauc par jonizācijas potenciālu. Tas palielinās, kā parādīts paziņojumu diagrammā.
III. Nepareizi. Elektrona afinitāte izsaka enerģiju, kas izdalās, kad neitrāls atoms gāzveida stāvoklī saņem elektronu, kas ir ļoti svarīgs nemetālu īpašums. Vislielākās elektroniskās afinitātes novēro halogēnos un skābeklī.
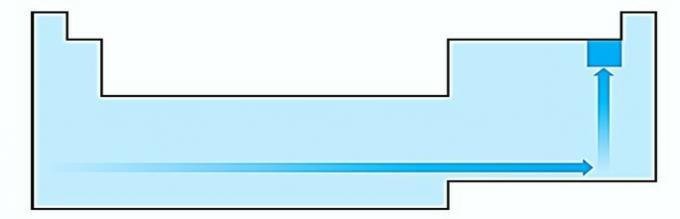
IV. PAREIZI Elektronegativitāte ir saistīta ar jonizācijas potenciālu un elektronu afinitāti. Halogēni kā tādi ir visvairāk elektronegatīvie elementi periodiskajā tabulā.
V. Nepareizi. Elektropozitivitāte notiek pretēji elektronegativitātei. Tas atspoguļo atoma spēju atteikties no elektroniem.
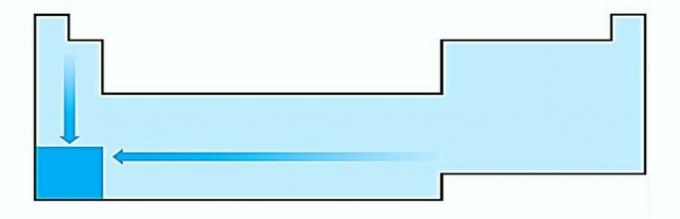
Tāpēc sārma metāliem ir visaugstākā elektropozitivitāte.
Pārbaudiet savas zināšanas, izmantojot šādus sarakstus:
- Vingrinājumi ar ķīmiskajām saitēm
- Elektroniskās izplatīšanas vingrinājumi
- Vingrinājumi par atomu modeļiem
- Termoķīmijas vingrinājumi


