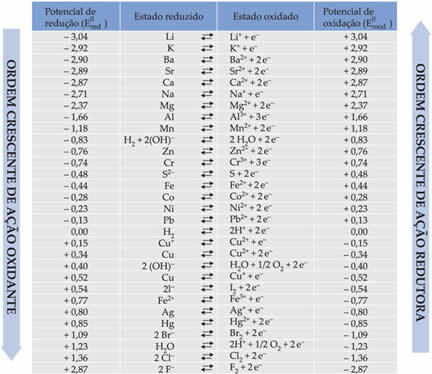
druskos tiltas pasiūlė anglų chemikas Fredericas Daniellas 1836 m., kai šis mokslininkas įsteigė baterija pavadintas jo vardu (Danilo krūva). šis tiltas yra U formos vamzdis, turintis du akytus galus. (sudarytas iš medvilnės arba agaro-agaro) ir jame yra vandens ir druskos suformuotas vandeninis tirpalas. Jis netiesiogiai sujungia dviejų ląstelės ląstelių (anodo ir katodo) tirpalus.
Stebėjimas: Anodas yra neigiamas akumuliatoriaus polius ir yra oksidacijos vieta, o katodas yra teigiamas polius ir kur vyksta redukcija.
Norint suprasti druskos tilto svarbą, iš pradžių būtina suprasti krūvos veikimą. Žr. Toliau pateiktą diagramą:
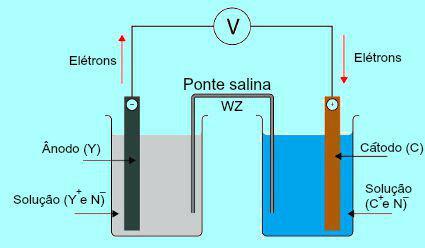
Bendroji „Daniell“ kamino schema
Iš pradžių anode esančios plokštės metalas (Y) oksiduojasi. Vykstant oksidacijai, metalas virsta katijonu, kuris patenka į tirpalą, kuriame yra plokštė. Dėl šios priežasties anodo tirpale pradeda būti didesnė katijonų koncentracija (Y+). Šiuo atveju pastebimas anodo metalinės plokštės sumažėjimas.
Y → ir- + Y+
Tada anodo plokštės metalo oksidacijos metu prarasti elektronai eina per išorinę elektros laidą ir eina į metalinę plokštę, esančią katode. Taigi, katode esanti plokštė įkraunama elektronais.
-
Šie katijonai (C.+) tirpale juda link katodo plokštės, nes ji yra įkrauta elektronais. Katijonai, gaudami plokštelėje esančius elektronus, tampa neutralūs (stabilūs ir tvirti) ir prie jų laikosi. Dėl šios priežasties katodo tirpale yra didesnė anijonų nei katijonų koncentracija. Šiuo atveju pastebimas katodo metalinės plokštės dydžio padidėjimas.
Nesustokite dabar... Po reklamos yra daugiau;)
Ç+ + ir- → C
Iš supratimo, kaip Danielio krūva, galima pastebėti, kad anode esantis tirpalas gauna didesnį kiekį Y katijonų+ dėl X plokštės metalo oksidacijos. Kita vertus, katode esantis tirpalas praranda katijonus (C.+), nes jiems sumažėja apnašų.
Būtent šiuo klausimu pabrėžiamas druskos tilto darbas. Pagrindinė šio tilto funkcija yra skatinti krūvių, esančių tiek anodo, tiek katodo tirpaluose, pusiausvyrą. Druskos tiltelyje mes visada turime druską (paprastai kalio chloridą arba amonio nitratą), atsiribojusią vandenyje. Žr. Druskos tilto lygties vaizdą:
WZ + H2O → W+ + Z-
Druskos tiltelyje yra du jonai (W+ ir Z-), kurie perkeliami į katodą ir anodą pagal:
) Anodas priima anijonus (Z-), esantį druskos tiltelyje dėl elemento (Y) oksidacijos, dėl kurio padidėja katijonų (Y+) tirpale.
B) Katodas gauna katijonus (W+), nes veikiant akumuliatoriui katijonas (C+), esantis tirpale, lentoje sumažėja. Taigi katodo tirpale yra didesnis anijonų kiekis (N-), todėl gauna druskos tiltelyje esantį katijoną.
Mano. Diogo Lopes Dias
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
DIENOS, Diogo Lopes. „Burių tiltas“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/ponte-salina.htm. Žiūrėta 2021 m. Birželio 28 d.