osmoso slėgis tai yra koligatyvinė savybė, atitinkanti slėgį, kurį reikia daryti sistemai, kad osmosas neatsirastų savaime.
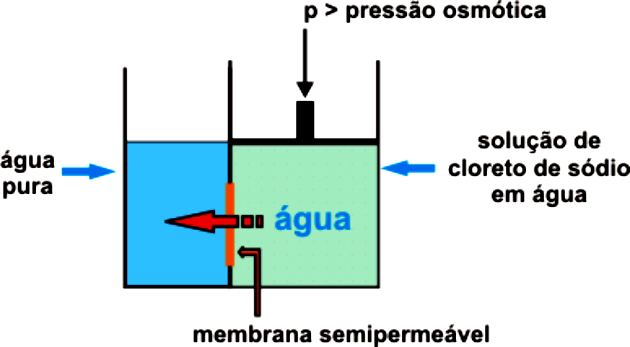
Osmosas yra vandens prasiskverbimas iš mažiau koncentruotos (hipotoniškos) į labiau koncentruotą (hipertoninę) terpę per pusiau laidžią membraną, kol pasiekiama pusiausvyra.
Norint, kad osmosas neprasidėtų ir vyktų natūraliai, reikia daryti išorinį spaudimą labiau koncentruotam tirpalui, užkertant kelią tirpiklio prasiskverbimui į labiau koncentruotą terpę. Tai osmosinis slėgis.
Kuo koncentruotesnis tirpalas, tuo didesnis osmosinis slėgis turėtų būti. Todėl osmosinis slėgis yra proporcingas ištirpusios medžiagos koncentracijai.
Kaip apskaičiuoti osmosinį slėgį?
Kiekvienas tirpalas turi skirtingą osmosinio slėgio vertę. Osmosinį slėgį galima apskaičiuoti pagal šią formulę:
π = M. A. T. i
Kur mes turime šiuos kintamuosius:
π = osmosinis slėgis;
M = koncentracija mol / l;
R = universali dujų konstanta, kurios vertė atitinka 0,082 atm. L. mol-1. K.-1 arba 62,3 mm Hg L. mol-1. K.-1;
T = temperatūra absoliučioje skalėje (Kelvinas);
i = Van’t Hoffo faktorius, kuris apima santykį tarp bendro galutinių ir pradinių dalelių skaičiaus joniniuose tirpaluose.
Mankšta išspręsta
1. (Puccamp-SP) Kartais 0,30 M gliukozės tirpalas naudojamas švirkščiant į veną, nes jo osmosinis slėgis yra artimas kraujo slėgiui. Koks yra osmosinis slėgis atmosferose esant 37 ° C temperatūrai?
a) 1,00.
b) 1,50.
c) 1.76.
d) 7,63.
e) 9,83.
Atsižvelgdami į klausimo pateiktus duomenis, turime:
M = 0,30 mol / l;
R = 0,082 atm. L. mol-1. K-1
T = 37 ° + 273 = 310 K
Dabar turite taikyti šias reikšmes osmosinio slėgio apskaičiavimo formulei:
π = M. A. T. i
π = 0,30. 0,082. 310
π = 7,63 atm (Alternatyva)
Sprendimų klasifikacija
Tirpalus galima suskirstyti į tris tipus pagal osmosinį slėgį:
- hipertoninis sprendimas: Turi didesnį osmosinį slėgį ir tirpiųjų medžiagų koncentraciją.
- izotoninis tirpalas: Kai tirpalai turi tą patį osmosinį slėgį.
- hipotoninis tirpalas: Turi mažesnį osmosinį slėgį ir tirpiųjų medžiagų koncentraciją.

Osmosinio slėgio svarba gyvoms būtybėms
Druskos tirpalas yra medžiaga, paruošta pagal osmosinio slėgio principus. Jis turi būti naudojamas esant osmosiniam slėgiui, lygiam tam, kuris randamas kūne, taip išvengiama Raudonosios ląstelės nepatirkite hemolizės ar nesusiglamžykite.
Kraujo osmosinis slėgis yra maždaug 7,8 atm. Todėl, norint tinkamai funkcionuoti organizme, raudonieji kraujo kūneliai turi turėti tą patį osmosinį slėgį, užtikrinantį normalų vandens srautą į ląsteles ir iš jų.
Pvz., Esant dehidracijai, nurodomas druskos tirpalo naudojimas, kuris turi būti izotoninis kraujo ląstelių ir kitų kūno skysčių atžvilgiu.
Druskos tirpalas atlieka kūno osmosinės pusiausvyros grąžinimo funkciją. Taip yra todėl, kad dehidracijos metu kraujas tampa labiau koncentruotas nei ląstelių vidus, todėl jos nudžiūsta.
Osmosas ir atvirkštinis osmosas
Kaip matėme, osmosas tai yra vandens praleidimo iš hipotoninės į hipertoninę aplinką procesas per pusiau laidžią membraną, kol pasiekiama pusiausvyra tarp koncentracijų.
Tuo tarpu atvirkštinė osmozė tai medžiagų išskyrimo procesas per membraną, kuri sulaiko ištirpusį medžiagą. Tirpiklis teka iš labiau koncentruotos terpės į mažiau koncentruotą terpę ir yra ištirpęs nuo ištirpusios medžiagos membrana, leidžiančia ją praeiti.
Tai atsitinka tik dėl daromo slėgio, todėl pusiau pralaidi membrana leidžia praleisti tik vandenį, išlaikydama ištirpusią medžiagą. Šis slėgis turi būti didesnis už natūralų osmosinį slėgį.
Pavyzdžiui, jei taikomas osmosinis slėgis yra didesnis nei būtina, atsiras atvirkštinis osmosas. Taigi srautas praeis iš terpės, kurioje yra didžiausia koncentracija, į tą, kurios koncentracija yra mažiausia.