Paviršiaus įtempimas yra reiškinys, atsirandantis ant skysčių, tokių kaip vanduo, paviršiaus, suformuojant ploną plėvelę.
Kai skystos būsenos vanduo užima indą, galime suvokti skysčio ir aplinkos atskyrimą. Taip yra todėl, kad vandens molekulių sąveika paviršiuje skiriasi nuo sąveikos skysčio viduje.
Paviršiuje vandens molekulė sąveikauja su molekulėmis šonuose ir apačioje. Viduje molekulę supa kitos molekulės, o vandenilio jungtimis vyksta sąveika visomis kryptimis.
Būtent dėl šios savybės mes stebime lašelio susidarymo reiškinį. Dėl šios priežasties vabzdžiai taip pat gali vaikščioti vandeniu.
Kas yra paviršiaus įtempimas?
Tai yra plonos plėvelės susidarymas po skysčiu dėl traukos nelygybės tarp jį sudarančių molekulių. Šis reiškinys ryškiau pasireiškia skysčiuose, kurie turi tarpmolekulinės jėgos intensyvus, kaip vanduo.
Sąveika tarp rūšių skystyje vadinama darniomis jėgomis. Skysčio viduje esančios molekulės visomis kryptimis traukia kaimynines molekules, o paviršiuje esančios molekulės sąveikauja su molekulėmis žemiau ir šalia jų.
Pažiūrėkite, kaip susidaro paviršiaus įtempimas vandenyje.
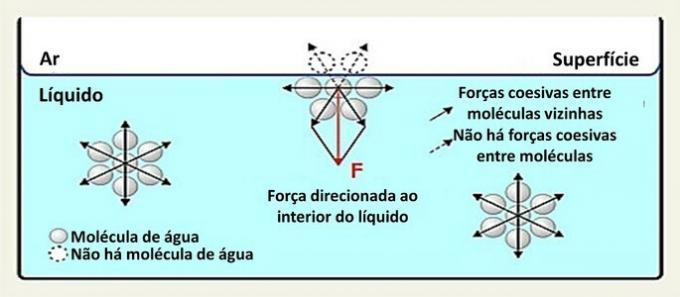
Vanduo (H2O) yra polinė molekulė, susidedanti iš 2 vandenilio atomų (teigiamų polių) ir vieno deguonies atomo (neigiamo poliaus), sujungtų kovalentiniai ryšiai. Teigiamą molekulės polių pritraukia kaimyninės molekulės neigiamas polius, formuojant vandenilio ryšius.
Šio tipo skysčio sąveika pasiskirsto visomis kryptimis. Paviršiuje jėgos nukreiptos žemyn ir į šonus, nes virš jų nėra vandens molekulių. Tai paverčia paviršiaus molekules darnesnėmis ir sukuria elastingą plėvelę.
Paviršiaus įtempimo vienetas nurodomas dalijant jėgos ir ilgio vienetus, dažniausiai priimant dyne / centimetras (dyne / cm) ir niutoną / metrą (N / m).
Vandens paviršiaus įtempimas yra didelis, kurio vertė yra 72,75 dyna / cm. Tačiau gyvsidabrio, skysto metalo, paviršiaus įtempimas yra maždaug 7 kartus didesnis nei vandens, 475 dyna / cm.
Norite sužinoti daugiau? Taigi patikrinkite šiuos tekstus:
- Vandens savybės
- Poliarinės ir apolinės molekulės
- Cheminiai ryšiai
Reiškiniai, kuriuos sukelia paviršiaus įtempimas
Paviršiaus įtampa yra atsakinga už kai kuriuos reiškinius, kuriuos stebime kasdieniame gyvenime. Pagrindiniai yra:
Gyvūnai, kurie vaikšto vandeniu

Vabzdžiai, vorai ir kiti gyvūnai gali vaikščioti ar ilsėtis Vanduo nes ant jo letenų galūnių yra plaukai, padengti riebia medžiaga, todėl jie negali prasiskverbti tarp vandens molekulių, kurios yra sujungtos ant paviršiaus.
Vandens lašelių susidarymas

Vandens lašai yra sferiniai dėl vandens susitraukimo molekulės paviršiaus, kurį sukelia paviršiaus įtempimas. Rutulys atsiranda todėl, kad tai yra geometrinė forma, kurioje yra mažiausias santykis tarp paviršiaus ploto ir tūrio. Todėl sferinė forma palaiko mažiausiai vandens molekulių, besiliečiančių su oru.
Vandens paviršiaus įtempimo pratimai
1. Paviršinio aktyvumo medžiaga yra medžiaga, veikianti kitą, kad pasikeistų:
a) Osmoliškumas.
b) paviršiaus įtempimas.
c) Elektroforezė.
d) Klampa.
e) Osmosinis slėgis.
Teisinga alternatyva: b) paviršiaus įtempimas.
a) NETEISINGAI. Osmoliškumas yra susijęs su ištirpusios medžiagos dalelių kiekiu, esančiu tam tikrame tirpiklio tūryje.
b) TINKAMA. Tiek plovikliai, tiek muilai sumažina vandens paviršiaus įtempimą ir paprastai vadinami paviršiaus aktyviųjų medžiagų, nes šių medžiagų molekulės yra tarp vandens molekulių ir sumažina įtampą paviršutiniškas.
c) NETEISINGAI. Elektroforezė yra molekulių atskyrimo pagal jų krūvius technika.
d) NETEISINGAI. Klampa yra fizinė savybė, lemianti skysčio atsparumą srautui.
e) NETEISINGAI. Osmosinis slėgis yra koligatyvinė savybė, atitinkanti slėgį, kurį reikia daryti sistemai, kad osmosas neatsirastų savaime.
Sužinokite daugiau apie šiame numeryje nagrinėjamas problemas:
- Materijos savybės
- Kolektyvinės savybės
- Osmoso slėgis
2. Skysčių paviršiaus įtempimas tiesiogiai priklauso nuo molekulių sąveikos procesų, pavyzdžiui, iš vandenilio jungimosi. Kurios iš žemiau esančių medžiagų paviršiaus įtempimas yra didžiausias?
a) benzenas
b) oktanas
c) etilo alkoholis
d) anglies tetrachloridas
e) etano rūgštis
Teisinga alternatyva: e) etano rūgštis.
a) NETEISINGAI. Benzenas yra angliavandenilis, nepolinė molekulė ir nesudaro vandenilio jungčių.
b) NETEISINGAI. Oktanas yra angliavandenilis, todėl jis yra nepolinė molekulė, kuri nesudaro vandenilio ryšių.
c) NETEISINGAI. Etilo alkoholis yra šiek tiek poliarinis junginys, galintis sudaryti vandenilio jungtis, tačiau molekulių sąveika yra ribota.
d) NETEISINGAI. Anglies tetrachloridas yra nepolinis organinis junginys, todėl vandenilio jungčių nesudaro.
e) TEISINGA. Karboksirūgšties funkcinė grupė (-COOH) gali užmegzti vandenilio jungtis arba su deguonimi, arba su hidroksilo vandeniliu.

Sužinokite daugiau apie šiame numeryje nagrinėjamas problemas:
- Molekulių poliškumas
- Organinės funkcijos
- Angliavandeniliai
paviršiaus įtempimo eksperimentas
Žiūrėkite toliau pateiktą vaizdo įrašą su eksperimentu, kuris parodo vandens paviršiaus įtempimą.