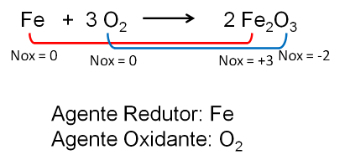
Grįžtamosios reakcijos, kuri yra pusiausvyroje, pusiausvyra bus pakeista tik įvykus bet kokiems išoriniams pokyčiams, nes pusiausvyra niekada nesikeičia savaime.
Vienas iš tokių pokyčių yra koncentracijos kitimas, kuris apima reagentų ar produktų pašalinimą arba pridėjimą.
Pažvelkime į pavyzdį:
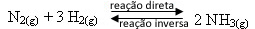
- Reagentų pridėjimas:
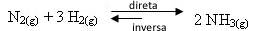
Jei į pusiausvyrą pridėsime daugiau vandenilio dujų arba daugiau azoto dujų, padidės reagentų koncentracijos ir kartu padidės tarp jų molekulių taip pat padidės efektyvūs sukrėtimai, dėl kurių padidės tiesioginės amoniako susidarymo reakcijos vystymosi greitis. (NH3 g)).
Tai reiškia, kad pridedant reagentų pusiausvyra perkeliama į dešinę pusę, link produktų susidarymo:

Tai atitinka „Le Chatelier“ principas kuris tai sako kai pusiausvyroje esančioje sistemoje atsiranda tam tikras sutrikimas, ji juda šio sutrikimo panaikinimo kryptimi, bandydama prisitaikyti prie naujos pusiausvyros.
Aukščiau nurodytu atveju atsitiks taip, kad laikui bėgant amoniako kiekis padidės ir vėl pasieks pusiausvyrą. Taigi santykis tarp produktų ir reagentų koncentracijų išliks pastovus, tai yra, pusiausvyros konstantos Kc vertė išliks ta pati.
Kc = __ [NH3]2__↑
[N2]. [H2]3 ↑
Tai atsitiks ir kitais atvejais, tai yra, jokie reagentų ar produktų koncentracijos pokyčiai nepakeis Kc vertės.
- Produktų pridėjimas:
Jei pridėsime daugiau amoniako, padidindami jo koncentraciją, dalis jo virs dujomis azotas ir vandenilis, didinant atvirkštinės reakcijos formavimosi greitį reagentai.
Nesustokite dabar... Po reklamos yra daugiau;)
Tai reiškia, kad pridedant produktų, pusiausvyra perkeliama į kairę, link reagentų susidarymo:
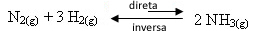
- Reagentų pašalinimas:
Jei pašalinsime vieną ar abu reagentus, sumažės jų koncentracija ir dėl to sumažės tiesioginės reakcijos vystymosi greitis. Taigi pusiausvyra bus nukreipta į daugiau reagentų susidarymą, kuris yra kairėje:
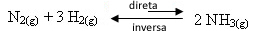
- Produkto pašalinimas:
Jei sumažinsime produktų koncentraciją, sumažės atvirkštinės reakcijos greitis, padidindamas pirmyn vykstančios reakcijos vystymosi greitį. Tai reiškia, kad balansas pasislenks į dešinę:
Trumpai tariant, galime pasakyti taip:

Svarbu pabrėžti, kad kietųjų medžiagų koncentracijos kitimas nepajudina pusiausvyros.
Taigi žemiau pateiktoje reakcijoje, jei pašalinsime arba pridėsime CO2 g) arba COg), pasikeis pusiausvyra. Bet jei mes sumažinsime arba pridėsime Cs, nieko neįvyks su cheminių medžiagų balansu:
Ç(s) + CO2 g) CO 2 COg)
Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Koncentracijos kitimas ir cheminės pusiausvyros poslinkis“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/variacao-concentracao-deslocamento-equilibrio-quimico.htm. Žiūrėta 2021 m. Birželio 28 d.