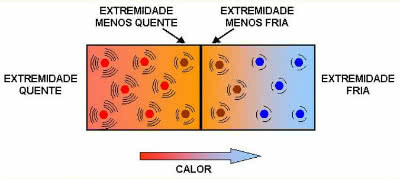
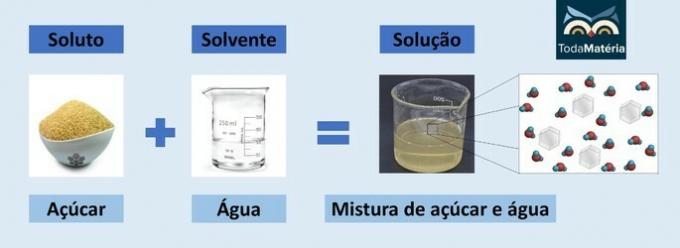
Galime tai pažymėti kai tik padidiname vieno ar visų reagentų, dalyvaujančių cheminėje reakcijoje, koncentraciją, padidėja jo vystymosi greitis, tai yra reakcijos greitis.
Taip pat yra priešingai. Pavyzdžiui, šiuo metu rekomenduojama vietoj įprasto alkoholio naudoti alkoholio gelį, nes yra mažesnė rizika jį sudeginti ir taip išvengti nelaimingų atsitikimų. Paprastas skystas alkoholis iš tikrųjų yra alkoholio ir vandens mišinys, kuriame gelio alkoholis turi mažiau alkoholio. Todėl, sumažinus vieno iš degimo reagentų koncentraciją, alkoholio atveju reakcija vyksta lėčiau. Kita vertus, kuo grynesnis alkoholis, tuo greitesnė degimo reakcija.

Kaip teigiama tekste Cheminių reakcijų atsiradimo sąlygos, viena iš reakcijos įvykimo sąlygų yra efektyvus susidūrimas tarp dalelių. Taigi, padidėjus reagentų koncentracijai, galima gauti didesnį dalelių ar molekulių kiekį vienoje erdvėje. Tai padidina susidūrimų tarp jų skaičių ir padidina tikimybę, kad įvyks efektyvūs susidūrimai, dėl kurių atsiras reakcija. Rezultatas yra tas, kad reakcija vyksta greičiau.
Nesustokite dabar... Po reklamos yra daugiau;)
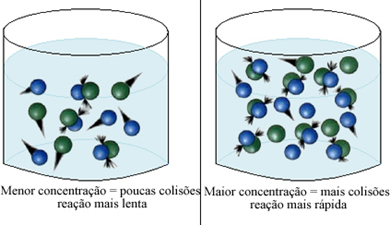
Norėdami tai pamatyti, pagalvokite apie šį pavyzdį: kai mes degame žarija ir norime, kad šis degimas vyktų greičiau, ar mes pučiame ar ventiliuojame žarijas? Kodėl tai veikia?
Na, vienas iš šios degimo reakcijos reagentų yra ore esantis deguonis. Kai mes purtome, oro srovė pašalina pelenus, kurie susidaro degimo metu, ir tai palengvina deguonies kontaktą su žarijomis. Tokiu būdu padidiname reagentų kontaktą ir pagreitiname degimo reakciją.
Trumpai tariant, mes turime:

Dirbant su dujomis, vienas iš būdų padidinti reagentų koncentraciją yra sumažinti slėgį. Tai atlikdami mes sumažiname tūrį ir dėl to padidėja reagento koncentracija.

Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Reagentų koncentracija ir reakcijų greitis“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm. Žiūrėta 2021 m. Birželio 27 d.