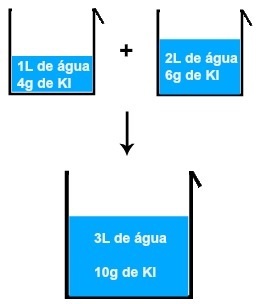
Tirpumas ir tirpiklis yra du homogeninio mišinio, vadinamo cheminiu tirpalu, komponentai.
- Tirpusyra medžiaga, kuri yra disperguota tirpiklyje. Jis atitinka medžiagą, kuri bus ištirpusi, ir paprastai tirpale būna mažesniu kiekiu.
- Tirpiklisyra medžiaga, kurioje ištirpusios medžiagos ištirps, kad susidarytų naujas produktas. Jis pateikiamas tirpale didesniu kiekiu.
Tirpumas tarp ištirpusio (disperguoto) ir tirpiklio (dispergento) vyksta sąveikaujant tarp jų molekulių.
Šių dviejų tirpalo komponentų skirtumas yra tas, kad ištirpusios medžiagos yra medžiaga, kuri ištirps, o tirpiklis yra medžiaga, kuri ištirps.
Geriausiai žinomas tirpiklis yra vanduo, laikomas tirpalu universalus tirpiklis. Taip yra todėl, kad jis gali ištirpinti didelį kiekį medžiagų.
Tirpiklis ir tirpiklio pavyzdžiai
Peržiūrėkite keletą cheminių tirpalų pavyzdžių ir suraskite kiekvieno iš jų ištirpusias medžiagas ir tirpiklius:
Vanduo ir druska
- Tirpumas: valgomoji druska - natrio chloridas (NaCl)
- Tirpiklis: vanduo
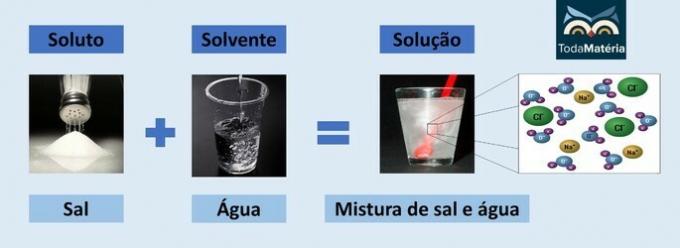
Kadangi tai joninis junginys, tirpale esantis natrio chloridas disocijuoja ir sudaro jonus, kuriuos savo ruožtu tirpina
Vanduo.Teigiamas vandens ašis (H+) sąveikauja su druskos anijonu (Cl-) ir neigiamą vandens ašį (O2-) sąveikauja su katijonu (Na+).
Tai yra tam tikro tipo elektrolitinis tirpalas, nes tirpale esančios joninės rūšys gali praleisti elektros srovę.
vandens ir cukraus
- Tirpiklis: cukrus - sacharozė (C.12H22O11)
- Tirpiklis: vanduo

Cukrus yra kovalentinis junginys ir ištirpęs vandenyje molekulės jie išsiskirsto, bet nepakeičia savo tapatybės.
Šis vandeninis tirpalas klasifikuojamas kaip neelektrolitinis, nes tirpale disperguotas tirpalas yra neutralus ir todėl nereaguoja su vandeniu.
Actas
- Tirpiklis: acto rūgštis (CH3COOH)
- Tirpiklis: vanduo

Actas yra tirpalas, kuriame yra ne mažiau kaip 4% acto rūgšties, a karboksirūgštis kuris būdamas poliarinis, vandenilio jungtimis sąveikauja su vandeniu, taip pat ir poliniu.
Svarbi tirpumo taisyklė yra tai, kad panašus ištirpsta panašus. Poliniai junginiai yra ištirpinti poliniuose tirpikliuose, o nepolinės - tirpsta nepoliniuose tirpikliuose.
Kiti sprendimai
Be skystų tirpalų, yra ir dujinių bei kietų tirpalų.
Oras, kuriuo kvėpuojame, yra dujinio tirpalo, kurio didesnės dujos yra azotas (78%) ir deguonis (21%), pavyzdys.
At metalo lydiniai jie yra tvirti sprendimai. Pavyzdžiui, žalvaris (cinkas ir varis) yra mišinys, naudojamas muzikos instrumentams gaminti.
Norite įgyti daugiau žinių? Taigi perskaitykite šiuos kitus tekstus:
- Cheminiai sprendimai
- tarpmolekulinės jėgos
- Vienarūšiai ir heterogeniniai mišiniai
Koks yra tirpumo koeficientas?
Tirpumo koeficientas yra tirpiklio, pridedamo prie tirpiklio tam tikroje temperatūroje, kad susidarytų prisotintas tirpalas, riba.
O tirpumo koeficientas kinta priklausomai nuo sąlygų ir gali padidėti arba sumažėti priklausomai nuo temperatūros pokyčių ir atitinkamo tirpalo.
Yra riba, iki kurios tirpiklis gali ištirpti.
Pavyzdys: Jei įdėsite cukraus į stiklinę vandens, pirmą akimirką pastebėsite, kad cukrus dingsta vandenyje.
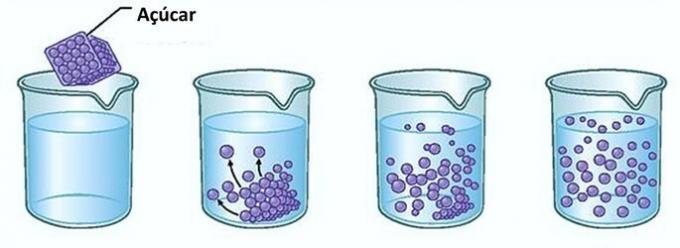
Tačiau jei toliau dėsite cukraus, pastebėsite, kad tam tikru momentu jis pradės kauptis stiklo dugne.
Taip yra todėl, kad vanduo, kuris yra tirpiklis, pasiekė ribą tirpumas ir didžiausias koncentracijos kiekis. Tirpalas, kuris lieka indo apačioje ir neištirpsta, vadinamas fono kūnas.
Stiklo dugne esantis cukraus perteklius neištirps ir neturės įtakos tirpalo koncentracijai. Be to, stiklinės dugne nusėdęs cukrus nepadarys vandens saldesnio.
Sprendimų klasifikacija
Tirpalai gali būti klasifikuojami pagal ištirpusio tirpalo kiekį. Taigi jie gali būti trijų tipų: sočiųjų, nesočiųjų ir persotintų.
- prisotinto tirpalo: Tirpalas pasiekė tirpumo koeficiento ribą, tai yra, tirpiklyje tam tikroje temperatūroje yra ištirpintas maksimalus ištirpusios medžiagos kiekis.
- nesočiųjų tirpalą: Ištirpusios ištirpusios medžiagos kiekis dar nepasiekė tirpumo koeficiento. Tai reiškia, kad galima pridėti daugiau tirpinio.
- persiotintas tirpalas: Tirpių yra daugiau nei įprastomis sąlygomis. Šiuo atveju jie sukelia nuosėdas.
Norėdami sužinoti daugiau apie sprendimus, perskaitykite šiuos tekstus.:
- Tirpalų skiedimas
- Moliškumas
- Molarizmas
- Titravimas
Tirpalų koncentracija
Pagal ištirpintą medžiagą ir tirpiklį galima apskaičiuoti tirpalo koncentraciją.
Bendra koncentracija apibrėžiama kaip ištirpusios medžiagos, ištirpintos tam tikrame tirpalo tūryje, masės santykis.
Koncentracija apskaičiuojama pagal šią formulę:
Esamas,
Ç: Koncentracija (g / l);
m: ištirpusios medžiagos masė (g);
V: tirpalo tūris (L).
Pavyzdys:
(Faap) Apskaičiuokite natrio nitrato vandeninio tirpalo, kuriame yra 30 g druskos, 400 ml tirpalo koncentraciją g / l:
Rezoliucija:
Laikykitės informacijos apie ištirpusios medžiagos ir tirpiklio kiekį. 400 ml vandeninio tirpalo (tirpiklio) yra 30 g druskos (ištirpusios medžiagos).
Tačiau tūris yra ml, ir mes turime jį pakeisti į L:
Dabar, norint sužinoti koncentraciją, tiesiog reikia taikyti formulę:
Tokiu rezultatu priėjome išvadą, kad sumaišę 30 g druskos su 400 ml vandens gausime tirpalą, kurio koncentracija yra 75 g / L.
Jei norite gauti daugiau informacijos, kaip apskaičiuoti bendrą koncentraciją, šie tekstai bus naudingi.:
- Tirpalo koncentracija
- Bendro susikaupimo pratimai