원자 부피는 원자가 차지하는 부피가 아니라 화학 원소의 주어진 원자 수의 고정 된 양이 차지하는 부피.
텍스트에서 화학 원소, 원소는 동일한 원자 번호, 즉 핵에서 동일한 양의 양성자를 갖는 원자 세트에 해당하는 것으로 나타났습니다. 원자량을 계산하기 위해 설정된 양은 아보가드로 상수, 6.02와 같습니다. 1023 원소의 1 몰에 해당하는 원자.
그래서 우리는 원자 부피는 원자 1 몰 (또는 6.02)의 부피입니다. 1023 원자)의 요소가 차지합니다.
이 양은 고체 원소의 밀도와 그 원소 원자 1 몰의 질량을 안다면 계산할 수 있습니다. 예를 들어, 나트륨 (Na)의 밀도는 0.97g / cm와 같다고 가정합니다.3 그리고 그 6.02. 1023 나트륨 원자의 질량은 23.0g입니다. 그러면 밀도의 공식에서 나트륨의 원자 부피에 도달 할 수 있습니다. 방법보기 :
밀도 = 파스타
음량
원자량 = 6.02의 질량. 1023 원소 원자
고체 요소 밀도
나트륨의 원자량 = 23.0g
0.97g / cm3
나트륨의 원자 부피 = 23.71 cm3
원자 부피 값은 원자의 크기뿐만 아니라 원자 사이의 거리도 포함합니다. 따라서 빈 공간도 포함되므로 우리는 할 수 없습니다 원자 부피 값을 원자 수 (6.02. 1023) 각 원자가 차지하는 부피를 찾습니다.
원자량은 주기적 특성, 즉 원소의 원자 번호에 따라 달라 지므로 연구하는 것이 중요합니다. 아래 이미지를보십시오. 원소의 원자 부피 위에서 아래로 성장즉, 동일한 주기율표 계열에 속하는 원소를 분석 할 때 원자 번호가 증가함에 따라 원자 부피도 증가합니다. 이는 이러한 의미에서주기가 증가하여 원자의 전자 층이 증가하고 결과적으로 원자가 차지하는 부피도 증가하기 때문입니다. 이것은 다음과 같은 성장 감각입니다. 원 자선.
반면에 수평 적으로 원자량은 중심에서 가장자리로 증가합니다. 왼쪽에서 시작하여 주기율표의 중앙으로 오른쪽으로 이동하면주기가 즉, 동일한 선의 요소는 동일한 양의 전자 층을 갖지만 원자 번호는 증가. 이것은 전자의 양 이이 방향으로 증가하여 더 큰 힘이 발생한다는 것을 의미합니다. 원자의 핵에 대한 전자의 인력, 원자 반경 감소 및 결과적으로 부피 감소 원자. 그러나 중앙에서 오른쪽으로, 이것은 계속 발생하지 않습니다. 왜냐하면이 영역에있는 요소의 경우 특히 비금속의 경우 원자 사이의 간격이 상대적으로 커서 원자량에 영향을 미칩니다. 그것을 증가시킵니다.
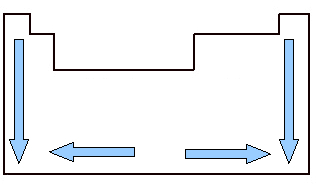
가족 및 기간에 따른 주기율표의 원자 부피 변화
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/volume-atomico.htm
