이라고 러더퍼드 모델 1911년 과학자 Ernest Rutherford가 원자에 대해 제안한 제안은 물질 구성 요소의 이상적인 형태와 구성을 입증할 목적으로 다음과 같습니다. 원자.
영형 러더퍼드 모델 그것은 일반적으로 태양계의 모델로 알려져 있습니다. 그 구조와 기능이 태양과 그 주위를 도는 행성 사이의 관계와 비교되었기 때문입니다.
그의 모델에서 Rutherford는 다음 표현에서 볼 수 있듯이 태양을 원자의 핵에 비교하고 원자의 전자를 태양계의 행성과 비교했습니다.
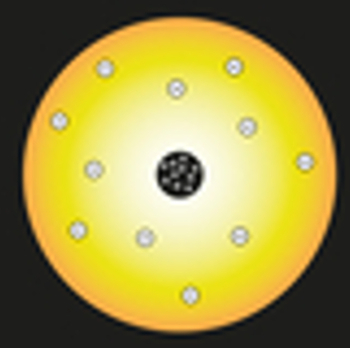
Rutherford 원자 모델의 표현
핵 내부에는 양성자(Eugen Goldstein이 발견)라고 하는 양전하를 띤 입자가 위치합니다. 이 핵은 작고 밀도가 높으며 원자의 가장 큰 질량을 가질 것입니다.
Rutherford가 수행한 실험
원자 모델의 생성에 대한 러더퍼드의 모든 제안은 알파 방사선 빔을 집중시킨 실험의 결과였습니다. 납 상자에 존재하는 방사성 폴로늄) 얇은 금판에 황화아연으로 뒤와 측면에 덮인 금속 판이 있습니다. 측면. 황화아연은 방사선을 받으면 빛나는 염입니다.
그런 다음 Rutherford는 이 실험에서 특히 세 개의 점(a, b, c)이 빛났다고 말했습니다.
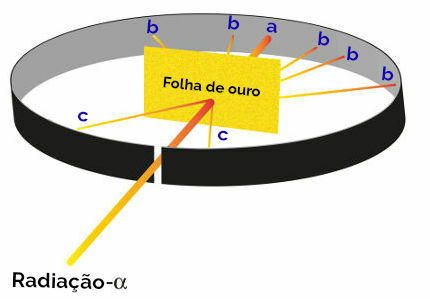
러더퍼드 실험의 표현
가리키다 (빛나는 빈도가 높음): 알파 방사선이 납 블록의 구멍 방향과 같이 아무 문제 없이 금판을 가로질러 있음을 나타냅니다.
포인트 b (작은 광선 발생): 알파 방사선이 금판을 통과했지만 교차하는 동안 편차가 있었음을 나타냅니다.
점 c (극소량의 빛): 금색 칼날 앞에 위치하여 알파 방사선이 통과하지 않았음을 나타냅니다.
Rutherford는 다음과 같이 해석하여 금판을 형성하는 원자에 이러한 관찰 결과를 돌렸습니다.
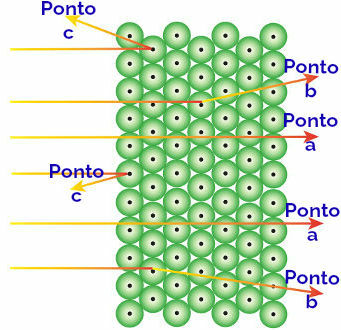
알파 방사선과 원자의 거동 표현
도달하는 알파 방사선 가리키다: 알파 방사선은 양수이고 원자의 거대한 빈 공간을 통과합니다. 또한 일부 궤도에는 전자가 있습니다.
도달하는 알파 방사선 포인트 b: 알파 방사선은 금판의 원자를 통과하지만 어느 순간에 도달합니다. 그것은 양전하를 띠는 원자의 작은 핵 가까이를 지나가면서 반발력을 발생시킵니다. 방사능.
도달하는 알파 방사선 점 c: 알파 방사선은 금판의 원자를 통과하지만 양전하를 띠는 작은 핵에 충돌하여 방사선에 반발력을 생성합니다.
러더퍼드 모델의 문제
많은 물리학자들은 Rutherford가 제안한 모델의 몇 가지 문제를 지적했습니다.
첫 번째 문제: 양전하를 띤 입자가 서로 반발한다면 어떻게 양전하를 띤 핵이 가능합니까?
두 번째 문제: 왜 전기구의 전자가 핵의 양성자에 끌리지 않습니까?
세 번째 문제: 일정한 운동을 하는 작은 물체인 전자는 왜 에너지를 잃고 핵으로 떨어지지 않는가?
* 이미지 크레딧: 스빅 / 셔터스톡
By Me 디오고 로페스 디아스
원천: 브라질 학교 - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-modelo-rutherford.htm