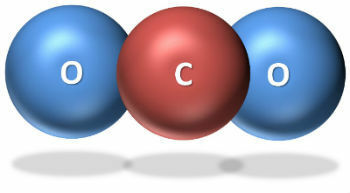
이산화탄소, 이산화탄소 또는 이산화탄소는 하나의 탄소 (C)와 두 개의 산소 (O) 원자로 구성된 분자입니다.
그것은 형태로 대기에서 발견됩니다 CO2.
Jan-Baptist Van Helmont가 1638 년에 발견 한 이산화탄소는 유기 제품의 호흡과 연소 과정에서 산소와 탄소 사이의 반응에 의해 생성됩니다.
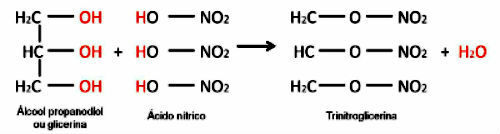
CO 형성의 화학 반응2 간단하며 다음과 같이 발생합니다.
풍모
이산화탄소는 무색, 무취, 공기보다 무거워 냄새 나 맛이 없어 환경에서 감지하기 어렵습니다.
대기 중 고농도에서, 그것은 형성하는 주요 가스 중 하나입니다 온실 효과.
이 과정의 결과로 이산화탄소는 대기 오염, 상승 온도 및 산성비.
여전히 광합성을 담당하며 연소. 그것 없이는 식물, 식물성 플랑크톤 및 조류가 광합성.
또한에 대해 읽으십시오 탄소 순환.
방송 소스

유기물의 연소는 CO 생산의 주요 원천입니다.2. 그것은 기름, 나무와 같은 제품의 연소로 인해 발생합니다. 화석 연료.
인간 활동, 특히 산업 활동은 이산화탄소 배출의 중요한 원천입니다.
발효, 유기물의 분해 및 살아있는 유기체의 호흡 과정도 CO 생성의 원천입니다.2.
화산 폭발, 삼림 벌채 및 화재도 이산화탄소를 방출합니다.
용도
천연 광합성 과정 외에도 CO2 그것은 식품 산업, 특히 탄산화라는 과정에서 음료에 사용됩니다.
이 공정은 청량 음료, 탄산수, 스파클링 와인 및 맥주 제조에 적용됩니다.
또한 드라이 아이스 (고체 이산화탄소) 생산과 소화기에도 사용됩니다.
이산화탄소는 이식을위한 장기 수송에 사용되는 조직 보존에도 근본적으로 중요합니다.
자세한 내용은 다음을 참조하십시오.
- 일산화탄소
- 분위기는 무엇입니까?
- 탄소
- 단순 및 복합 물질