영형 염화나트륨 (식용 소금)은 우리가 일상 생활에서 수제 또는 가공 (공업화 된) 식품에 소금을 뿌리는 데 사용하는 소금입니다. 과일, 채소, 콩류, 씨앗 등과 같이 우리가 매일 소비하는 다양한 자연 식품에도 존재하는 물질입니다.
이 텍스트에서 당신은 인간의 일상 생활에 중요한 물질에 대한 모든 것을 알게 될 것입니다.
정의
염화나트륨은 염의 무기 기능에 속하며 나트륨 양이온 (Na)의 결합으로 구성됩니다.+) 그건 음이온 c그곳에오레 토 (Cl-) ~ a 이온 결합.
b) 화학적 특성
염화나트륨은 두 가지 화학 원소로 구성됩니다.
→ 나트륨 (Na) :
금속 계열에 속함 (양이온을 쉽게 형성 할 수 있음) 알칼리성 (AI);
원자가 껍질에 전자가 있습니다.
원자 번호는 11과 같습니다.
전기 양성 (전자를 잃는 능력)이 높습니다.
→ 염소 (Cl)
할로겐 계열 (VIIA)에 속합니다.
비금속입니다 (그래서 쉽게 음이온이됩니다).
원자가 껍질에 7 개의 전자가 있습니다.
원자 번호는 17과 같습니다.
높은 전기 음성도 (전자를 얻을 수있는 능력)가 있습니다.
염화나트륨을 형성하는 두 가지 화학 원소가 각각 존재하기 때문에 높은 전기 양성과 높은 전기 음성도, 그들 사이에는 이온 결합이 있습니다 (잃고 얻는 경향이있는 원자 사이에 설정 됨) 전자).
염화나트륨의 화학 구조는 아래 구조에서 볼 수 있듯이 6 개의 나트륨 양이온 (파란색 구체)과 상호 작용하는 단일 염화물 음이온 (녹색 구체)으로 구성됩니다.
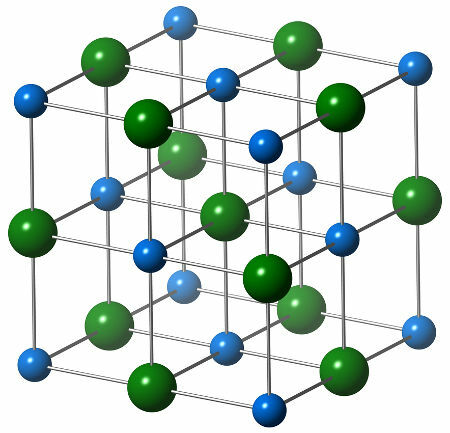
염화나트륨의 결정 구조 표현
c) 물리적 특성
퓨전 포인트 :
염화나트륨은 801의 온도에서 고체 상태에서 액체 상태로 변환 될 수 있습니다. 영형씨.
비점:
염화나트륨은 1465의 온도에서 액체에서 기체 상태로 변환 될 수 있습니다. 영형씨.
극성
이온 결합에 의해 유래 된 물질, 즉 이온 성 화합물이기 때문에 염화나트륨은 극성이 있습니다.
물에 대한 용해도
우리는 25에서 1L의 물에 녹일 수 있습니다. 영형C, 최대 359g의 염화나트륨.
다른 용매에 대한 용해도 :
염화나트륨은 극성 화합물이기 때문에 기름과 같은 비극성 용매에 용해 될 수 없습니다.
밀도:
염화나트륨의 밀도는 2.165g / mL이므로 밀도가 1g / mL 인 물보다 밀도가 높습니다.
전기 전도도 :
이온 성 화합물이기 때문에 염화나트륨은 다음과 같은 경우에만 전류를 전도 할 수 있습니다.
그것은 녹은 상태, 즉 액체입니다.
물에 용해.
d) 획득 방법
염화나트륨은 물리적 또는 화학적으로 얻을 수 있습니다.
1영형) 육체 화 :
분수 결정화
염화나트륨은 바다에서 물을 증발시켜 얻습니다.
지하 광산
광산 기술을 사용하여 광산에서 추출됩니다.
지하 퇴적물
그것은 물에 용해 (광물에 존재하는 소금이 용해 됨)하고이어서 펌핑함으로써 깊은 지하 침전물에서 추출됩니다.
2영형) 화학적으로 얻기
합성 반응
염화나트륨은 염소 가스와 금속 나트륨 사이의 합성 (단순한 물질이 복합 물질을 생성 함)의 화학 반응에서 얻을 수 있습니다.
2에서(에스) + Cl2 (g) → 2 NaCl(에스)
중화 반응:
염화나트륨을 화학적으로 얻는 또 다른 방법은 염산과 수산화 나트륨 사이의 중화 반응을 통해 소금과 물을 형성하는 것입니다.
HCl(1) + NaOH(여기) → NaCl(여기) + H2영형(1)
e) 인간에 대한 중요성
염화나트륨 자체는 인체에서 기능을하지 않지만 나트륨 양이온 (Na+) 및 염화 음이온 (Cl-),이 두 이온 각각은 우리 몸에 몇 가지 중요한 기능을합니다. 다음 기능 중 일부를 참조하십시오.
→ 나트륨 양이온 (Na+)
혈액 응고를 방지합니다.
신장과 담석의 형성과 싸 웁니다.
체액 조절에 참여하십시오.
혈압 조절에 참여하십시오.
→ 염화 음이온 (Cl-)
위액의 형성 및 구성에 참여 (염산 – HCl);
췌장 주스 형성에 참여.
f) 인체 손상
염화나트륨의 과도한 섭취는 인간에게 다음과 같은 해를 끼칠 수 있습니다.
→ 신체의 과도한 나트륨 양이온으로 인한 손상 :
상처 치유 시간 증가;
발생률 증가 급격한 복통;
혈압 상승;
신장 과부하;
신체의 체액 유지 증가.
→ 신체의 과도한 염화 음이온으로 인한 손상 :
파괴 비타민 E;
신체의 요오드 생성 감소.
g) 기타 응용
소금물에 사용되는 것 외에도 염화나트륨은 다음과 같은 상황에서도 사용할 수 있습니다.
샴푸 생산;
종이 생산;
생산품 수산화 나트륨 (NaOH);
세제 생산;
비누 생산;
눈보라로 고통받는 곳에서 눈이 녹습니다.
금속 나트륨 생산;
염소 가스 생산;
신체 전해질 대체를위한 등장 론에서;
코 충혈 완화제에서;
식염수 생산; 다른 응용 프로그램 중에서.
나로. Diogo Lopes Dias

