როგორც ტექსტშია განმარტებული გადაწყვეტილებები გაჯერება, ქიმიური ხსნარები წარმოიქმნება ა ხსნადი ზე გამხსნელი. თითოეულ ხსნადს აქვს a ხსნადობის კოეფიციენტი სპეციფიკური, რომელიც მოცემულია მოცემულ გამხსნელში ხსნადი ხსნადის მაქსიმალური რაოდენობით ტემპერატურა.
გრაფიკის აგება ხსნადობის მრუდით
მაგალითად, ხსნადობის კოეფიციენტი KNO– ს3 არის 31,2 გ 100 გრ წყალში 20 ° C ტემპერატურაზე. თუ კალიუმის ნიტრატის ზუსტად იმ რაოდენობას გავხსნით 100 გ წყალში 20 ° C ტემპერატურაზე, გაჯერებული ხსნარი. ამ მარილის ნებისმიერი დამატებითი რაოდენობა გამოიყოფა (ქმნის ქვედა ტანს კონტეინერში).

ამასთან, ხსნადობის კოეფიციენტი განსხვავდება ტემპერატურის შესაბამისად. ასე რომ, თუ ამ გაჯერებულ ხსნარს გავაცხელებთ KNO ქვედა კორპუსით3, ნალექი თანდათან იხსნება წყალში. ქვემოთ იხილეთ KNO ხსნადობის კოეფიციენტების მნიშვნელობები3 100 გრ წყალში სხვადასხვა ტემპერატურაზე:
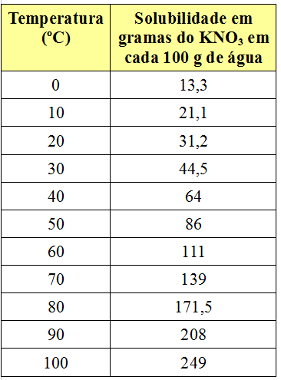
გაითვალისწინეთ, რომ ხსნადობა ამ მარილის წყალში იზრდება ტემპერატურის მომატება. უმეტეს ნივთიერებებში ესეც ასეა. თუ ამ მნიშვნელობებს ჩავსვამთ ა გრაფიკული, ჩვენ გვექნება შემდეგი:
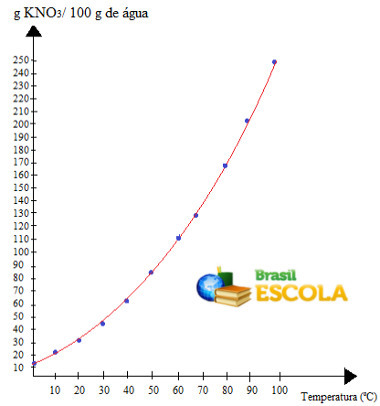
ეს არის ზარი ხსნადობის მრუდი KNO– ს3. ჩვენ ვამბობთ, რომ ის აღმავალია, რადგან ის იზრდება ტემპერატურის მატებასთან ერთად.
ხსნადობის ხსნადობის მრუდის მახასიათებლები გრაფაში
თითოეულ ნივთიერებას აქვს თავისი ხსნადობის მრუდი მოცემული გამხსნელისთვის. ზოგიერთ ამ ნივთიერებას აქვს შემცირებული ხსნადობა ტემპერატურის მატებასთან ერთად, ისევე როგორც CaCrO– ს შემთხვევაში4, რომელსაც აქვს ხსნადობის მრუდი ქვევით ეს ნიშნავს, რომ თუ ამ მარილის გაჯერებულ ხსნარს გავათბობთ, გახსნილი მარილის ნაწილი გამოილექება.
რაც შეეხება სხვა ნივთიერებებს, ტემპერატურის მომატება არ ერევა იმდენად ხსნადობაში, როგორც ეს ხდება სუფრის მარილის (NaCl) ხსნართან. 20 ° C- ზე, NaCl- ის ხსნადობის კოეფიციენტი 36 გ 100 გრ წყალშია, მაგრამ თუ ტემპერატურას 100 ° C- მდე გავზრდით, ეს ხსნადობა მხოლოდ 39,8 გ-მდე გაიზრდება, რაც ძალიან მცირე ზრდაა.
ასევე არსებობს ნივთიერებები, რომლებშიც ხსნადობა მხოლოდ ტემპერატურის ზრდის გარკვეულ წერტილამდე იზრდება, რადგან ამის შემდეგ ხსნადობა იკლებს. ეს ხდება, მაგალითად, ჰიდრატირებული ნივთიერებებით, რომლებიც თბება, მიაღწევს დეჰიდრატაციის დროს. ამიტომ, მისი შემადგენლობის შეცვლისას, იცვლება მისი ხსნადობის ვარიაცია ტემპერატურასთან ერთად. ეს მოვლენა შეიძლება დაფიქსირდეს გრაფაში ხსნადობის მრუდის ინფლექციების საშუალებით.
ქვემოთ წარმოგიდგენთ ა გრაფიკი ხსნადობის მრუდებით სხვადასხვა ნივთიერებების:
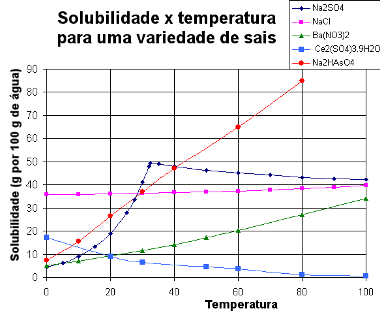
სხვადასხვა მარილების ხსნადობის მრუდი
ამ ტიპის გრაფიკის საშუალებით შეგვიძლია შევადაროთ სხვადასხვა მარილების ხსნადობა ერთ გამხსნელში და იმავე ტემპერატურაზე.
ხსნარის კლასიფიკაცია ხსნადობის მრუდის მქონე გრაფის გამოყენებით
საათზე ხსნადობის მრუდები ისინი ასევე ხელს უწყობენ ხსნარების გაჯერების განსაზღვრას, ანუ არის ისინი გაჯერებული, გაჯერებული, გაჯერებული ფონით ან ზედ გაჯერებული. იხილეთ მაგალითი:
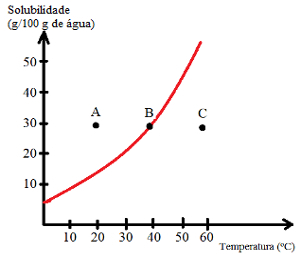
იხილეთ რა ტიპის ხსნარებია მითითებული A, B და C წერტილებით:
A: ქვედა ტანით გაჯერებული. A წერტილში 30 გრ ხსნადი იხსნება 100 გრ წყალში 20 ° C ტემპერატურაზე. მრუდი გვიჩვენებს, რომ ამ ეტაპზე ხსნადობის კოეფიციენტია დაახლოებით 15 გ / 100 გ წყალი. ამრიგად, რადგან ხსნადი ნივთიერების რაოდენობა უფრო მეტია, მიიღება გაჯერებული ხსნარი ქვედა კორპუსით.
B: გაჯერებული. წერტილი B მდებარეობს ზუსტად ხსნადობის მრუდზე, რაც მიუთითებს იმაზე, რომ ხსნარი გაჯერებულია, ვინაიდან 100 გ წყალში გახსნილია 30 გ ხსნადი 40 ° C ტემპერატურაზე. ეს არის ზუსტად ამ ხსნადობის ხსნადობის კოეფიციენტი ამ ტემპერატურაზე.
C: უჯერი. არსებობს 30 გრ ხსნადი, რომელიც გახსნილია 100 გრ წყალში 60 ° C ტემპერატურაზე. მრუდი გვიჩვენებს, რომ ამ ეტაპზე ხსნადობის კოეფიციენტი 50 გრ / 100 გრ წყალზე მეტია. ამრიგად, ვინაიდან გახსნილი ხსნადი ნივთიერებების ხსნადობის კოეფიციენტზე ნაკლებია, არსებობს უჯერი ხსნარი.
ამრიგად, შეგვიძლია დავასკვნათ, რომ:
მრუდის ზემოთ წერტილები: გაჯერებული ხსნარები ფონის კორპუსით;
წერტილები მრუდზე: გაჯერებული ხსნარები;
მრუდის ქვეშ წერტილები: უჯერი ხსნარები.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/graficos-das-curvas-solubilidade.htm