ქიმიური რეაქციის ჩასატარებლად აუცილებელია ოთხი ძირითადი პირობის დაკმაყოფილება, რომლებიც:
1. რეაგენტები უნდა დაუკავშირდნენ;
2. რეაგენტებს შორის უნდა არსებობდეს ქიმიური დამოკიდებულება;
3. რეაქტიულ ნაწილაკებს შორის შეჯახება უნდა იყოს ეფექტური;
4. აქტივობის ენერგიას უნდა მიაღწიოს.
მოკლედ იხილეთ თითოეული შემთხვევა:
1.რეაგენტებს შორის კონტაქტი:
ეს მდგომარეობა აშკარაა, რადგან მაშინაც კი, თუ რეაქტიულებს დიდი დამოკიდებულება აქვთ ერთმანეთთან, ისევე როგორც მჟავებისა და ბაზების შემთხვევაში, თუ ისინი გამოყოფენ, რეაქცია არ მოხდება. მათ უნდა დაუკავშირდნენ, რომ მათი ნაწილაკები შეეჯახონ, გატეხონ რეაქტივების ობლიგაციები და შექმნან პროდუქციის ბმები.

2.ქიმიური დამოკიდებულება:
როგორც ვნახეთ, რეაგენტების კონტაქტში მოყვანა აუცილებელია, მაგრამ არ არის საკმარისი. მაგალითად, თუ ნატრიუმს წყალთან შევეხებით, უკიდურესად სასტიკი რეაქცია მოხდება, მაგრამ თუ ოქროს დავდებთ, ვერანაირ განსხვავებას ვერ ვხედავთ. ეს იმიტომ ხდება, რომ სხვადასხვა ნივთიერებებს ერთმანეთთან განსხვავებული ქიმიური დამოკიდებულება აქვთ, ან მათ შეიძლება საერთოდ არ ჰქონდეთ რაიმე დამოკიდებულება. რაც მეტია ქიმიური დამოკიდებულება, მით უფრო სწრაფია რეაქცია.
აღნიშნულ მაგალითებში ნატრიუმს დიდი დამოკიდებულება აქვს წყალთან, იმდენად, რომ იმისათვის, რომ არ მოხდეს კონტაქტი ჰაერის ტენიანობასთან, მეტალის ნატრიუმი ინახება ნავთის შემადგენლობაში. ოქრო ინერტულია, ამიტომ ოქროს ძეგლები ასე გრძელდება, ეგვიპტის სარკოფაგების მსგავსად.

3.შეჯახების თეორია:
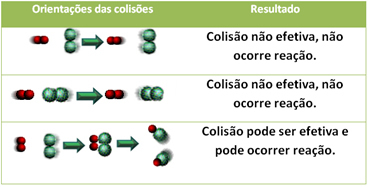
ნაერთებშიც კი, რომლებსაც აქვთ ქიმიური დამოკიდებულება, რეაქციის მისაღწევად აუცილებელია მათი ნაწილაკები, ატომები ან მოლეკულები ეფექტურად დაეჯახონ ერთმანეთს. ყველა ნაწილაკი, რომელიც ეჯახება, ამას ეფექტურად არ ახდენს, მაგრამ შოკი, რომლის შედეგადაც ხდება გატეხვა რეაგენტის ობლიგაციები და ახალი ობლიგაციების წარმოქმნა არის ის, რაც ხდება სწორი ორიენტაციით და ენერგიით საკმარისი.
ქვემოთ ნაჩვენებია ორი არაეფექტური შეჯახების და ერთი ეფექტური შეჯახების შემთხვევა, რომლის შედეგადაც ხდება რეაქცია.
4.აქტივაციის ენერგია და აქტივირებული კომპლექსი:
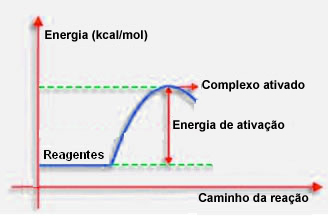
როგორც წინა პუნქტში იყო ნათქვამი, ეფექტური შეჯახება, გარდა ხელსაყრელი მითითებებისა, ასევე საჭიროებს საკმარის ენერგიას. თითოეული რეაქციისთვის საჭირო ენერგიის მინიმალურ რაოდენობას აქტივაციის ენერგია ეწოდება.
თუ რეაქტორებს აქვთ აქტივაციის ენერგია ტოლი ან მეტი ენერგია, კარგად ორიენტირებული შოკის დროს, ჩამოყალიბდება თავდაპირველად გააქტიურებული კომპლექსი, რომელიც წარმოადგენს შუალედურ სტრუქტურას რეაქტორებსა და პროდუქტები გააქტიურებულ კომპლექსში არსებობს დასუსტებული რეაგენტის ობლიგაციები და წარმოიქმნება ახალი პროდუქტის ობლიგაციები.
ამრიგად, აქტივაციის ენერგია მუშაობს ერთგვარი ბარიერი რეაქციის წარმოსაქმნელად, რადგან რაც უფრო დიდია, მით უფრო გაუჭირდება რეაქციის მოხდენა. ზოგიერთ შემთხვევაში საჭიროა რეაგენტების ენერგიის მიწოდება. მაგალითად, გაზს ამზადებს ჰაერში ჟანგბადთან ურთიერთქმედებასთან დაკავშირებით, მაგრამ საჭიროა ენერგიის მიწოდება მაშინ, როდესაც ასანთი ერთმანეთს გავაერთიანებთ, წინააღმდეგ შემთხვევაში რეაქცია არ ხდება. დაწყებისთანავე, რეაქცია გამოყოფს საკმარის ენერგიას სხვა მოლეკულების გასააქტიურებლად და რეაქციის გასაგრძელებლად.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm
