მჟავები და ბაზები ორი ქიმიური ფუნქციაა, რომლებიც საწინააღმდეგოდ ითვლება., ეს იმიტომ ხდება, რომ მათი თვისებები, როგორც წესი, შებრუნებულია. მაგალითად, თუ გავითვალისწინებთ ყოველდღიურ ცხოვრებაში არსებულ საკვებს, რომელიც მჟავეა, დავინახავთ, რომ მათი გემო, ზოგადად, მჟავეა, როგორც ეს ლიმონის შემთხვევაში ხდება. ამასთან, ძირითად საკვებს აქვს შემკვრელი გემო (რომელიც "უკავშირებს" პირს), მწვანე ბანანის მსგავსად.
მაგრამ ნივთიერების იდენტიფიცირება როგორც მჟავე ან ძირითადი მხოლოდ გემოვნებით, ისევე როგორც მეთოდი, რომელსაც აქვს მრავალი წარუმატებლობის შანსი, ეს ასევე ძალზე საშიშია, რადგან ბევრი მჟავა და ფუძეა ძლიერი, ტოქსიკური და შეიძლება მოკლას, მაგალითად, მჟავა. გოგირდოვანი (H2მხოლოდ4), რომელიც გამოიყენება ავტომობილების ბატარეებში და ნატრიუმის ჰიდროქსიდი (NaOH), კომერციულად ცნობილი როგორც კაუსტიკური სოდა.
ამრიგად, ორგანოლეპტიკური თვისებები (თვისებები, რომლებიც ეხება ჩვენს გრძნობებს, როგორიცაა გემო და სუნი) არ არის მჟავებისა და ბაზების იდენტიფიკაციის თვისებები. ქვემოთ გაითვალისწინეთ ამ ორგანული ფუნქციების სხვა თვისებები, რომლებიც ემსახურება მათ შედარებას და გარჩევას:
- წყალში ხსნადობა:
შენ მჟავები ჩვეულებრივ კარგად ხსნადი წყალში, ხოლო უმეტესობა ბაზები é უხსნადი. ტუტე ლითონის ფუძეები ხსნადია, ტუტე მიწაზე ლითონების ცუდად იხსნება და სხვა ლითონების ფუძეები არ იხსნება (გამონაკლისი არის ამონიუმის ჰიდროქსიდი, NH4OH, რომელიც მხოლოდ წყალხსნარში არსებობს, ამიაკის გაზს ბუშტავს წყალში და, შესაბამისად, მასში ხსნადია).
როდესაც ჩვენ ვამბობთ ”უხსნად”, ვგულისხმობთ იმას, რომ ეს ნივთიერებები პრაქტიკულად არ იხსნება, რადგან არც ერთი ნივთიერება წყალში სრულად არ იხსნება.
- სტრუქტურა:
Ყველა მჟავები მოლეკულურია, ანუ ჩამოყალიბდა კოვალენტური ბმებით, რომლებშიც ელექტრონები არიან გაზიარებული. მაგალითად, არის მარილმჟავა გაზი, რომელიც წარმოიქმნება წყალბადსა და ქლორს შორის წყვილი ელექტრონების გაზიარებით:

უკვე ბაზები შეიძლება იყოს იონური და მოლეკულური. ტუტე და ტუტე მიწის ლითონები აქვთ იონურს, დანარჩენები კი მოლეკულურია.
მაგალითები:
NaOH: იონური ფუძე, რომელიც წარმოიქმნება Na იონებით+ და ოჰ-;
NH4OH: ამიაკის მოლეკულური ბაზა წყალში.
- ელექტროგამტარობა:
ყველა მჟავები მხოლოდ ელექტროენერგიას ატარებენ წყალში გახსნისას, რადგან ისინი წყალში იმყოფებიან, ისინი იონიზაციას განიცდიან, ანუ გამოყოფენ იონებს.
მაგალითი:
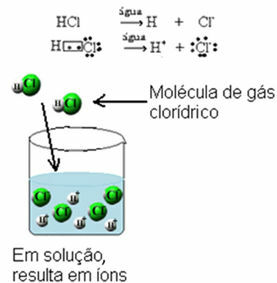
ყველა ბაზები ასევე ახდენენ ელექტრულ დენადობას ხსნარში., რადგან იონური განიცდის დისოციაციას (გამოყოფს იონებში უკვე არსებულ ფორმულას) და მოლეკულურებს განიცდის იონიზაციას, რეაგირებს წყალთან და გამოყოფს იონებს. საათზე ტუტე ლითონის ფუძეები ასევე ახორციელებენ ელექტროენერგიას, როდესაც ისინი თხევად (მდნარ) მდგომარეობაში არიან.
- მოქმედება ინდიკატორებზე:
შენ მჟავა-ტუტოვანი მაჩვენებლები არის ბუნებრივი ან სინთეზური ნივთიერებები, რომლებიც განიცდიან ფერის შეცვლას მჟავასთან ან ფუძესთან შეხებისას. თუ მჟავა იწვევს ინდიკატორის ფერის შეცვლას, ფუძე დაუბრუნებს ინდიკატორს თავდაპირველ ფერს და პირიქით.
მაგალითად, ფენოლფთალინი ფართოდ გამოიყენება მჟავა-ტუტოვანი მაჩვენებელი და ძირითად გარემოში ხდება ძალიან ინტენსიური ვარდისფერი; უკვე მჟავე გარემოში ხდება უფერო. ლაკმუსის ქაღალდი ასევე კარგი მაჩვენებელია, რადგან მჟავაში ის წითლდება; და ერთ ბაზაზე, ის ლურჯი ხდება.
ეს ასევე ემსახურება pH განსხვავების მითითებას, რომელიც მჟავებსა და ბაზებს შორის არსებობს.
- PH:
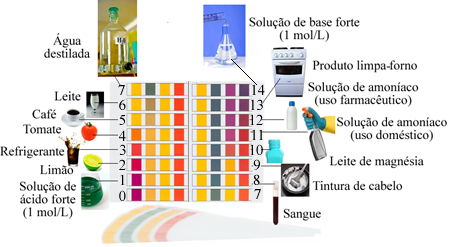
ნეიტრალურად თვლილ საშუალო ფენას აქვს pH ტოლი 7-ის, როგორც გამოხდილი წყლის შემთხვევაში.
მჟავების pH 7-ზე ნაკლებია, მიუხედავად იმისა ბაზებს აქვთ 7-ზე მეტი pH.
ხსნარის მაგალითები, რომლებიც pH- ით ახლოსაა მასშტაბით.
- საპასუხო მოქმედება:
კონტაქტში მოხვედრისას მჟავები და ფუძეები რეაგირებენ ერთმანეთთან, ანეიტრალებენ ერთმანეთს, ანუ pH– ს ნეიტრალური ხდიან. ეს იმიტომ ხდება, რომ H კათიონი+ მჟავასგან რეაგირებს OH ანიონთან- ფუძიდან, წყლის წარმოქმნით. ამ ტიპის რეაქციას ეწოდება ა ნეიტრალიზაციის რეაქცია და ის ასევე აწარმოებს მარილს.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/comparacao-entre-acidos-bases.htm

