კუთხოვანი გეომეტრია არის რამდენიმე ტიპის ერთ – ერთი მოლეკულური გეომეტრია, რომელიც კვლავ შეიძლება იყოს წრფივი, პირამიდული, ბრტყელი ტრიგონალური, tetrahedralდა ა.შ. კუთხოვანი გეომეტრია გვხვდება მხოლოდ იმ მოლეკულებში, რომლებსაც აქვთ შემდეგი მახასიათებლები:
ტრიატომიკა, ანუ მათ მხოლოდ სამი ატომი აქვთ;
მინიმუმ სამი ელექტრონული ღრუბელი ჰქონდეთ ცენტრალურ ატომში.
Შენიშვნა: ელექტრონული ღრუბელი ყველაფერია კოვალენტური ბმა (ერთი, ორმაგი, სამმაგი ან კოორდინატი) ატომებსა და ელექტრონულ წყვილებს შორის ვალენტობის ფენა რომლებიც არ მონაწილეობენ ზარში.
იხილეთ მოლეკულების რამდენიმე მაგალითი, რომლებსაც აქვთ კუთხოვანი გეომეტრია:
პირველი მაგალითი: წყალი (H2ო)

ჩვეულებრივი წყლის სტრუქტურა
წყლის სტრუქტურაში გვაქვს:
სამი ატომი: ორი წყალბადის და ერთი ჟანგბადის;
ჟანგბადი არის ცენტრალური ატომი, რადგან იგი ქმნის ბმების მეტ რაოდენობას (ორი, რადგან ის მიეკუთვნება VIA ოჯახს);
ორი ერთჯერადი კავშირი ჟანგბადსა და წყალბადებს შორის. ეს იმიტომ ხდება, რომ თითოეულ წყალბადს შეუძლია მხოლოდ ერთი კავშირის შექმნა და ჟანგბადის ორი კავშირი;
ჟანგბადში ოთხი არააკავშირებელი ელექტრონი, რადგან მას აქვს ექვსი ელექტრონი ვალენტურ გარსში და მხოლოდ ორს იყენებს ობლიგაციებში.
ამიტომ, ისევე როგორც წყლის მოლეკულაში, ცენტრალურ ატომში არის სამი ატომი და ოთხი ელექტრონული ღრუბელი (ორი ერთი ბმა და ორი არამკავშირებელი ელექტრონული წყვილი), გეომეტრია კუთხოვანია.
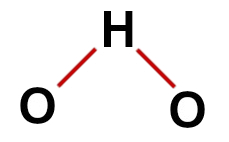
წყლის სწორი სტრუქტურული ფორმულა
Შენიშვნა: ყოველთვის, როდესაც მოლეკულა წარმოადგენს ამ შაბლონებს, ატომებს შორის წარმოქმნილი კუთხე დაახლოებით 109 º 28-ია'.
მე -2 მაგალითი: გოგირდის დიოქსიდი (SO2)

გოგირდის დიოქსიდის ჩვეულებრივი სტრუქტურა
გოგირდის დიოქსიდის სტრუქტურაში გვაქვს:
სამი ატომი: ორი ჟანგბადი და ერთი გოგირდის ატომი;
გოგირდი ცენტრალური ატომია, რადგან ის ყველაზე მცირე ელემენტია მოლეკულაში, ვინაიდან ყველა ელემენტს სჭირდება იგივე რაოდენობის ობლიგაციების შექმნა (ორი);
ორმაგი კავშირი გოგირდსა და ერთ ჟანგბადს შორის. ეს იმიტომ, რომ ორივეს ორი კავშირი სჭირდება;
ერთი კოორდინატიული ან დავათი კოვალენტური ბმა, რადგან გოგირდი სტაბილური იყო სხვა ჟანგბადთან დაწყვილების შემდეგ, მაგრამ მაინც არის ჟანგბადის ატომი, რომელსაც სჭირდება ორი ელექტრონი;
ჟანგბადში ოთხი არააკავშირებელი ელექტრონი. ეს იმიტომ, რომ ჟანგბადს ექვსი ელექტრონი აქვს ვალენტურ გარსში და მხოლოდ ორს იყენებს ობლიგაციებში.
ამრიგად, ისევე როგორც გოგირდის დიოქსიდის მოლეკულაში, ცენტრალურ ატომში არის სამი ატომი და ოთხი ელექტრონული ღრუბელი (ორი ერთი ბმა და ორი წყვილი არამკავშირებელი ელექტრონი), გეომეტრია კუთხოვანია.
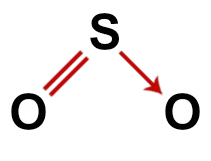
გოგირდის დიოქსიდის სწორი სტრუქტურული ფორმულა
Შენიშვნა: ყოველთვის, როდესაც მოლეკულას აქვს ეს ნიმუშები, ატომებს შორის წარმოქმნილი კუთხე დაახლოებით 120-იაო.
ჩემ მიერ. დიოგო ლოპეს დიასი
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm

