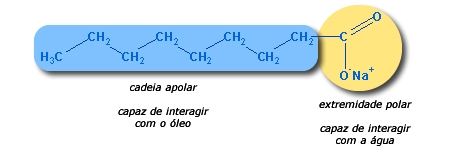
მჟავას ოქსიდები არის ის ოქსიდები, რომლებიც წყალთან რეაგირებისას წარმოქმნიან მჟავას, როგორც პროდუქტს. ფუძესთან რეაგირებისას, პროდუქტები იქნება მარილი და წყალი.
ამ ნაერთებს, ჩვეულებრივ, აქვთ კოვალენტური ხასიათი, ანუ ისინი არიან მოლეკულური, წყალში ხსნადი და წარმოიქმნება ძირითადად არალითონებით, რომლებიც მაღალი ელექტრონეგატივითობის ელემენტებია. ლითონებით წარმოქმნისას მათ აქვთ მაღალი დაჟანგვის რიცხვი (ელექტრული მუხტი).
მაგალითები:
კომპანია2მხოლოდ2მხოლოდ3, პ2ო5, კლ2ო6, იქ2არა2ო4არა2ო5და ა.შ.
ქვემოთ მოცემულია მჟავა ოქსიდების დამახასიათებელი რეაქციების ზოგადი სქემა და მაგალითი:
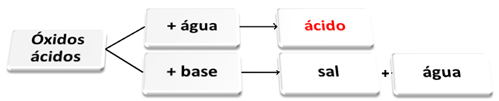
მჟავა ოქსიდები რეაგირებენ წყალთან და ფუძესთან
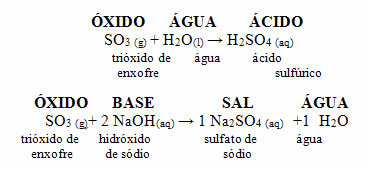
მჟავას ოქსიდებს ასევე უწოდებენ ანჰიდრიდები, რადგან ეს სიტყვა ბერძნულიდან მოდის ანჰიდროსი, რაც ნიშნავს "წყალი არ არის", და მჟავა ოქსიდები შეიძლება ჩაითვალოს "უწყლო მჟავად".
ზოგიერთი მჟავა ოქსიდის თვისებები და გამოყენება:
• ნახშირორჟანგი (ნახშირორჟანგი) - CO2:
ეს ნაერთი გამოიყენება როგორც გაზი გამაგრილებელ სასმელებში და მინერალურ წყლებში, რადგან მაღალ წნევაზე ზემოქმედებისას იგი წყალში ხსნადი ხდება. იგი ამ პროდუქტებში აწარმოებს მჟავე გარემოს, რადგან ეს არის მჟავე ოქსიდი, რომელიც რეაგირებს წყალთან და წარმოქმნის მჟავას, ქვემოთ მოცემული რეაქციის შესაბამისად:

78 ° C ტემპერატურაზე დაბლა, იგი მყარ მდგომარეობაშია და ცნობილია მშრალი ყინულის სახელით, რომელსაც თავისი სახელი მიენიჭა, რადგან მისი გარეგნობა ყინულს ჰგავს. საერთო, მაგრამ ის არ დნება, თხევად მდგომარეობაში გადადის ოთახის ტემპერატურაზე, მაგრამ ის მიდის ორთქლის მდგომარეობაში, დიდები. ამრიგად, ეს ფუნქცია გამოიყენება როგორც სცენური რესურსი კონცერტებში, ფილმებში, თეატრებში, წვეულებებში და ა.შ.

ნახშირორჟანგი არის მჟავა ოქსიდი
ის ასევე გვხვდება ატმოსფეროში ადამიანის სუნთქვის, წიაღისეული საწვავის (ნახშირის, ნავთობპროდუქტების, ალკოჰოლის და ა.შ.) დაწვის და ტყის ხანძრების შედეგად. ამრიგად, ის მჟავე წვიმაზე პასუხისმგებელთაგანია.
• გოგირდის ოქსიდები - SO2 ამიტომაც3
ეს ოქსიდები ასევე არსებობს ატმოსფეროში, ბუნებრივი და ხელოვნური წარმოშობისაა. ბუნებრივი ხდება მცენარეებისა და ცხოველების ვულკანური ამოფრქვევებისა და დაშლის შედეგად. ხელოვნური შეესაბამება ამ ოქსიდების უდიდეს რაოდენობას, როგორც ისინი გამოიდევნება წიაღისეული საწვავის დაწვით, ძირითადად დიზელის ზეთით, რომელიც შეიცავს გოგირდს, როგორიცაა უწმინდურება.
გოგირდის დიოქსიდი (SO2) რეაგირებს ჟანგბადთან ატმოსფეროდან და წარმოქმნის გოგირდის ტრიოქსიდს (SO3). როდესაც ეს უკანასკნელი ოქსიდი რეაგირებს წვიმის წყალთან, წარმოიქმნება გოგირდის მჟავა, რომელიც ძალიან ძლიერია და ზიანს აყენებს.
• გოგირდის დაწვა საწვავიდან: S + O2 → ოპერაციული სისტემა2
• SO2- ის SO3- ით გარდაქმნა: SO2 +2 → ოპერაციული სისტემა3
SO2 და SO3 რეაქციები წყლის მჟავებთან მიმართებაში: SO2 + თ2O → H2მხოლოდ3
მხოლოდ3 + თ2O → H2მხოლოდ4
• დინიტროგენის ტეტროქსიდები (აზოტ-აზოტის ანჰიდრიდი) - N2ო4
ამ ნაერთს აქვს დუღილის წერტილი 22ºC, აქვს ყვითელი ფერი და საკმაოდ არამდგრადია. იგი წარმოიქმნება ატმოსფეროში აზოტის დაჟანგვის შედეგად და შეიძლება იყოს თხევადი სახით, მონონიტროგენის დიოქსიდის ან აზოტის ოქსიდის დიმერის სახით (NO2). ამ ტემპერატურის ზემოთ იგი იღებს NO- ს ფორმას2:
ნ2ო4 ↔ არა2
ეს არის უკიდურესად ტოქსიკური გაზი და მისი ინჰალაცია ფატალურია. იგი ასევე გამოიყენება სარაკეტო საწვავის შემადგენლობაში.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია