ქიმიური ელემენტების ორგანიზების ერთ-ერთი გზაა ოჯახები, რომლებიც პერიოდული ცხრილის ვერტიკალურ თანმიმდევრობებს შეესაბამება.
საათზე 18 სვეტი ცხრილი აჯგუფებს ელემენტებს ქიმიური თვისებების მსგავსების მიხედვით.
ქიმიური ელემენტების ოჯახებში ორგანიზება იყო ნაპოვნი სხვადასხვა ინფორმაციის სტრუქტურირებისა და მათი მარტივი ფორმით წარმოდგენის პრაქტიკული გზა.
ქიმიური ელემენტის ადგილმდებარეობის გასამარტივებლად ოჯახები დანიშნულ იქნა 1-დან 18-მდე ნომრებში შემდეგნაირად:
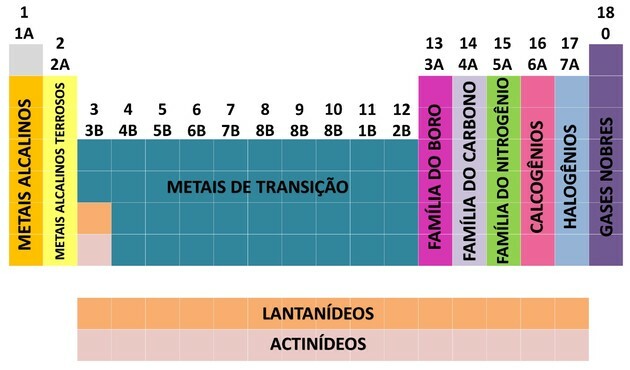
მრავალი მეცნიერის წვლილისა და მონაცემთა მოწყობის სხვადასხვა მცდელობის შედეგად, პერიოდული სისტემა ჩამოყალიბდა, ელემენტების განლაგების წესრიგის დამყარება.
ოჯახების ნომენკლატურა
- ცხრილში მოცემული ოჯახები იყოფა A (წარმომადგენელი) და B (გარდამავალი), მათი იდენტიფიცირება ხდება ასოებით და ციფრებით.
- შენ წარმომადგენლობითი ელემენტები 0, 1A, 2A, 3A, 4A, 5A, 6A და 7A ოჯახები შეესაბამება.
- შენ გარდამავალი ელემენტები 1B, 2B, 3B, 4B, 5B, 6B, 7B და 8B ოჯახები შეესაბამება.
- სუფთა და გამოყენებითი ქიმიის საერთაშორისო კავშირის (IUPAC) დადგენილებით, ოჯახები გამოვლინდნენ ჯგუფები 1-დან 18-მდე.
პერიოდული ცხრილი და ელექტრონული განაწილება
მსგავსება ერთი და იმავე ოჯახის ელემენტებს შორის ხდება იმის გამო, რომ ატომური ვალენტური ელექტრონების რაოდენობა მიწისქვეშა მდგომარეობაში იგივეა გარკვეული ჯგუფის წევრებისთვის.
Მაგალითად:
| ჯგუფი 1 | Eletronic განაწილება |
|---|---|
| 3წაიკითხა | 2-1 |
| 11საათზე | 2-8-1 |
| 19კ | 2-8-8-1 |
| 37რბ | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87ძმაკაცი | 2-8-18-32-18-8-1 |
1 ჯგუფის ატომებს ელექტრონები გადანაწილებული აქვთ ერთზე მეტ ენერგეტიკულ დონეზე, მაგრამ ყველას აქვს ვალენტური ელექტრონი.
ამით ჩვენ ვაკვირდებით, რომ ხდება ელექტრონული განაწილება ატომის საფუძველში, ჩვენ ვხვდებით მის პოზიციას პერიოდულ სისტემაში.
წარმომადგენლობითი ელემენტები
წარმომადგენლობითი ელემენტები შედარებით ნაკლებად რთულ ქიმიურ ქცევას ავლენენ, ვიდრე გარდამავალი ელემენტები და ქმნიან ჩვენს გარშემო არსებულ ნივთიერებების უმეტესობას.
წარმომადგენლობითი ელემენტების ზოგიერთ ოჯახს ენიჭება სპეციალური სახელები, როგორც ნაჩვენებია ქვემოთ:
ჯგუფური |
ოჯახი | კონკრეტული სახელი | სახელის წარმოშობა | ელემენტები | ელექტრონული კონფიგურაცია |
|---|---|---|---|---|---|
| 1 | 1 ა | ტუტე ლითონები | ლათინურიდან ტუტე, რაც ნიშნავს "მცენარეების ნაცრისფერს". | Li, Na, K, Rb, Cs და Fr | ჩვენ1 |
| 2 | 2 ა | დედამიწის ტუტე ლითონები | ტერმინი "მიწიერი" ნიშნავს "დედამიწაზე არსებულ". | იყავი, მგ, Ca, Sr, Ba და Ra | ჩვენ2 |
| 13 | 3 ა | ბორის ოჯახი | ოჯახის პირველი ელემენტის სახელი. | B, Al, Ga, In, Tl და Nh. | ჩვენ2np1 |
| 14 | 4 ა | ნახშირბადის ოჯახი | ოჯახის პირველი ელემენტის სახელი. | C, Si, Ge, Sn, Pb და Fl. | ჩვენ2np2 |
| 15 | 5 ა | აზოტის ოჯახი | ოჯახის პირველი ელემენტის სახელი. | N, P, As, Sb, Bi და Mc. | ჩვენ2np3 |
| 16 | 6 ა | ქალკოგენები | ბერძნულიდან ხალხები, რადგან ისინი სპილენძის მადნებში ნაპოვნი ელემენტებია. | O, S, Se, Te, Po და Lv. | ჩვენ2np4 |
| 17 | 7 ა | ჰალოგენები | ბერძნული გამოთქმა ნიშნავს მარილის შემქმნელებს. | F, Cl, Br, I, At და Ts. | ჩვენ2np5 |
| 18 | 0 | კეთილშობილი გაზები | ითვლებოდა, რომ არ მოხდეს რეაქცია სხვა ნივთიერებებთან. | ის, ნე, არ, კრ, ქსე, რე და ოგ. | 1 ს2 (ის) ან ჩვენ2np6 |
ცხრილის საშუალებით, ჩვენ ვხედავთ:
- ზემოთ წარმოდგენილი ელემენტები კლასიფიცირებულია, როგორც წარმომადგენლობითი, რადგან მათ აქვთ ყველაზე ენერგიული ელექტრონი s ან p ქვეს დონეზე.
- ელექტრონები ნაწილდება ენერგიის დონეზე და n წარმოადგენს ატომის ყველაზე შორეულ დონეს მიწის მდგომარეობაში.
- წარმომადგენლობითი ელემენტები, IUPAC– ის რეკომენდაციის მიხედვით, მიეკუთვნება 1,2,13,14,15,16,17 და 18 ჯგუფებს.
ო წყალბადის იგი კლასიფიცირებულია სხვა ელემენტების გარდა. თუნდაც 1s ელექტრონული კონფიგურაციით1, ის არ არის 1 ჯგუფის ნაწილი სინგულარული ქცევის წარმოდგენისთვის.
გარდამავალი ელემენტები
გარდამავალი ელემენტები შეესაბამება 3-დან 12-ე ჯგუფებს. ისინი ამ სახელს იღებენ იმიტომ, რომ მათ აქვთ შუალედური მახასიათებლები 1 და 2 ჯგუფებსა და წარმომადგენლობით არალითონურ ელემენტებს შორის.
შენ გარდამავალი ლითონები IUPAC განსაზღვრავს შემდეგს:
გარდამავალ ელემენტს აქვს არასრული d ქვედენა ან შეიძლება შექმნას კატიონები არასრული d ქვექვემდებარებით.
როდესაც მიწისქვეშა მდგომარეობის ატომის ყველაზე ენერგიული ელექტრონი არასრული d ქვედენაშია, იგი ხასიათდება როგორც გარე გარდამავალი.
ლანთანიდები და აქტინიდები შინაგანი გარდამავალი ელემენტებია, რადგან მათ აქვთ მინიმუმ ერთი არასრული ქვესასვლელი.
როდესაც ელემენტებს აქვთ ელექტრონები, რომლებიც ავსებენ d ან f ორბიტალებს, ისინი ავლენენ მსგავს თვისებებს და მათი კლასიფიკაცია შეიძლება d ან f ორბიტალურ ელემენტებად. გარე ან შიდა გარდამავალი.
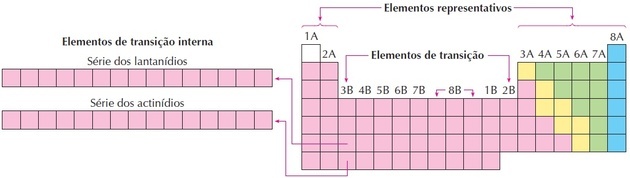
როგორც სურათზე ვხედავთ, ოჯახი 8B შეესაბამება 3 სვეტს, ისინი ჯგუფები 8, 9 და 10, რომლებიც ასე დაჯგუფდა, რადგან მათ აქვთ მსგავსი მახასიათებლები.
ოჯახების ძირითადი მახასიათებლები
ქვემოთ მოცემულ ცხრილში მოცემულია ჯგუფების ძირითადი თვისებები პერიოდულ ცხრილში:
| ჯგუფური | მახასიათებლები | რთული ნივთიერებები მეტი საერთო |
მოვლენები |
|---|---|---|---|
| 1 | მყარი და გამოუყენებელი გარემო პირობებში. ძალიან რეაქტიული, რბილი და კარგი ელექტროენერგია. | მარილები, ჰიდროქსიდები და ოქსიდები |
რეაგირებენ ჰალოგენებთან და ქმნიან მარილებს. |
| 2 | ნაკლებად რეაქტიული და უფრო რთული, ვიდრე 1 ჯგუფი. ვერცხლისფერი მყარი კარგი გამტარობით. | მარილები, ჰიდროქსიდები და ოქსიდები |
მარილებისა და ოქსიდების წარმოქმნა. |
| 3-დან 12-მდე | ისინი ქმნიან კომპლექსებს. ეს არის მეტალის მყარი, მყარი და მყიფე, გარდა მერკური, რომელიც არის თხევადი. | მარილები, ოქსიდები და კომპლექსები. მაგ: AgNO3, TiO და [Cr (OH)3(ჰ2ო)3] |
მინერალებში ოქსიდების სახით. |
| 13 | მყარი გარემო პირობებში, ვერცხლი, ბორის გარდა. | ოქსიდები მაგ: ბ2ო3 |
მინერალებში ოქსიდების სახით. |
| 14 | მყარია გარემო პირობებში. | C და Si– ს ატომებს შეუძლიათ ჯაჭვებში განლაგება და უზარმაზარი მრავალფეროვანი ნივთიერებების წარმოება. | ცოცხალ ორგანიზმებში და სილიკატების ან ოქსიდების სახით. |
| 15 | მყარი, გარდა აზოტისა, რომელიც აირია ატმოსფერულ პირობებში. | ოქსიდები და მჟავები მაგ: არა2 და ჰ3მტვერი4 |
ატმოსფერო, ცოცხალი ორგანიზმები და მინერალები. |
| 16 | მყარი, გარდა ჟანგბადის, რომელიც აირისებრია ატმოსფერულ პირობებში. | სულფიდები და ოქსიდები მაგ: ZnS და SiO2 |
ატმოსფერო, ცოცხალი ორგანიზმები და მინერალები. |
| 17 | ისინი ქმნიან დიატომიურ მოლეკულებს და ძალიან რეაქტიული არიან. ისინი ელექტროენერგიისა და სითბოს ცუდი გამტარნი არიან. ისინი აგრესიულები არიან ცოცხალი არსებებისა და გარემოს მიმართ. | მჟავები და მარილები. მაგ: HCl და KBr |
იმყოფებიან ნივთიერებებში ორგანული და მინერალური. |
| 18 | ისინი ძალიან სტაბილურია და გვხვდება გაზების სახით. | ისინი ძნელად ქმნიან რთულ ნივთიერებებს. | გაზები ატმოსფეროში. |
ქიმიური და ფიზიკური თვისებები განასხვავებს ერთ ოჯახს ოჯახისგან. როგორც ვნახეთ, ქიმიური თვისებები უკავშირდება ელექტრონები ვალენტობის, და მათი მეშვეობით, ატომი ურთიერთქმედებს სხვასთან, პასუხისმგებელია ქიმიურ ქცევაზე და ქიმიური ბმები ჩამოყალიბდა.
იმავე ჯგუფის ელემენტების ფიზიკური თვისებები შეიძლება განსხვავდებოდეს ატომური რიცხვისა და მასის მიხედვით.
Სავარჯიშოები
ახლა, როდესაც თქვენ ცოტა მეტი იცით პერიოდული ცხრილის ოჯახების შესახებ, შეამოწმეთ თქვენი ცოდნა და ნახეთ რა ისწავლეთ.
1) განვიხილოთ პერიოდული ცხრილიდან შემდეგი ამონაწერი.
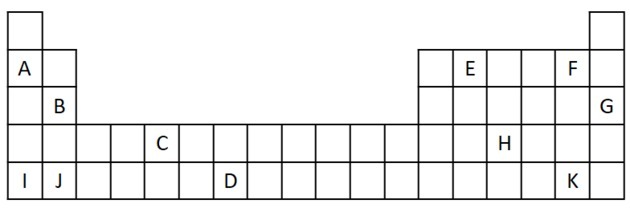
ა) დაასახელეთ ორი ელემენტი, რომლებსაც აქვთ ორი ვალენტური ელექტრონი.
ბ) მიუთითეთ ელემენტი, რომელიც მწვავედ რეაგირებს წყალთან და წარმოქმნის ლითონის ჰიდროქსიდს.
გ) მიუთითეთ არარეაქტიული ელემენტი.
დ) მიუთითეთ ორი ელემენტი, რომლებიც გაერთიანებულია ტუტე მეტალებთან და წარმოქმნის მარილებს.
პასუხი:
ა) B და J
ორი ვალენტური ელექტრონი შეესაბამება ჯგუფს 2, რომელსაც აქვს ns ელექტრონის კონფიგურაცია2 და სავარჯიშოში წარმოდგენილია B და J.
ბ) A, B, I ან J.
მე და A წარმოვადგენთ ოჯახის 1 ელემენტს; B და J 2 ოჯახიდან არიან. როგორც თვისებების ცხრილში ვნახეთ, 1 და 2 ჯგუფის ელემენტები ძალიან რეაგირებენ და შეუძლიათ შექმნან ჰიდროქსიდები, როგორც მოცემულ მაგალითებში: KOH და Mg (OH)2.
გ) გ
კეთილშობილი გაზები ძალიან სტაბილურია და, შესაბამისად, არ არის ძალიან რეაქტიული. ასო G მოცემულია ცხრილში, როგორც ამ ოჯახის ელემენტი.
დ) F და K
ჰალოგენები რეაგირებენ ტუტე მეტალებთან და ქმნიან მარილებს. ამის ყველაზე გავრცელებული მაგალითია სუფრის მარილი, NaCl.
2) შემდეგ ნახატზე მოცემულია სამი ქიმიური ელემენტი, მარცხნიდან მარჯვნივ, ლითიუმი, ნატრიუმი და კალიუმი.

შეარჩიეთ ვარიანტი, რომელიც სწორად ასრულებს თითოეულ შემდეგ დებულებას.
1.1) "შეგვიძლია ვთქვათ, რომ ლითიუმი, ნატრიუმი და კალიუმი ...
(ა)… ეკუთვნის იმავე პერიოდს. ”
(B)… აქვს იგივე ატომური ნომერი. ”
(C)… იმავე ჯგუფს მიეკუთვნება. ”
(D)… აქვს იგივე მასის ნომერი. ”
1.2) "ელემენტები ლითიუმი, ნატრიუმი და კალიუმი ...
(ა)… აქვს ძალიან მსგავსი ქიმიური თვისებები. ”
(B)… აქვს ძალიან განსხვავებული ქიმიური თვისებები. ”
(C) non არალითონებია. ”
(დ)… წყალთან რეაგირება მჟავე ხსნარების შესაქმნელად. ”
პასუხები:
1.1) (C) იმავე ჯგუფს მიეკუთვნება.
1.2) (A) აქვს ძალიან მსგავსი ქიმიური თვისებები.
ამ ინფორმაციის მიღება შეგვიძლია პერიოდული ცხრილის კონსულტაციით ან ელემენტების ლითიუმის, ნატრიუმის და კალიუმის ელექტრონული განაწილებით. ჩვენ ვნახავთ, რომ სამივეს ელექტრონი აქვს ვალენტურ გარსში და რადგან ისინი ერთი ჯგუფის ნაწილია, ქიმიური თვისებები ძალიან ჰგავს ერთმანეთს.
3) განვიხილოთ შემდეგი ცხრილი, სადაც წარმოდგენილია ზოგიერთი ქიმიური ელემენტის ატომური რიცხვები და ელექტრონული განაწილება.
| ელემენტი | ქიმიური სიმბოლო | ატომური ნომერი | Eletronic განაწილება |
|---|---|---|---|
| ლითიუმი | წაიკითხა | 3 | 2,1 |
| ბერილიუმი | იყოს | 4 | 2,2 |
| ფტორი | ვ | 9 | 2,7 |
| ნეონი | ჰაჰ | 10 | 2,8 |
| ქლორი | კლ | 17 | 2,8,7 |
| არგონი | Საჰაერო | 18 | 2,8,8 |
| კალიუმი | კ | 19 | 2,8,8,1 |
| კალციუმი | Აქ | 20 | 2,8,8,2 |
მიუთითეთ თითოეული ელემენტის ჯგუფი.
პასუხი:
ლითიუმი და კალიუმი: ჯგუფი 1. (მათ აქვთ ელექტრონი ვალენტურ გარსში).
ბერილიუმი და კალციუმი: ჯგუფი 2. (მათ აქვთ ორი ელექტრონი ვალენტურ გარსში).
ფტორი და ქლორი: ჯგუფი 17. (მათ აქვთ შვიდი ელექტრონი ვალენტურ გარსში).
ნეონი და არგონი: ჯგუფი 18. (მათ აქვთ რვა ელექტრონი ვალენტურ გარსში).
შეამოწმეთ მისაღები გამოცდის კითხვები კომენტარებული რეზოლუციით სავარჯიშოები პერიოდულ ცხრილზე და გამოუქვეყნებელი კითხვები ამ თემაზე პერიოდული ცხრილის ორგანიზებაზე სავარჯიშოები.