ნიობიუმი (Nb) არის ატომური რიცხვის 41 ქიმიური ელემენტი, რომელიც პერიოდული სისტემის მე -5 ჯგუფს მიეკუთვნება.
ეს არის ბუნებრივად ხელმისაწვდომი გარდამავალი ლითონი მყარ მდგომარეობაში, რომელიც 1801 წელს აღმოაჩინა ბრიტანელმა ქიმიკოსმა ჩარლზ ჰეჩეტმა.
მინერალები, რომლებიც შეიცავს ნიობიუმ, იშვიათია მსოფლიოში, მაგრამ უხვადაა ბრაზილიაში, ამ ლითონის უდიდესი მარაგების მქონე ქვეყანაში.
თავისი თვისებების, მაღალი გამტარობისა და კოროზიის წინააღმდეგობის გამო, ამ ელემენტს აქვს მრავალი პროგრამა, დაწყებული ფოლადის წარმოებიდან დამთავრებული რაკეტის წარმოებამდე.
შემდეგ, ჩვენ გავეცნობით ამ ქიმიურ ელემენტს და მახასიათებლებს, რაც მას ასე მნიშვნელოვნად აქცევს.
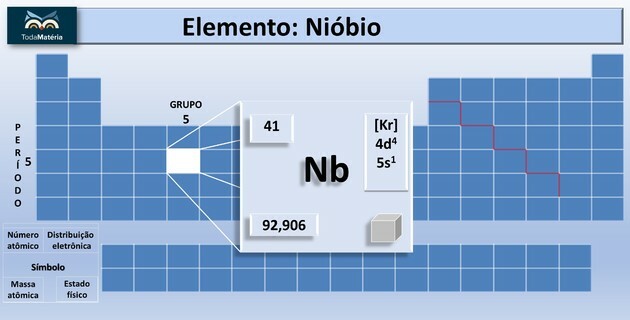
რა არის ნიობიუმი?
ნიობიუმი ცეცხლგამძლე მეტალია, ანუ ის ძალზე მდგრადია სითბოს და ცვეთის მიმართ.
ამ კლასის ლითონებია: ნიობიუმი, ვოლფრამი, მოლიბდენი, ტანტალი და რინიუმი, ნიობიუმი ყველაზე მსუბუქია.
ნიობიუმი ბუნებაში გვხვდება მინერალებში, რომლებიც ჩვეულებრივ უკავშირდება სხვა ელემენტებს, ძირითადად ტანტალს, რადგან მათ ორივეს ძალიან ჰგავს ფიზიკურ-ქიმიური თვისებები.
ეს ქიმიური ელემენტი კლასიფიცირებულია როგორც გარდამავალი მეტალი პერიოდულ სისტემაში. ეს არის ნათელი, დაბალი სიმტკიცე, დაბალი წინააღმდეგობა ელექტრული დენის გავლასთან და მდგრადია კოროზიის მიმართ.
ნიობიუმის ფიზიკური თვისებები
| ფიზიკური მდგომარეობა | მყარია ოთახის ტემპერატურაზე |
|---|---|
| ფერი და გარეგნობა | მეტალის ნაცრისფერი |
| სიმჭიდროვე | 8,570 გ / სმ3 |
| შერწყმის წერტილი | 2468 ° C |
| Დუღილის წერტილი | 4742 ° C |
| კრისტალური სტრუქტურა | სხეულზე ორიენტირებული კუბიკი - CCC |
თერმული კონდუქტომეტრული |
54,2 ვტ მ-1 კ-1 |
ნიობიუმის ქიმიური თვისებები
| კლასიფიკაცია | გარდამავალი ლითონი |
|---|---|
| ატომური ნომერი | 41 |
| ბლოკი | დ |
| ჯგუფური | 5 |
| დროის კურსი | 5 |
| ატომური წონა | 92,90638 u |
| ატომური სხივი | 1,429 Å |
| საერთო იონები | შენიშვნა5+ და ნბ3+ |
| ელექტრონეგატიურობა | 1.6 პაულინგი |
ამ ლითონის გამოყენების მთავარი უპირატესობა ის არის, რომ ამ ელემენტის მხოლოდ რაოდენობას, გრამებში შეუძლია შეცვალოს რკინის ტონა, რაც ლითონს მსუბუქს ხდის, კოროზიისადმი მდგრადია და სხვა ეფექტური
სად გვხვდება ნიობიუმი?
ბუნებაში არსებულ სხვა ნივთიერებებთან შედარებისას, ნიობიუმს აქვს დაბალი კონცენტრაცია, 24 მილიონი ნაწილის პროპორციით.
ეს ლითონი გვხვდება შემდეგ ქვეყნებში: ბრაზილია, კანადა, ავსტრალია, ეგვიპტე, კონგოს დემოკრატიული რესპუბლიკა, გრენლანდია, რუსეთი, ფინეთი, გაბონი და ტანზანია.
ნიობიუმი ბრაზილიაში
1950-იან წლებში ბრაზილიელმა გეოლოგმა ჯალმა გუიმარესმა აღმოაჩინა პიროქლორის მადნის უდიდესი საბადო, რომელიც ამ ლითონს შეიცავს.
დიდი რაოდენობით მადნები, რომლებიც შეიცავს ნიობიუმს, მდებარეობს ბრაზილიაში, მსოფლიოს უდიდეს მწარმოებელში, რომელიც ლითონის მარაგების 90% -ზე მეტს ფლობს.
შესწავლილი ნაკრძალები მდებარეობს მინას ჯერაისის, ამაზონასის, გოიასისა და რონდონიას შტატებში.
ნიობიუმის მადნები
ნიობიუმი ბუნებაში გვხვდება, რომელიც ყოველთვის უკავშირდება სხვა ქიმიურ ელემენტებს. უკვე ცნობილია 90 – ზე მეტი მინერალური სახეობა, რომლებიც ბუნებაში შეიცავს ნიობიუმ და ტანტალს.
ქვემოთ მოცემულ ცხრილში შეიძლება ნახოთ საბადოები, რომლებიც შეიცავს ნიობიუმს, ძირითად მახასიათებლებს და ნიობიუმის შემცველობას თითოეულ მასალაში.
| კოლუმბიტი ტანტალიტი | |
|---|---|
 | |
| შემადგენლობა: | (Fe, Mn) (Nb, Ta)2ო6 |
| ნიობიუმის შემცველობა (მაქსიმალური): | Nb 76%2ო5 |
| Მახასიათებლები: |
|
| პიროქლორიტი | |
|---|---|
 | |
| კომპოზიცია: | (ზე2,Აქ)2(Nb, Ti) (O, F)7 |
| ნიობიუმის შემცველობა (მაქსიმალური): | Nb 71%2ო5 |
| მახასიათებლები: |
|
| ლოპარიტი | |
|---|---|
 | |
| შემადგენლობა: | (C, Na, C)2(Ti, Nb)2ო6 |
| ნიობიუმის შემცველობა (მაქსიმალური): | Nb 20%2ო5 |
| Მახასიათებლები: |
|
ნიობიუმის გამოკვლევა
ნიობიუმის მადნები განიცდიან გარდაქმნებს მანამ, სანამ პროდუქტები არ წარმოიქმნება ბაზარზე.
პროცესის ნაბიჯების შეჯამება შეიძლება შემდეგნაირად:
- სამთო
- ნიობიუმის კონცენტრაცია
- ნიობიუმის გადამუშავება
- ნიობიუმის პროდუქტები
სამთო მოპოვება ხდება იქ, სადაც მადნის მარაგია, რომლებიც მოიპოვება ასაფეთქებელი ნივთიერებების გამოყენებით და გადაჰყავთ ქამრებით იქ, სადაც ხდება კონცენტრაციის ეტაპი.
კონცენტრაცია ხდება მადნის დაშლისთანავე, დაფქვის შედეგად კრისტალები უფრო წვრილდება და ხდება მათი გამოყენება მაგნიტური გამოყოფა რკინის ფრაქციები ამოღებულია საბადოდან.
ნიობიუმის გადამუშავებისას ხდება გოგირდის, წყლის, ფოსფორისა და ტყვიის მოცილება.
ნიობიუმის შემცველი ერთ-ერთი პროდუქტია რკინის-ნიობიუმის შენადნობი, რომელიც მზადდება შემდეგი განტოლების შესაბამისად:
ამ პროცესს ალუმინოთერმიას უწოდებენ, როდესაც მადნის კონცენტრატი რეაქტორებში შერეულია რკინის ჯართით ან რკინის ოქსიდით.
ლითონის ოქსიდები რეაგირებენ ალუმინთან მაღალი ტემპერატურის პირობებში და წარმოქმნიან საინტერესო პროდუქტს.
ნიობიუმის ყველაზე გაყიდვადი პროდუქტებია:
- ნიობიუმის კონცენტრატები: ფუძე, რომელიც შეიცავს 58% Nb- ს2ო5.
- რკინა-ნიობიუმის შენადნობი: შეიცავს 65% ნიობიუმს.
- მაღალი სისუფთავის ოქსიდი: გამოიყენება სპეციალური მასალების წარმოებაში.
რისთვის არის ნიობიუმი?
ნიობიუმის მახასიათებლები ამ ელემენტს უფრო სასურველს ხდის და უთვალავი რაოდენობით ხმარდება.
1905 წლიდან მისი აღმოჩენის შემდეგ, ნიობიუმზე განაცხადების გამოკვლევა დაიწყო, როდესაც გერმანელმა ქიმიკოსმა ვერნერ ფონ ბოლტონმა წარმოადგინა ელემენტი სუფთა სახით.
50-იანი წლები წარმოადგენდა ნიობიუმის აპლიკაციების დიდ ძიებას, რადგან მანამდე ის არ წარმოებულა ფართო მასშტაბით.
ამ პერიოდის განმავლობაში ცივმა ომმა გამოიწვია ინტერესი ამ ლითონის მიმართ, რომელიც კოსმოსური კომპონენტებისთვის უნდა გამოეყენებინა.
ქვემოთ მოცემულია ნიობიუმის გამოყენების გზების ჩამონათვალი.
ლითონის შენადნობები

ნიობიუმის დამატება შენადნობში ზრდის მის გამკვრივებას, ანუ გამკვრივების უნარს სითბოს ზემოქმედების და შემდეგ გაცივების დროს. ამრიგად, ნიობიუმის შემცველი მასალა შეიძლება დაექვემდებაროს სპეციფიკურ სითბოს მკურნალობას.
ნახშირბადთან და აზოტთან ნიობიუმის მიჯაჭვულობა ხელს უწყობს შენადნობის მექანიკურ თვისებებს, ზრდის, მაგალითად, მექანიკურ სიმტკიცეს და გამძლეობას აბრაზიული ცვეთის მიმართ.
ეს ეფექტები სასარგებლოა, რადგან მათ შეუძლიათ გააგრძელონ შენადნობის სამრეწველო გამოყენება.
ფოლადი, მაგალითად, არის მეტალის შენადნობი, რომელსაც წარმოქმნის რკინა და ნახშირბადი. ნიობიუმის დამატება ამ შენადნობში შეიძლება ჰქონდეს უპირატესობები:
- Საავტომობილო ინდუსტრია: მსუბუქი ავტომობილის წარმოება და უფრო მდგრადია შეჯახებისგან.
- მშენებლობა: აუმჯობესებს ფოლადის შედუღებადობას და უზრუნველყოფს დამუშავებას.
- სატრანსპორტო მილსადენების ინდუსტრია: საშუალებას აძლევს კონსტრუქციებს უფრო თხელი კედლებით და უფრო დიდი დიამეტრით, უსაფრთხოებაზე გავლენის გარეშე.
სუპერ შენადნობები

სუპერშენადნობი არის მეტალის დისკები, მაღალი გამძლეობით მაღალი ტემპერატურისა და მექანიკური სიმტკიცის მიმართ. ნიობიუმის შემცველი შენადნობები ამ მასალას გამოსადეგია საჰაერო ტურბინების წარმოებაში ან ენერგიის წარმოებაში.
მაღალ ტემპერატურაზე მუშაობის უპირატესობა სუპერ შენადნობებს ქმნის მაღალი ხარისხის რეაქტიული ძრავებისაგან.
ზეგამტარი მაგნიტები

ნიობიუმის ზეგამტარობა იწვევს ნიობიუმ-გერმანიუმის, ნიობიუმ-სკანდიუმის და ნიობიუმ-ტიტანის ნაერთების გამოყენებას:
- MRI აპარატების სკანერი.
- ნაწილაკების ამაჩქარებლები, როგორიცაა დიდი ადრონული კოლაიდერი.
- ელექტრომაგნიტური გამოსხივების აღმოჩენა და კოსმოსური გამოსხივების შესწავლა ნიობიუმის ნიტრიტის შემცველი მასალებით.
ოქსიდები
ნიობიუმის სხვა გამოყენება ხდება ოქსიდების, ძირითადად Nb– ის სახით2ო5. ძირითადი მიზნებია:
- ოპტიკური ლინზები
- კერამიკული კონდენსატორები
- pH სენსორები
- ძრავის ნაწილები
- სამკაულები
ნიობიუმის ისტორია და აღმოჩენა
1734 წელს ჯონ უინთროპის პირადი კოლექციის ზოგიერთი მადნები ამერიკიდან ინგლისში გადაიტანეს და ეს ნივთები ლონდონის ბრიტანეთის მუზეუმის კოლექციის ნაწილი იყო.
სამეფო საზოგადოებაში გაწევრიანების შემდეგ, ბრიტანელმა ქიმიკოსმა ჩარლზ ჰეტჩეტმა ყურადღება გაამახვილა მუზეუმში არსებული მადნების შემადგენლობის გამოკვლევაზე. ასე 1801 წელს მან გამოყო ქიმიური ელემენტი, ოქსიდის სახით და დაარქვა მას კოლუმბიუმი და მადნეული, საიდანაც მოპოვებული იქნა კოლუმბიტი.
1802 წელს შვედმა ქიმიკოსმა ანდერს გუსტაფ ეკერბერგმა მოახსენა ახალი ქიმიური ელემენტის აღმოჩენის შესახებ და მას ტანტალი უწოდა, ბერძნულ მითოლოგიაში ზევსის ძის მითითებით.
1809 წელს ინგლისელმა ქიმიკოსმა და ფიზიკოსმა უილიამ ჰაიდ ვოლასტონმა გააანალიზა ეს ორი ელემენტი და დააკვირდა, რომ მათ ძალიან ჰგავს მსგავსი მახასიათებლები.
ამ ფაქტის გამო, 1809 წლიდან 1846 წლამდე კოლუმბიუმი და ტანტალი იგივე ელემენტად ითვლებოდა.
მოგვიანებით, გერმანელმა მინერალოგმა და ქიმიკოსმა ჰაინრიხ როუზმა, რომელიც იკვლევდა კოლუმბიტის მადნს, აღნიშნა, რომ ტანტალიც იყო.
როუზმა აღმოაჩინა ტანტალის მსგავსი სხვა ელემენტის არსებობა და მას უწოდა ნიობიუსი, ბერძნული მითოლოგიიდან, ტანტალუსის ასულის, ნიობეს მითითებით.
1864 წელს შვედმა ქრისტიან ბრომსტრანდმა მოახერხა ნიობიუმის იზოლირება წყალბადის ატმოსფეროში გაცხელებული ქლორიდის ნიმუშიდან.
1950 წელს სუფთა და გამოყენებითი ქიმიის კავშირმა (IUPAC) დაამტკიცა ნიობიუმი, როგორც ოფიციალური სახელი და არა კოლუმბიუმი, რადგან ისინი იგივე ქიმიური ელემენტია.
ნიობიუმის რეზიუმე
ქიმიური ელემენტი: ნიობიუმი | |||
|---|---|---|---|
| სიმბოლო | შენიშვნა | აღმომჩენი | ჩარლზ ჰეტჩეტი |
| ატომური ნომერი | 41 | ატომური მასა | 92 906 უ |
| ჯგუფური | 5 | დროის კურსი | 5 |
| კლასიფიკაცია | გარდამავალი ლითონი | Eletronic განაწილება | [Kr] 4d35-იანები2 |
| მახასიათებლები |
|
||
| მთავარი მადნები |
|
||
| ძირითადი პროდუქტები |
|
||
| პროგრამები |
|
||
| შემთხვევა | Მსოფლიოში |
|
|
| Ბრაზილიაში |
|
მტრების სავარჯიშოები და მისაღები გამოცდები
1. (Enem / 2018) ბერძნულ მითოლოგიაში ნიობია ტანტანუსის ქალიშვილი იყო, ორი პერსონაჟი, რომელიც ცნობილია ტანჯვით. ქიმიური ელემენტი ატომური ნომრით (Z) 41 – ის ტოლია ქიმიური და ფიზიკური თვისებები იმდენად მსგავსია ატომური ნომერი 73 – ის ელემენტთან, რომ ისინი დაიბნა.
ამიტომ, ბერძნული მითოლოგიის ამ ორი პერსონაჟის საპატივცემულოდ, ამ ელემენტებს მიენიჭათ ნიობიუმის (Z = 41) და ტანტალის (Z = 73) სახელები. ამ ორმა ქიმიურმა ელემენტმა დიდი ეკონომიკური მნიშვნელობა შეიძინა მეტალურგიაში, წარმოებაში სუპერგამტარები და მაღალი დონის ინდუსტრიის სხვა პროგრამებში, სწორედ ქიმიური და ფიზიკური თვისებების გამო ორივესთვის საერთო.
კეანი, ს. ქრება კოვზი: და სხვა ჭეშმარიტი ისტორიები სიგიჟის, სიყვარულისა და ქიმიური ელემენტებისგან სიკვდილის შესახებ. რიო დე ჟანეირო: ზაჰარი, 2011 (ადაპტირებულია).
ამ ელემენტების ეკონომიკური და ტექნოლოგიური მნიშვნელობა განპირობებულია მათი ქიმიური და ფიზიკური თვისებების მსგავსებით
ა) ჰქონდეს ელექტრონები ვ ქვედენაში.
ბ) შინაგანი გადასვლის ელემენტები.
გ) პერიოდულ ცხრილში იმავე ჯგუფს მიეკუთვნება.
დ) აქვთ მათი ყველაზე შორეული ელექტრონები, შესაბამისად, 4 და 5 დონეზე.
ე) განლაგდეს ტუტე მიწის და ტუტეების ოჯახში, შესაბამისად.
სწორი ალტერნატივა: გ) პერიოდულ ცხრილში იმავე ჯგუფს მიეკუთვნება.
პერიოდული სისტემა ორგანიზებულია 18 ჯგუფად (ოჯახებად), სადაც თითოეულ ჯგუფს აერთიანებს მსგავსი თვისებების ქიმიური ელემენტები.
ეს მსგავსება ხდება იმის გამო, რომ ჯგუფის ელემენტებს იგივე რაოდენობის ელექტრონები აქვთ ვალენტურ გარსში.
ელექტრონული განაწილების გაკეთება და ელექტრონების დამატება ყველაზე ენერგიული ქვესკნელიდან უკიდურეს ქვეგანშენებამდე ვხვდებით ჯგუფს, რომელსაც ორი ელემენტი ეკუთვნის.
| ნიობიუმი | |
|
განაწილება ელექტრონიკა |
1 ს2 2-იანები2 2 გვ6 3 ს2 3 გვ6 4-იანები2 3D10 4 გვ65-იანები2 4 დ3 |
|
ჯამი ელექტრონები |
უფრო ენერგიული + უფრო გარეგანი 4 დ3 + 5 წმ2 = 5 ელექტრონი |
| ჯგუფური | 5 |
| ტანტალი | |
|
განაწილება ელექტრონიკა |
1 ს2 2-იანები2 2 გვ6 3 ს2 3 გვ6 4-იანები2 3D10 4 გვ6 5-იანები2 4 დ10 5 გვ66 წლები2 4 ვ145 დ3 |
|
ჯამი ელექტრონები |
უფრო ენერგიული + უფრო გარეგანი 5 დ3 + 6 წმ2 = 5 ელექტრონი |
| ჯგუფური | 5 |
ელემენტები ნიობიუმი და ტანტალი:
- ისინი პერიოდულ ცხრილში იმავე ჯგუფს მიეკუთვნებიან.
- მათ აქვთ ყველაზე შორეული ელექტრონები, შესაბამისად, 5 და 6 დონეზე და ისინი განლაგებულია მე -5 და მე -6 პერიოდში.
- მათ აქვთ ელექტრონები დ ქვექვემდებარებაში და, შესაბამისად, ისინი გარდამავალი ელემენტებია.
2. (IFPE / 2018) ბრაზილია არის მსოფლიოში ყველაზე დიდი ნიობიუმის მწარმოებელი, ამ ლითონის მარაგის 90% -ზე მეტს შეადგენს. ნიობიუმი, Nb სიმბოლო, გამოიყენება სპეციალური ფოლადების წარმოებაში და კოროზიის და ექსტრემალური ტემპერატურის ერთ-ერთი ყველაზე მდგრადი ლითონია. Nb ნაერთი2ო5 ეს არის თითქმის ყველა შენადნობებისა და ნიობიუმის ნაერთების წინამორბედი. მონიშნეთ ალტერნატივა Nb– ის საჭირო მასით2ო5 მიიღონ 465 გრამი ნიობიუმი. მოცემულია: Nb = 93 გ / მოლ და O = 16 გ / მოლ.
ა) 275 გ
ბ) 330 გ
გ) 930 გ
დ) 465 გ
ე) 665 გ
სწორი ალტერნატივა: ე) 665 გ
ნიობიუმის წინამორბედი ნაერთია Nb ოქსიდი2ო5 და შენადნობებში გამოყენებული ნიობიუმი არის ელემენტარული ფორმის Nb.
ამიტომ, ჩვენ გვაქვს შემდეგი სტეიომეტრიული კავშირი:
Nb 1 მოლი2ო5 წარმოქმნის 2 მოლ Nb, რადგან ნიობიუმის ოქსიდი იქმნება ამ ლითონის 2 ატომით.
პირველი ეტაპი: გამოთვალეთ წარმოებული ნიობიუმის მოლების რაოდენობა, რომელიც შეესაბამება 465 გ-ს.
თუ გაანგარიშებით დავინახეთ, რომ ნიობიუმის მასა შეესაბამება 5 მოლს, მაშინ Nb მოლების რაოდენობა2ო5 გამოყენებულია ამ მნიშვნელობის ნახევარი, რადგან:
მე -2 ეტაპი: გამოთვალეთ ნიობიუმის ოქსიდის მოლური მასა.
მე -3 საფეხური: გამოთვალეთ ნიობიუმის ოქსიდის მასა, რომელიც შეესაბამება 2,5 მოლს.
3. (UECE / 2015) ბრაზილია ფლობს მსოფლიოში ნიობიუმის მარაგების 98% -ს, რომელსაც აქვს მრავალი სამრეწველო პროგრამა, მაგალითად, ძვირფასეულობის წარმოებაში, ჰიპერალერგენული იმპლანტები, ელექტროსერამიკა, სუპერგამტარ მაგნიტები, მაგნიტურ-რეზონანსული აპარატები, ლითონის შენადნობები, სპეციალური მონეტები და ფოლადი. ნიობიუმისთვის გადახედეთ ქვემოთ მოცემულ დებულებებს და აღნიშნეთ ერთადერთი ნამდვილი ალტერნატივა.
ა) მისი დიფერენცირებული ელექტრონი განლაგებულია ბოლოსწინა გარსში.
ბ) ეს არის წარმომადგენლობითი ელემენტი.
გ) მისი ელექტრონეგატიურობა უფრო დაბალია, ვიდრე ვანადიუმისა.
დ) პერიოდული ცხრილის მეოთხე პერიოდს განეკუთვნება.
სწორი ალტერნატივა: ა) მისი დიფერენციალური ელექტრონი განლაგებულია ბოლოსწინა გარსში.
ნიობიუმის ელექტრონული განაწილების განხორციელებისას, შესაძლებელია იმის დანახვა, რომ მისი დიფერენციალური ელექტრონი მდებარეობს წინა ბოლოს გარსში.
იმის გამო, რომ მას აქვს დიფერენცირებული ელექტრონი d ქვექვემდებარებაში, ეს არის გარე გარდამავალი ელემენტი.
ვინაიდან მისი ყველაზე შორეული დონე მეხუთე ფენაშია, ნიობიუმი მაგიდის მეხუთე პერიოდში მდებარეობს.
ელექტრონეგატიულობა არის თვისება, რომელიც უკავშირდება ელემენტის ელექტრონების მოზიდვის უნარს და ის იცვლება ატომური რადიუსი: რაც უფრო მცირეა ატომური რადიუსი, მით მეტია ელექტრონების მოზიდვა და, შესაბამისად, მით უფრო დიდია ელექტრონეგატიურობა.
ცხრილის ელექტრონეგატივობის მნიშვნელობებთან დაკავშირებით, შესაძლებელია დაინახოთ, რომ ნიობიუმსა და ვანადიუმს აქვთ 1,6 პაულინგის სიახლოვე.
4. (UEA / 2014) ნიობიუმის ბუნებრივი იზოტოპია 93შენიშვნა ნეიტრონების რაოდენობა ამ იზოტოპში არის
ა) 41.
ბ) 52.
გ) 93.
დ) 134.
ე) 144.
სწორი ალტერნატივა: ბ) 52.
იზოტოპები არის ქიმიური ელემენტის ატომები, სხვადასხვა მასის რაოდენობით.
ატომური მასა შეესაბამება ელემენტის პროტონებისა და ნეიტრონების ჯამს.
პროტონის რაოდენობა წარმოადგენს ქიმიური ელემენტის ატომურ რაოდენობას და იზოტოპებისთვის ის არ იცვლება.
ამრიგად, იზოტოპების მასობრივი ვარიაცია ხდება ნეიტრონების განსხვავებული რაოდენობის გამო.
თუ ნიობიუმის ატომური რაოდენობაა 41, მაშინ ნეიტრონების რაოდენობა მოცემულია გაანგარიშებით:
5. (IFMG / 2015) ქიმიური ელემენტი ნიობიუმი, Nb, ბერძნული ქალღმერთის ნიობეს სახელს ატარებს. ბრაზილია ლითონის მსოფლიოში უდიდესი მწარმოებელია, წარმოების 75% -ს შეადგენს. მისი შენადნობების თერმული სტაბილურობის გამო, ნიობიუმი გამოიყენება ძრავების, წინაძრავის მოწყობილობებისა და სხვადასხვა ზეგამტარ მასალების სპეციალური მაღალი სიმტკიცე ფოლადის შენადნობების წარმოებაში. პერიოდულ ცხრილში ნიობიუმის პოზიციის დაკვირვებით, სწორია იმის თქმა, რომ:
ა) თქვენი ყველაზე ენერგიული ქვესკნელი იქნება ქვედენა დ.
ბ) არის ტუტე ლითონების ოჯახის კუთვნილი ელემენტი.
გ) ქმნის სხვა იონურ ნაერთებს სხვა მეტალებთან.
დ) მის კატიონებს ექნებათ სუფთა ელემენტზე მეტი ატომური რადიუსი.
სწორი ალტერნატივა: ა) თქვენი ყველაზე ენერგიული ქვესკნელი იქნება ქვედენა დ.
პერიოდული ცხრილის დათვალიერებით ვხვდებით, რომ ნიობიუმი ხასიათდება როგორც გარე გარდამავალი ელემენტი, რომელიც პერიოდული ცხრილის მე -5 ჯგუფს მიეკუთვნება, რადგან მისი ყველაზე ენერგიული ქვექვეშა დ არის.
ამ ინფორმაციას ასევე შეგვიძლია მივიღოთ ელექტრონული გზით.
რადგან ეს არის მეტალი, ეს ელემენტი ქმნის მეტალურ კავშირებს სხვა მეტალებთან, როგორც შენადნობთან რკინა-ნიობიუმი ან ასევე კოვალენტური ბმები, ელექტრონების გაზიარებით, როგორც ნიობიუმის ოქსიდში შენიშვნა2ო5.
6. (UFSC / 2003) ნიობიუმი აღმოაჩინა 1801 წელს, ინგლისელმა ქიმიკოსმა ჩარლზ ჰეჩეტმა. ბრაზილია ფლობს ნიობიუმის კონცენტრატის მსოფლიო წარმოების 93% -ს. ყველაზე დიდი საბადოები მდებარეობს მინას ჯერაისის, გოიასისა და ამაზონის შტატებში. მეტალს ძირითადად იყენებენ რკინა-ნიობიუმის შენადნობების და სხვა უფრო რთული შენადნობების წარმოებაში, რომლებიც გამოყენებულია რეაქტიული ტურბინების, რაკეტებისა და კოსმოსური ხომალდების მშენებლობაში. მისი ოქსიდები გამოიყენება სათვალის, ფოტოგრაფიული კამერების და სხვა ოპტიკური აღჭურვილობის მსუბუქი ლინზების წარმოებაში. მოცემულია (Z = 41). რაც შეეხება ნიობიუმს, მონიშნეთ სწორი წინადადება (ებ) ი.
(01) ნიობიუმი, 3 ელექტრონის დაკარგვისას, იღებს კრიპტონის კონფიგურაციას.
(02) ნიობიუმს შეუძლია შექმნას M ტიპის ლითონის ოქსიდები2ო5 წელს2ო3.
(04) ნიობიუმის ქიმიური სიმბოლოა Ni.
(08) ნიობიუმი გარდამავალი მეტალია.
(16) რკინა-ნიობიუმის შენადნობი არის მყარი ხსნარის მაგალითი.
სწორი ალტერნატივები: 02 + 08 + 16 = 26.
(01) არასწორი.
| ელემენტები | Eletronic განაწილება |
| 36კრ | 1 ს2 2-იანები2 2 გვ6 3 ს2 3 გვ6 4-იანები2 3D10 4 გვ6 |
|
41შენიშვნა 41შენიშვნა3+ |
1 ს2 2-იანები2 2 გვ6 3 ს2 3 გვ6 4-იანები2 3D10 4 გვ6 5-იანები2 4 დ3 1 ს2 2-იანები2 2 გვ6 3 ს2 3 გვ6 4-იანები2 3D10 4 გვ6 4 გვ6 4 დ2 |
(02) სწორია
ნიობიუმის 3+ და 5+ დაჟანგვის რიცხვების გათვალისწინებით, მას შეუძლია შექმნას ნაერთები:
| დაჟანგვის ნომერი 5+ | დაჟანგვის ნომერი 3+ |
| შენიშვნა2ო5 | შენიშვნა2ო3 |
(04) არასწორი
ნი არის ნიკელის ელემენტის სიმბოლო. ნიობიუმის სიმბოლოა Nb.
(08) სწორია
ნიობიუმი არის გარე გარდამავალი მეტალი, რომელიც ეკუთვნის პერიოდული სისტემის მე -5 ჯგუფს.
(16) სწორია
მყარი ხსნარი შეესაბამება იმავე ფაზაში ორი ან მეტი კომპონენტის ნარევს, რომელიც მყარია და ლითონებს შორის საერთოა.
7. (UERJ / 2013) ნიობიუმი არის ლითონი, რომელიც გვხვდება ბუნებრივ დეპოზიტებში, ძირითადად ოქსიდების სახით.
დეპოზიტში, რომელიც შეიცავს ნიობიუმს დაჟანგვის ნომრით +5, ამ ლითონის უპირატეს ოქსიდის ფორმულა შეესაბამება:
ა) NbO5
ბ) ნბ5ო
გ) Nb5ო2
დ) ნბ2ო5
სწორი ალტერნატივა: დ) ნბ2ო5
ჟანგბადი ქმნის ორ კავშირს და აქვს ფიქსირებული დაჟანგვის ნომერი, რომელიც არის 2-.
ამიტომ, ნიობიუმის ოქსიდის შესაქმნელად, ჟანგბადი უნდა დაერთოს ამ ლითონის 2 ატომს.
ნიობიუმს აქვს სხვადასხვა ჟანგვის მდგომარეობა. დაჟანგვის ნომერი 3+ ის უკავშირდება 3 ჟანგბადს და Nox 5+ ის ქმნის ნაერთს: Nb2ო5 სადაც 2 ნიობიუმის ატომი უკავშირდება 5 ჟანგბადის ატომს.
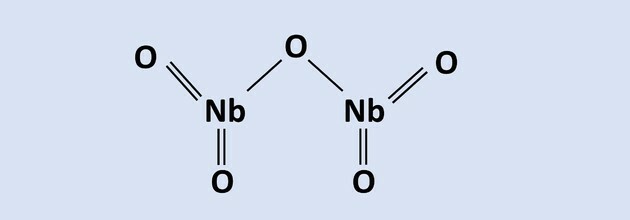
წაიკითხეთ ტექსტი 8-დან 10-მდე კითხვებზე პასუხის გასაცემად.
ნიობიუმი დიდი ტექნოლოგიური მნიშვნელობის ლითონია და მისი ძირითადი მსოფლიო რეზერვები მდებარეობს აქ
ბრაზილია, პიროქლორინის მადნის სახით, რომელიც შედგება Nb2ო5. მისი ექსტრაქციული მეტალურგიის ერთ-ერთ პროცესში ალუმინოთერმია გამოიყენება Fe ოქსიდის არსებობისას2ო3, შედეგად წარმოიქმნება ნიობიუმის და რკინის და ალუმინის ოქსიდის შენადნობი, როგორც სუბპროდუქტი. ამ პროცესის რეაქცია განტოლებაშია წარმოდგენილი:
ბუნებაში, ნიობიუმი ჩნდება სტაბილური იზოტოპის ნიობიუმ -93 სახით, მაგრამ ცნობილია რამდენიმე არასტაბილური სინთეზური იზოტოპი, რომლებიც იშლება რადიაციის გამოსხივებით. ერთ-ერთი მათგანია ნიობიუმ -95, რომელიც იშლება მოლიბდენის -95 ელემენტამდე.
(Systemss.dnpm.gov.br; ტექნოლოგია ლითონი. მატერი. მაღაროელი., სან პაულო, ვ. 6, არა 4, გვ. 185-191, აპრილი-ივნისი. 2010 და გ. Audi და სხვ. / ბირთვული ფიზიკა A 729 (2003) 3–128. ადაპტირებული)
8. (FGV / 2019) ალუმინოთერმიის რეაქციაში ნიობიუმის და რკინის შენადნობის მისაღებად, გაწონასწორებულ განტოლებაში წარმოდგენილი სტეიომეტრიის გათვალისწინებით, პროცესში ჩართული ელექტრონების საერთო რაოდენობაა
ა) 6.
ბ) 12.
გ) 18.
დ) 24.
ე) 36.
სწორი ალტერნატივა: ე) 36.
Redox რეაქცია ხდება ელექტრონების დაკარგვასთან და მოგებასთან ერთად.
როდესაც ელემენტი ამცირებს, ის იძენს ელექტრონებს და როდესაც ელემენტი იჟანგება, ის კარგავს ელექტრონებს.
როდესაც ელემენტი ამცირებს ის არის ჟანგვითი საშუალება, მაშინ როდესაც ელემენტი იჟანგება ეს არის შემამცირებელი საშუალება.
ამ გზით, ელექტრონების რაოდენობა, რომლებიც დაკარგა ერთმა ელემენტმა და მიანიჭა მეორეს, ტოლია.
| ელემენტი | NOX | რეაქცია | ელექტრონები | |
| ნიობიუმი |
+5 3შენიშვნა2ო5 |
0 6Nb |
შემცირება | 3.2.5 = 30 და- მიღწევები |
| რკინა |
+3 რწმენა2ო3 |
0 2Fe |
შემცირება | 2.3 = 6 და- მიღწევები |
| ალუმინის |
0 12ალ |
+3 6 ალ2ო3 |
დაჟანგვა | 6.2.3 = 36 და- დაიკარგა |
ალუმინის მუხტი ალუმინის ოქსიდის პროდუქტზე არის 3+, ანუ თითოეულმა ალუმინმა დაკარგა 3 ელექტრონი.
პროდუქტებში გვაქვს 12 ალუმინის ატომი, რაც პროცესში ჩართული ელექტრონების საერთო რაოდენობას ქმნის:
12. 3 = 36 ელექტრონი.
9. (FGV / 2019) ალუმინოთერმიის დროს ნიობიუმისა და რკინის შენადნობის წარმოებისთვის Nb სტოიომეტრიული რაოდენობით2ო5 და ფე2ო3 და ზედმეტი მეტალის ალუმინის გამოყენება, ჩამოყალიბდა 6,12 ტონა ალ.2ო3. ამ ოპერაციის შედეგად მიღებული ნიობუმისა და რკინის მოლში, თანხების ჯამი შეადგენს
ა) 6 × 104
ბ) 6 106
გ) 8 × 103
დ) 8 × 104
ე) 8 × 106
სწორი ალტერნატივა: დ) 8 × 104.
პირველი ნაბიჯი: გამოთვალეთ Al- ის მოლური მასა2ო3
მე -2 ნაბიჯი: გამოთვალეთ Al- ის მოლების რაოდენობა2ო3
მე -3 ნაბიჯი: შეასრულეთ სტოიქომეტრიული ურთიერთობები.
ქიმიურ განტოლებაში ვხედავთ, რომ არსებობს კავშირი: 6 მოლი ნიობიუმი, 6 მოლი ალუმინის და 2 მოლი რკინის.
წარმოქმნილი მოლების რაოდენობის თანაფარდობით, ჩვენ გვაქვს:
ნიობიუმისა და რკინის რაოდენობით ჯამი, moles, არის:
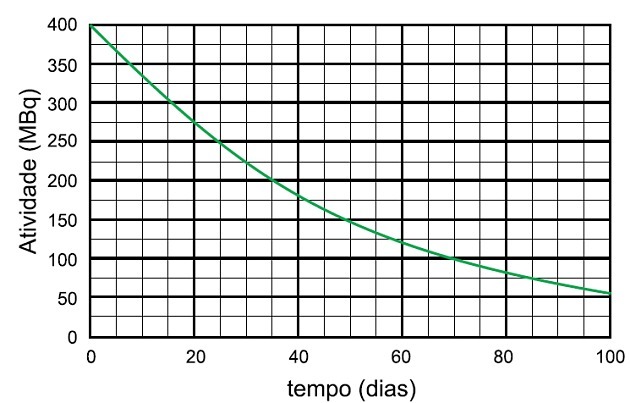
ნიობიუმ -95 რადიოიზოტოპის დაშლის პროცესში, ამ ნიმუშის აქტივობის შესამცირებლად საჭირო დრო 25 MBq და გამოყოფილი სახეობების სახელია
ა) 140 დღე და ნეიტრონები.
ბ) 140 დღე და პროტონები.
გ) 120 დღე და პროტონები.
დ) 120 დღე და ნაწილაკები–.
ე) 140 დღე და ნაწილაკები–.
სწორი ალტერნატივა: ე) 140 დღე და ნაწილაკები–.
ნახევარგამოყოფის პერიოდი არის დრო, რაც საჭიროა რადიოაქტიური ნიმუშის საქმიანობის განახევრებაზე.
დიაგრამაზე ვხედავთ, რომ რადიოაქტიური აქტივობა იწყება 400 MBq- დან, ამიტომ ნახევარგამოყოფის პერიოდი არის დრო, რაც საჭიროა აქტივობის დაშლას 200 MBq- მდე, რაც თავდაპირველის ნახევარია.
გრაფიკში ვაანალიზებთ, რომ ეს დრო იყო 35 დღე.
იმისათვის, რომ აქტივობა ისევ განახევრდეს, გავიდა კიდევ 35 დღე და აქტივობა გადავიდა 200 MBq– დან 100 MBq– ზე, როდესაც სხვა 35 დღე გავიდა, ანუ 400 – დან 100 MBq– მდე 70 დღე გავიდა.
ნიმუშის 25 MBq- მდე დაშლისთვის საჭიროა ნახევარგამოყოფის 4 დრო.
რაც შეესაბამება:
4 x 35 დღე = 140 დღე
რადიოაქტიური დაშლის დროს, ემისიები შეიძლება იყოს ალფა, ბეტა ან გამა.
გამა გამოსხივება არის ელექტრომაგნიტური ტალღა.
ალფა ემისიას აქვს დადებითი მუხტი და ამცირებს მასის 4 ერთეულს და დაშლილი ელემენტის ატომურ რიცხვში 2 ერთეულს, აქცევს მას სხვა ელემენტად.
ბეტა-ემისია არის მაღალსიჩქარიანი ელექტრონი, რომელიც ზრდის დაშლილი ელემენტის ატომურ რაოდენობას ერთი ერთობით, აქცევს მას სხვა ელემენტად.
ნიობიუმ -95 და მოლიბდენ -95 აქვთ იგივე მასა, ამიტომ ბეტა-ემისია მოხდა, რადგან: