ო სარეცხი ფხვნილი ეს არის საწმენდი საშუალება, რომელიც მოსახლეობის დიდი ნაწილის ყოველდღიური ცხოვრების ნაწილია, რადგან ის გამოიყენება ხალხის ტანსაცმლის რეცხვაში. ეს არის პროდუქტი, რომელმაც შეცვალა საპნის საპონი, ვინაიდან, ზოგადად, სარეცხის პროცესში ხალხს ჩვევა ჰქონდა ტანზე ტრიალი.

მაგალითად, ჭურჭლის რეცხვაში ფართოდ გამოიყენება ბარის საპონი
ფხვნილის საპონი პირველად 1946 წელს აწარმოეს, მას შემდეგ, რაც რამდენიმე მცდელობა მოხდა, რომ საპონი საპონი ყოფილიყო. ერთ-ერთი მცდელობა იყო საპნის ფანტელები ან გრანულები წარმოება. ამასთან, ეს მცდელობები წარმატებული არ აღმოჩნდა, რადგან საპონი ურთიერთქმედებს მყარ წყალში არსებულ იონებთან, რაც ძირითადად აფერხებს დასუფთავების მოქმედებას.
რატომ არ შეგვიძლია ასე ვუწოდოთ სამრეცხაოს სარეცხი საშუალება?
ქიმიურად რომ ვთქვათ, სამრეცხაოს სარეცხი საშუალება ასე ვერ დავარქვით. თუ ამ პროდუქტების შეფუთვას დავაკვირდებით, დავინახავთ, რომ მასზე წერია სარეცხი მანქანები და არა სარეცხი ფხვნილი. სწორია მისი დარეკვა ფხვნილის სარეცხი საშუალება, რადგან მისი ქიმიური შემადგენლობა განსხვავდება საპნის შემადგენლობისგან.
სარეცხი ფხვნილის, ან უკეთესი, სარეცხის ფხვნილის ქიმია ეფუძნება საპნის და სარეცხის ძირითად განსხვავებას. იხილეთ ამ მასალების განმარტება და ქიმიური მახასიათებლები:
ა) სარეცხი საშუალებები:
ეს არის ქიმიური ნივთიერებები, რომლებსაც აქვთ ძალიან გრძელი ჯაჭვები (დიდი რაოდენობით ნახშირბადი) მხოლოდ ნახშირბადის და წყალბადის ატომებით არის დაკომპლექტებული, რასაც ჩვენ რეგიონებს ვუწოდებთ არაპოლარული ასევე, ამ გრძელი ჯაჭვის ბოლოს, არსებობს პოლარული ჯგუფი.
სარეცხის პოლარული ნაწილი განპირობებულია სულფონატის ჯგუფის, ანუ გოგირდის ატომის ურთიერთქმედებით ჟანგბადის სამი ატომი, ან ფოსფატის ჯგუფი, რომელსაც აქვს ფოსფორის ატომი, რომელიც ურთიერთქმედებს სამ ატომთან ჟანგბადი. იხილეთ სარეცხი საშუალების სტრუქტურის წარმოდგენა:
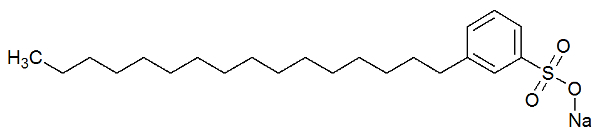
სარეცხი საშუალების სტრუქტურული ფორმულა
სარეცხი საშუალების პოლარული ნაწილი (ნატრიუმის სულფონატის მიერ წარმოქმნილი) შეუძლია წყლის ურთიერთქმედება წყლის მოლეკულებთან. არაპოლარული ნაწილი (მხოლოდ ნახშირბადებისა და წყალბადებისაგან შედგება) ურთიერთქმედებს ცხიმის მოლეკულებთან. ამრიგად, სარეცხი საშუალება ცხიმს წყალთან ურთიერთქმედებაში ქმნის ემულსიას.
ბ) საპნები
მარილები არიან კარბოქსილის მჟავები წარმოიშვა ქიმიური რეაქციიდან ცხიმებსა და ძლიერ ბაზებს შორის, მაგალითად NaOH. იხილეთ საპნის ქიმიური სტრუქტურის წარმოდგენა:
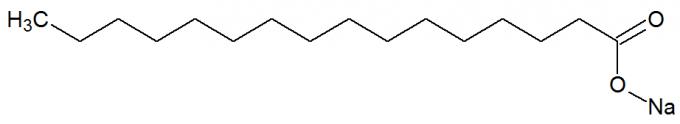
საპნის სტრუქტურული ფორმულა
მათ ასევე აქვთ გრძელი ნახშირბადის ჯაჭვები არაპოლარული და პოლარული ნაწილით. ამ გზით საპნის არაპოლარული ნაწილი (მხოლოდ ნახშირბადებისა და წყალბადებისაგან შედგება) ურთიერთქმედება შეუძლია ცხიმები და მისი პოლარული ნაწილი (წარმოქმნილია COONa ჯგუფის მიერ) წყალთან ერთად ქმნის ემულსიებს, როგორიცაა სარეცხი საშუალებები.
ამ ტექსტის ფოკუსირებულია "საპნის" ფხვნილის ქიმიაუფრო სწორად, ფხვნილის სარეცხი ქიმიური შემადგენლობა, ჩვენ წარმოგიდგენთ ყველა ქიმიურ ნივთიერებას, რომლებიც მისი შემადგენლობის ნაწილია, ასევე თითოეული მათგანის მნიშვნელობა:
ფხვნილის სარეცხი ქიმიური შემადგენლობა
ანიონული ზედაპირული აქტი (როგორიცაა ნატრიუმის ალკილ ბენზოლ სულფონატი და ნატრიუმის ალკილ ეთერ სულფონატი). ისინი უერთდებიან ცხიმის მოლეკულას და წყლის მოლეკულას, რითაც ქსოვილს ცხიმი აშორებს;
ფერმენტები: ლიპაზები და პროტეაზები გამოიყენება ლაქების მოცილებაში. ეს იმიტომ ხდება, რომ ქიმიურად, ფერმენტები ბიოქიმიური კატალიზატორია, რომლებიც ხელს უწყობენ რთული მოლეკულების უფრო მარტივ მოლეკებად გარდაქმნას. ამრიგად, უფრო პატარა მოლეკულების ამოღება უფრო ადვილია ტანსაცმლიდან;
მათეთრებელი (ნატრიუმის პერბორატი): იგი მოქმედებს დაჟანგვის, შემცირების ან ფერმენტული მოქმედებით. წყალში ის აწარმოებს წყალბადის პეროქსიდს, რომელიც ძლიერი მჟანგავი საშუალებაა. ისინი ქიმიურად რეაგირებენ სამოსის პიგმენტთან, შეცვლიან სტრუქტურას და იწვევს ფერის შეცვლას;
ოპტიკური ბლოკატორები: ისინი არიან ნივთიერებები, რომლებიც იწოვენ ულტრაიისფერ გამოსხივებას ან ულტრაიისფერ სინათლეს და, ამის შემდეგ მალევე გამოყოფენ ლურჯ ფლუორესცენტულ შუქს, ნიღბავს, მაგალითად, მოყვითალო ფერის ტანსაცმელს;
სუნამოები: ეს არის ესენციები, რომლებიც გამოიყენება სარეცხი პროცესის შემდეგ ტანსაცმელზე სასიამოვნო სუნის დასატოვებლად. აღსანიშნავია, რომ სუნამოები ესენციაა (ისინი ეთერის ფუნქციას განეკუთვნებიან);
საღებავები: ნივთიერებები, რომლებიც გამოიყენება პროდუქტის გასაფერადებლად;
სეკრეტორული და ქელეტირების საშუალებები: EDTA (ეთილენედიამინის ტეტრაცეტის მჟავა) არის სეკვესტრის მაგალითი. ისინი ურთიერთქმედებენ კალციუმის, მაგნიუმის და რკინის იონებთან, რომლებიც ძირითადად მყარ წყალშია, და არ იძლევა რაიმე მოქმედების კომპონენტის ურთიერთქმედებას, მაგალითად, ზედაპირულად აქტიურ ნივთიერებას.
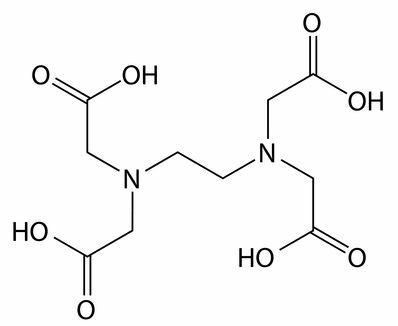
EDTA სეკვესტრის სტრუქტურული ფორმულა
ჩემ მიერ. დიოგო ლოპეს დიასი
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/quimica-sabao-po.htm
