“ქიმიური ბმა ”- ეს იყო ტერმინი, რომელიც პირველად გამოიყენა გილბერტ ნიუტონ ლუისმა 1920 წელს სტატიაში, თუ რატომ რატომ რომ ატომები ერთმანეთთან იკვრებიან და ქმნიან ნივთიერებებს და ასევე რატომ იკვრება ისინი ათასობითზე მეტი წლის.
აქამდე ცნობილი და პერიოდულ ცხრილში ჩამოთვლილი ქიმიური ელემენტების უმეტესობის ატომები ბუნებაში არ ჩანს იზოლირებული ფორმით. ჩვენს ყოველდღიურ ცხოვრებაში არსებული მასალების უმეტესობა არის ნივთიერებები, რომლებიც შეიძლება იყოს მარტივი (შედგება ატომებისაგან) მხოლოდ ერთი ტიპის ქიმიური ელემენტის) ან კომპოზიტებისა (აქვთ ორი ან მეტი ქიმიური ელემენტის ატომები ბევრი განსხვავებული).
ეს იმიტომ ხდება, რომ ატომებს აქვთ ქიმიური კავშირების შექმნის უნარი სხვა ატომებთან, რომლებიც შეიძლება იყოს იგივე ელემენტი ან სხვადასხვა ელემენტები. ეს კავშირები იმდენად ძლიერია, რომ ყოველგვარი გარეგანი ზემოქმედების გარეშე, უმეტეს შემთხვევაში ატომები დარჩებიან შეერთებულ მდგომარეობაში.
გონების რუკა: ქიმიური ობლიგაციები

* გონებრივი რუქის PDF გადმოსაწერად, Დააკლიკე აქ!
მაგალითად, ხშირია ბუნებაში თავისუფალი ჟანგბადის ატომის პოვნა; ამასთან, ჩვენ ვხვდებით რამდენიმე ნივთიერებას, რომელშიც ის სხვა ატომებთან არის დაკავშირებული. მარტივი ნივთიერების მაგალითია ჟანგბადის გაზი, რომელშიც თითოეული მოლეკულა შედგება ორი შეკრული ჟანგბადის ატომისგან (O
2); ხოლო კომპოზიციური ნივთიერების მაგალითია წყალი, სადაც თითოეულ მოლეკულას აქვს ორი წყალბადის ატომი, რომლებიც დაკავშირებულია ჟანგბადის ატომთან (H2ო)ერთადერთი ელემენტები, რომლებიც ბუნებაში სტაბილურად იზოლირებულია, არის კეთილშობილი გაზები, ეს არის პერიოდული სისტემის მე –18 ოჯახის ელემენტები (ის, ნე, არ, კრ, ქს და რნ). ყველა ამ ელემენტს საერთო აქვს ის ფაქტი, რომ მათ აქვთ უკანასკნელი ელექტრონული გარსი (ვალენტური ფენა) რვა ელექტრონი, გარდა ჰელიუმის (ის), რომელსაც აქვს მხოლოდ ერთი ელექტრონული გარსი (K ფენა) და, შესაბამისად, ფლობს ორ ელექტრონს, რაც არის ელექტრონების მაქსიმალური რაოდენობა ფენა.
ამრიგად, გილბერტ ნ. ლუისი და ასევე მეცნიერი უოტერ კოსელი მივიდნენ იმ დასკვნამდე, რომ დანარჩენი ელემენტების ატომებს სავალდებულოა ჰქონდეთ რვა ელექტრონი (ან ორი, თუ მხოლოდ K გარსი გაქვთ) და ამით სტაბილიზაციას ახდენენ. იგი შეიქმნა, მაშინ ვალენტობის ელექტრონული თეორია, რაც მიუთითებს რამდენ ქიმიურ ბმას ქმნის ელემენტის ატომი, ახსნილი იდეის საფუძველზე.
ამიტომ, ატომები ქმნიან ქიმიურ კავშირებს, ცდილობენ დაკარგონ, მოიპოვონ ან გაიზიარონ ვალენტური გარსის ელექტრონები, სანამ არ მიაღწევენ შემდეგ კეთილშობილ გაზს.ამ თეორიას ასევე მოუწოდა ოქტეტების წესი.
მაგალითად, ჟანგბადი ორვალენტიანია, რადგან მას აქვს ექვსი ელექტრონი ვალენტურ გარსში. ამიტომ, მას კიდევ ორი ელექტრონის მიღება სჭირდება, რომ ჰქონდეს კეთილშობილი გაზის ნეონის (Ne) კონფიგურაცია, ანუ ვალენტური გარსის რვა ელექტრონი, რაც ამ შემთხვევაში L გარსია. ჟანგბადის გაზისა და წყლის შემთხვევაში, ჩვენ გვაქვს შემდეგი:
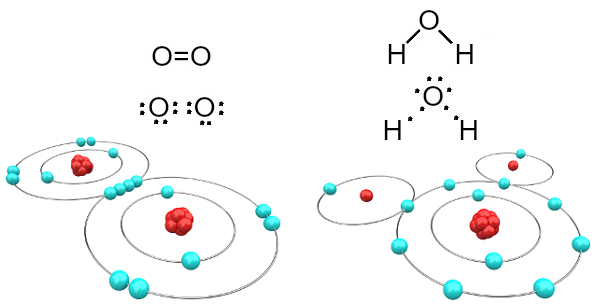
ჟანგბადის და წყლის მოლეკულები, რომლებიც წარმოიქმნება კოვალენტური ბმებით
გაითვალისწინეთ, რომ პირველ შემთხვევაში (ჟანგბადის გაზი - O2), ჟანგბადის თითოეულ ატომს აქვს ორი ელექტრონი, რომელთაგან ორივეს რვა ელექტრონი აქვს ვალენტობის გარსში. ეს ნიშნავს, რომ ა ორმაგი ბმა (ორი კავშირი ერთდროულად ორ ატომს შორის).
წყლის შემთხვევაში, წყალბადის ორი ატომიდან თითოეულს ელექტრონი აქვს ჟანგბადის ცენტრალურ ატომთან და ყველა სტაბილურია (ჟანგბადს აქვს ვალენტის რვა ელექტრონი და თითოეულ წყალბადს აქვს ორი ელექტრონები). აქ ასევე გაკეთებულია ორი მარტივი კავშირი.
ამ ტიპის ქიმიური ბმა, რომელშიც ყველა ატომს უნდა მიიღოს ელექტრონი (წყალბადის, არალითონებისა და ნახევრად მეტალების) და რომელშიც ელექტრონები წყვილებად არის განაწილებული, ე.წ. კოვალენტური ბმა.
მაგრამ არსებობს კიდევ ორი სახის ქიმიური ბმა:
(1) იონური ბმა → ხდება ელექტრონების საბოლოო გადატანა ერთი ატომიდან მეორეზე. ამ ტიპის კავშირი გვხვდება ლითონის ატომებს შორის (რომლებსაც აქვთ ელექტრონების დაკარგვის ტენდენცია სტაბილური) და წყალბადის ატომები, არამეტალები და ნახევრად მეტალები (რომლებსაც აქვთ ელექტრონების დარჩენის ტენდენცია სტაბილური).
მაგალითად არის ნატრიუმის ქლორიდი (NaCl - სუფრის მარილი), სადაც ნატრიუმი არის ლითონი, რომელსაც აქვს ელექტრონის დაკარგვის ტენდენცია, ხოლო ქლორი არის არამეტალი, რომელსაც აქვს ელექტრონის მიღების ტენდენცია. ამრიგად, ნატრიუმი აბარებს(წითელი ისარი)ელექტრონი ქლორისგან, ქმნის მარილს, ძალიან სტაბილურ ნივთიერებას. რადგან ამთავრებენ (შავი ისარი) იონები, რომლებიც ქიმიური სახეობებია, საწინააღმდეგო მუხტებით (+ და -), ერთი იონი იზიდავს მეორეს ახლომახლო და იონური მტევანი იონების უზარმაზარი რაოდენობით იქმნება, ისევე როგორც კრისტალები სუფრის მარილში.

ნატრიუმის ქლორიდის ფორმირება იონური კავშირით
(2) ლითონის კავშირი → ეს არის თეორია, რომ ლითონები (როგორიცაა ალუმინის, ოქრო, ვერცხლი, სპილენძი და ა.შ.) წარმოიქმნება ნეიტრონის ატომების გროვით და კატიონები, რომლებიც ერთად იმართება თავისუფალი ელექტრონების ერთგვარი "ღრუბელი" (ელექტრონები, რომლებიც დაიკარგა კათიონების წარმოქმნისას ციტირებულია). ელექტრონების ეს ღრუბელი (ან ზღვა) იმოქმედებს, როგორც მეტალიკი, რომელიც ატომებს ერთმანეთთან იკავებს.
ამ ტიპის ქიმიური ობლიგაციების, აგრეთვე ოქტეტის წესის შესახებ მეტი ინფორმაციისთვის წაიკითხეთ ქვემოთ მოცემული სტატიები.
გონების რუკა მ. ვიქტორ რიკარდო ფერერერას მიერ
ქიმიის მასწავლებელი
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-ligacao-quimica.htm

