このテキストでは、 のチャート 体調の変化 に 純粋な物質、このタイプの図の解釈方法と混合物のグラフの表現方法。
これを行うために、水の例を考えてみましょう。 -10ºCの温度で氷を1杯取り、1気圧の圧力で加熱プロセスを開始するとします。 温度が-10ºCから-9ºC、-8ºCなどに上昇すると、氷は0ºCの温度に達するまで固体状態のままになります。
その時点で、それは液体状態に移行し始めます、すなわち、融合が起こり始めます。 温度は以前のように上昇し続けることはありませんが、すべての氷が溶けるまで0°Cで一定に保たれます。

すべての固体を溶かした後、システムの温度は100°Cの温度に達するまで上昇し続けます。 この温度で、液体状態にあった水は蒸気状態に変化し始めます。つまり、沸騰します。
それが起こったのと同じように 融点、沸点では、すべての液体が蒸気になるまで温度も一定に保たれます。 その後、システムを加熱し続けると、温度は上昇し続けます。
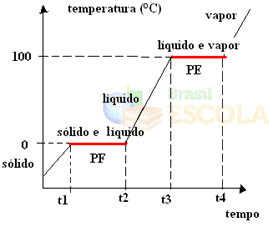
準備ができました! これは、水の物理的状態またはその加熱曲線の変化を表すグラフまたは図です。 逆のプロセスの場合、次の水冷却曲線が得られます。
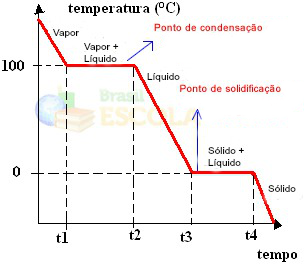
これらのグラフの非常に重要な側面は、2つのレベルで形成されていることです。つまり、温度がしばらく一定に保たれる2つのポイントがあります。 これは常に純粋な物質の状態変化で発生します。 唯一の違いは、融点と沸点の値です。
今やめないで... 広告の後にもっとあります;)
たとえば、酸素は水とは異なり、液体ではなく、室温(約20ºC)の気体です。 これは、海面での融点が-223.0°C、沸点が-183.0°Cであるためです。 物理的な状態変化チャートを参照してください。

一般的なミックスグラフィック
混合物を加熱または冷却している場合、融点と沸点は 決定された定数値、つまり、グラフで観察された2つのレベルは形成されません 上記。
物理的状態の変化は、一定量ではなく温度範囲で発生します。 たとえば、融点は特定の温度で始まり、別の温度で終わります。次のグラフに示すように、沸点についても同じことが起こります。
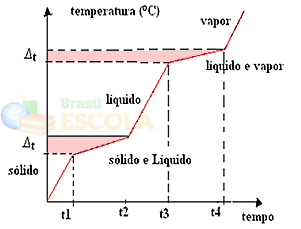
2つの例外は、共晶混合物と共沸混合物です。 それらに何が起こるかを見てください:
a)共晶混合物
共晶混合物は、溶融中は純粋な物質であるかのように動作します。つまり、この時点では、凝集状態の変化の開始から終了まで温度は一定に保たれます。

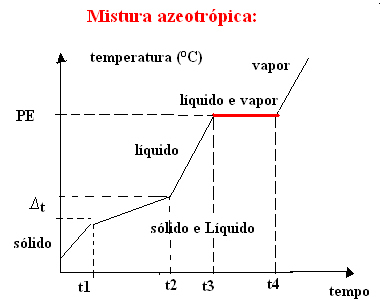
b)共沸混合物
共沸混合物は、沸騰中は純粋な物質のように振る舞います。つまり、この時点で、温度は凝集状態の変化の最初から最後まで一定に保たれます。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "物理的状態の変化のチャート"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm. 2021年6月28日にアクセス。