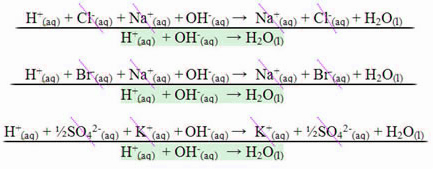いくつか 化学反応 私たちの日常生活では、次の形でエネルギーの喪失と獲得が起こります 熱、結合の形成と破壊はエネルギーと物質の相互作用を伴うため。 反応に加えて、これはまた発生します 物理的状態の変化.
発熱過程
の一般的な反応 燃焼 木の燃焼です。 このプロセスは、光だけでなく熱の形でエネルギーを放出することで発生することが知られています。 したがって、この反応はと呼ばれます 発熱 (接頭辞「exo」は「外部」を意味します)、熱が放出されると。
1 発熱過程 これは反応ではなく、むしろ凝集状態の変化であり、雪の形成です。 液体の水は固化し、熱が放出されると雪を形成します。 このプロセスでは、より具体的には、7.3kJの熱が放出されます。
これらの中で 発熱過程、のバリエーション エンタルピー (ΔH)、つまり、放出される熱量は常に負(ΔH<0)になります。これは、 エンタルピー変動 試薬のエンタルピーによって生成物のエンタルピーを減少させることによって測定されます:
ΔH= H製品-H試薬
今やめないで... 広告の後にもっとあります;)
または
ΔH= H最後の-H初期
エネルギーが放出されたため、製品のエンタルピーは低くなり、したがって、エンタルピーの変動は負になります。 発熱反応および現象の他の例を以下に示します。

吸熱プロセス
熱を吸収する反応または物理的状態の変化は、 吸熱プロセス. の例 吸熱反応 (接頭辞「endo」は「内部」を意味します)は、エネルギーが必要な食品の調理です。 一方、吸熱反応である物理的状態の変化は、液体の水の蒸発であり、これが発生するためには、44kJを吸収する必要があります。
この場合、生成物のエンタルピーまたは最終状態が増加すると、エネルギーが吸収されるため、エンタルピーの変動は常に正になります(ΔH> 0)。 吸熱プロセスの他の例に注意してください。

要するに:
我ら 発熱過程、 システムは熱を失い、環境は加熱されます。
我ら 吸熱プロセス、 システムは熱を獲得し、環境は冷えます。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "吸熱および発熱プロセス"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/processos-endotermicos-exotermicos.htm. 2021年6月27日にアクセス。
化学

ボイルの法則によると、地獄はどのようになりますか、地獄は吸熱または発熱のプロセスです 吸熱および発熱、熱吸収、熱放出、圧力積、一定温度、 ボイルの法則。