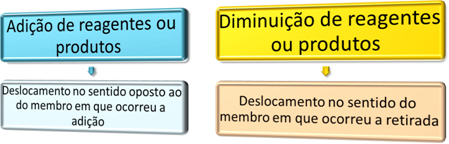
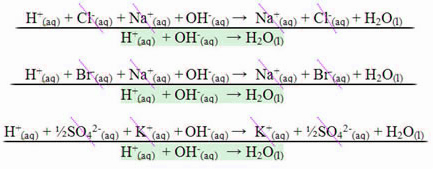ルシャトリエの原理:平衡状態にあるシステムに力が加えられると、その力の影響を減らすために、システムはそれ自体を再調整する傾向があります。
酸性度と塩基性度の変化は、化学物質のバランスに対する外力として機能します。 次に、システムはこの力の影響を軽減するために移動する必要があります。 システムのバランス、集中力を変えることができる要因の例を見てみましょう。
2 CrO2-4(aq) + 2 H+(ここに) ↔CrO2-7(ここに)+ H2O (1)
このバランスにレモン(酸性溶液)を数滴加えると、それは右または左に移動し、製品の1つの形成に有利に働きます。
これは、このアクションによって、方程式のメンバーの1つに含まれるH +イオンの量が増えるためです。 これが左側の反応物で発生した場合、バランスは右側にシフトしてバランスを取ります。
システムに塩基性NaOH溶液を加えると、反応を逆転させることができます。 OH-イオンの存在はH +イオンを消費し、バランスは左にシフトします。
結論:イオン濃度(CrO2-7)が優勢で、バランスが左にシフトします。 イオン濃度(CrO 2-4)が優先され、バランスが右にシフトします。
今やめないで... 広告の後にもっとあります;)
リリア・アルベス
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "ルシャトリエの原理"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/principio-le-chatelier.htm. 2021年6月28日にアクセス。