תגובות להפחתת חמצון המתרחשות בנוכחות מי חמצן (תמיסה מימית של מי חמצן - H2או2 (aq)) מהווים מקרה מיוחד שיש לנתח אותו בנפרד, בעיקר באשר ליתרתו. הסיבה לכך היא שהחמצנים במי חמצן, שיש להם Nox השווה ל- -1, יכולים להתחמצן או להפחית.
לדוגמה, בואו נסתכל על שני מקרים בהם הוא מתנהג תחילה כחומר מחמצן (צמצום) ואז כסוכן צמצום (חמצון):
- חומר מחמצן: בכל פעם שמופחת מי חמצן, הפועל כחומר מחמצן, הוא מייצר מים כמוצר.
אם נוסיף תמיסת מי חמצן לתמיסה המכילה יוני יודיד (I-) במדיום חומצי, יהיה לנו:
ה2או2 (aq) + אני-(פה) + H+(פה) → H2או(1) + אני2 (ים)
ראו שנוצרים מים ויוד. אך כדי לבדוק אם מימן החמצן אכן פעל כסוכן חמצון והופחת, צפו בקביעת מספרי החמצון (NOx): *

חמצן חמצן של מי חמצן ירד מ -1 ל -2, בהתחשב בכך שהוא קיבל אלקטרון אחד. עם זאת, מכיוון שיש לנו שני חמצנים בכל מולקולת מי חמצן (H2או2), וריאציית ה- Nox תהיה שווה ל -2.
אז, כפי שמוצג בטקסט "איזון חיזור", צעד הכרחי לאיזון התגובות בשיטת הפחתת החמצון הוא להפוך את ערכי הווריאציות של ה- Nox לפי המקדמים, בהיותם, במקרה זה, כדלקמן:
* ח2או2 = 2 (∆ Nox) = 2 → 2 יהיה המקדם של ה- I-;
* אני-= ∆ Nox = 1 → 1 יהיה המקדם של H2או2.
לפיכך, יש לנו:
1 שעה2או2 (aq) + 2 אני-(פה) + H+(פה) → H2או(1) + אני2 (ים)
להכות את המקדמים האחרים על ידי איזון לפי ניסויים:
- מכיוון שבחבר הראשון ישנם שני אטומי חמצן, מקדם המים בחבר השני חייב להיות שווה ל -2. ומכיוון שיש גם שני יונים של יוד בחבר הראשון, מקדם היוד בחבר השני יהיה 1. אל תשכח שעלינו להכפיל את המדד במקדם כדי למצוא את הכמות הנכונה של אטומים ויונים בכל חבר:
1 שעה2או2 (aq) + 2 אני-(פה) + H+(פה) → 2 ח2או(1) + 1 אני2 (ים)
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
- עכשיו נותר רק לאזן את קטיון המימן של החבר הראשון, והמקדם שלו יצטרך להיות שווה ל -2, משום שבחבר השני יש לו 4 מימנים ובחבר הראשון כבר יש לו שניים:
1 שעה2או2 (aq) + 2 אני-(פה) +2 ח+(פה) → 2 ח2או(1) + 1 אני2 (ים)
- סוכן צמצום: בכל פעם שמימן חמצן מתחמצן, משמש כסוכן הפחתה, הוא מייצר חמצן (O2) כמוצר.
דוגמה שבה מי חמצן מצטמצם היא כאשר הוא בא במגע עם אשלגן פרמנגנט (KMnO4). לחומר זה צבע סגול מאוד אופייני, אך כאשר הוא בא במגע עם מי חמצן הוא הופך לחסר צבע. הסיבה לכך היא שכל המנגן נמצא ביון MnO4- של פתרון permanganate מצטמצם, מה שמוליד את יון Mn2+, כפי שמוצג מטה:
+1 -1 +7 -2 +1 0 +2 +1 -2
ה2או2 + MnO4-+ H+ → ה2 + Mn2++ H2או
בחישוב ה- Nox אנו רואים שהחמצן במימן החמצן אכן מתחמצן וגורם להפחתת המנגן:
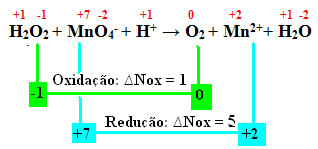
כמו בדוגמה הקודמת, ה- ∆ Nox של מי חמצן יהיה שווה ל- 2, שכן ישנם שני אוקסיגנים וכל אחד מאבד אלקטרון. לכן יש לנו:
* O2 = 2 (∆ Nox) = 2 → 2 יהיה המקדם של MnO4-;
* MnO4- = ∆ לא = 5 → 5 יהיה המקדם של ה- O2.
וכמו כל O2 מגיע ממי חמצן, שני החומרים מקבילים זהה:
5 ה2או2 + 2MnO4-+ H+ → 5 או2 + Mn2++ H2או
איזון בשיטת הניסוי, יש לנו:
5 שעות2או2 + 2 MnO4-+ 6 ח '+ → 5 O2 + 2 דקות2++ 8 ח2או
* לכל שאלה לגבי אופן חישוב מספר החמצון (Nox) של אטומים ויונים בתגובה, קרא את הטקסט "קביעת מספר החמצון (Nox)".
מאת ג'ניפר פוגאצה
בוגר כימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "תגובות להפחתת חמצון המערבות מי חמצן"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-envolvendo-agua-oxigenada.htm. גישה אליו ב -28 ביוני 2021.



