O זירקוניום, סמל Zr, מספר אטומי 40, הוא יסוד כימי השייך לקבוצה 5 של טבלה מחזורית. הוא בולט בעמידותו הרבה בפני קורוזיה, כמו גם ביציבות תרמית טובה.
האלמנט הוא מבחינה כימית מאוד דומה ל הפניום, ובגלל זה, לכל דגימת זירקוניום טבעי יש תכולת הפניום קטנה. הוא מצוי בשפע בקרום כדור הארץ, עם תכולה גבוהה בהרבה מזו של יסודות בשימוש נרחב כמו נחושת, אבץ ועופרת.
לזירקוניום יש יישום רחב בתעשייה הגרעינית, שכן ספיגת הנייטרונים הנמוכה שלו הופכת אותו לציפוי מצוין לדלק עשיר באורניום דו חמצני. בנוסף, מכיוון שהוא נחשב לא רעיל ומאוד תואם ביולוגי, נעשה שימוש בזירקוניום בתותבות כירורגיות ובשתלים.
קראו גם: אורניום - יסוד בעל חשיבות רבה לייצור אנרגיה
סיכום על זירקוניום
זירקוניום הוא א מַתֶכֶת שייך לקבוצה 5 של הטבלה המחזורית.
הוא תמיד מופיע בטבע עם תכולה קטנה של הפניום, מכיוון שהיסודות הללו דומים מאוד מבחינה כימית.
זירקוניט ובאדליייט הם עפרות הזירקוניום העיקריות.
ההפרדה בין זירקוניום להפניום קשה מאוד.
לזרקוניום יש קורוזיה טובה ועמידות בטמפרטורה גבוהה.
ניתן להשתמש בו בהשתלות שיניים ובתותבות אחרות, מכיוון שהוא אינו רעיל ובעל תאימות ביולוגית גבוהה.
חלק ניכר מהזירקוניום משמש את התעשייה הגרעינית.
היסוד התגלה בשנת 1789 על ידי המדען הגרמני מרטין קלפרוט.
תכונות זירקוניום
סֵמֶל: Zr.
מספר אטומי: 40.
מסה אטומית: 91.224 C.M.u.
אלקטרושליליות: 1,33.
נקודת היתוך: 1855 מעלות צלזיוס.
נקודת רתיחה: 4409 מעלות צלזיוס.
צְפִיפוּת: 6.52 גרם ס"מ-3 (ב-20 מעלות צלזיוס).
תצורה אלקטרונית: [Kr] 5s2 4ד2.
סדרת כימיה: קבוצה 4, מתכות מעבר.
תכונות של זירקוניום
זירקוניום, בצורתו המתכתית, הוא א מתכת אפרפרה ושיש לו עמידות טובה בפני קורוזיה, בעיקר בגלל שכבת ZrO2 שנוצר סביבו, מגן על המסה המתכתית הפנימית. עם זאת, אם מחולק דק, זירקוניום הוא פירופורי מאוד, כלומר, הוא יכול להתלקח באופן ספונטני במגע עם אוויר, במיוחד בטמפרטורות גבוהות.
מבחינה כימית, זירקוניום קרוב מאוד להפניום, לא מעט בגלל שהיסודות מתרחשים יחד בטבע. לכן, כמו הפניום, זירקוניום אינו סובל מהתקפות כימיות חומצות דָלִיל (חוץ מה"פ) אלא אם כן הם מחוממים. תמיסות אלקליות אינן יעילות במיוחד על זירקוניום, אפילו בטמפרטורות גבוהות יותר.
במערכות טמפרטורות גבוהות יותר, לזירקוניום יש את היכולת להגיב עם רובם לא מתכות. בעת התגובה, ניתן לראות כי תרכובות זירקוניום עם מספר חמצון +4 הן היציבות ביותר, כמו במקרה של ZrO2 או ZrCl4. מצבי חמצון נמוכים יותר, כגון +3, פחות יציבים, הבדל מ טִיטָן, האלמנט הקל ביותר בקבוצה 4, שיש לו יציבות טובה עם העומס הזה.
היכן ניתן למצוא זירקוניום?

בין היסודות בלוק d של הטבלה המחזורית, זירקוניום הוא הרביעי בשכיחותו, מאחורי בַּרזֶל, טיטניום ו מַנגָן. הם קיימים יותר מ 30 עפרות שיש ליומ זירקוניום בחוקתו. בין הידועים והחשובים ביותר הם זירקוניט (הידוע גם בשם זירקון), ZrSiO4, ו-baddeleyite (או baddeleite), ZrO2. Baddeleyite אפילו נמצא בברזיל.
המדינות עם עתודות הזירקוניום הגדולות ביותר הן אוסטרליה, דרום אפריקה ומוזמביק. עם זאת, היצרניות הגדולות ביותר הן סין, צרפת, הודו, רוסיה, גרמניה וארצות הברית.
מעניין, זירקוניום זה נמצא בשפע בחלקם כוכבים. האלמנט אפילו זוהה ב שמש ובמטאוריטים. דגימות ירח שהושגו באמצעות משימות אפולו הוכיחו תוכן גבוה של ZrO2 בסלעים אלה בהשוואה לסלעים יבשתיים.
ראה גם: זהב - מתכת אצילה הבולטת במוליכות החשמלית הטובה שלה
השגת זירקוניום
את הזירקוניום מתרחש באופן טבעי עם הפניום, תמיד עם תכולה של היסוד השני שמשתנה בין 1 ל-3% במסה. למרות התוכן הנמוך שלהם, ההפרדה בין השניים קשה מאוד.
בדרך כלל, תהליך קרול משמש למיצוי זירקוניום. בתהליך זה, ה-ZrO2 הכלול בעפרות הופך, בטמפרטורה גבוהה, ל-ZrCl4. בדרך זו ניתן להשיג זירקוניום באמצעות מגנזיום כמפחית. התגובות הבאות מדגימות את התהליך.
ZrO2 → ZrCl4 (באמצעות CCl4 בטמפרטורה של 770 K)
ZrCl4 → Zr (באמצעות Mg באווירת Ar בטמפרטורה של 1420 K)
עם זאת, הדמיון הכימי הגדול בין Zr ל-Hf אומר שהפניום נשאר במערכת הסופית כטומאה מתמשכת. לפיכך, יש צורך שימוש בטכניקות מתכות להפרדה בין Zr ל-Hf. התעשייה כבר מפתחת מסלולים הידרו-מטלורגיים (כלומר, המתרחשים בתמיסה מימית) ופירומטלורגית (ללא נוכחות של מים).
טכניקה הידרומטלורגית היא התגבשות חלקית של מלחי K2ZrF6 וק2HfF6, שאין להם אותה מסיסות במים. טכניקת פתרון נוספת היא מיצוי ממסים, לפיה תרכובות Zr ו-Hf מומסות. במים ולאחר מכן מופק באופן סלקטיבי עם ממיסים אורגניים כגון מתיל איזובוטיל קטון ו הוֹקָרָה. לאור קושי ההפרדה, זירקוניום מסחרי משווק בדרך כלל עם תכולה של 1 עד 3% במסה של Hf.
יישומי זירקוניום
הזירקוניום המתכתי הוא עובד ב ליגות, בעיקר בפלדה, כדי לשפר אותם מבחינת עמידות מכנית וקורוזיבית. גם יציבות המתכת בטמפרטורות גבוהות מאפשרת כך בשימוש בספינות חלל, אשר סובלים מנזק רב בגלל התנאים הקיצוניים בהם נתקלים במהלך הכניסה המחודשת לאטמוספירה של כדור הארץ.
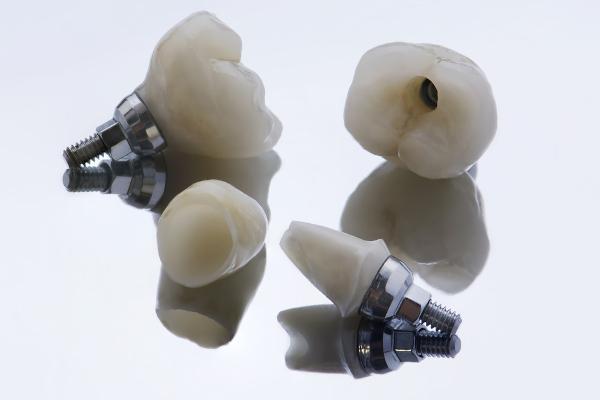
מכיוון שזירקוניום מוכר כיסוד לא רעיל ועמיד מאוד בפני קורוזיה, בנוסף להתאמה ביולוגית טובה, השימוש ביישומים כירורגיים נחקר גם, כמו בתותבות ושתלים דנטליים.
זירקוניום דו חמצני, ZrO2, בעל נקודת התכה גבוהה מאוד, בטווח של 2500 מעלות צלזיוס. לפיכך, הוא משמש ב ייצור מיכלים בעלי עמידות בחום גבוהה, בנוסף לקרמיקה עמידה במיוחד. קרמיקה זו אף נוצלה במכונות חיתוך מסיבה זו. ה-ZrO2 זה יכול לשמש גם במוצרי קוסמטיקה, אנטי-פרספירנטים, אריזות מזון ואפילו אבני חן מזויפות.
ראוי לציין שחלק ניכר מהזירקוניום משמש את ה תעשייה גרעינית. יש, למשל, ליגת Zircaloy®, סגסוגת מתכת של זירקוניום ופח שפותחה אך ורק למטרות גרעיניות.
בתעשייה הגרעינית, זירקוניום הוא משמש באריזה המכילהêm תחמוצת אורניום, דלק של תחנות כוח. בגלל שהוא עמיד מאוד למים ועם לכידה נמוכה של נויטרונים, מסתבר שזה חומר טוב למטרה זו. כדאי לזכור כי משתמשים בניוטרונים במהלך ביקוע, ולכן חיוני שזירקוניום לא ילכד אותם. אי-הלכידה גם גורמת לכך שהזירקוניום לא מופיע רדיואקטיבי. זו הסיבה שבמקרה זה לא יכולים להיות לזירקוניום עקבות של הפניום, מתכת בעלת יכולת מצוינת ללכוד נויטרונים.
בדוק את זה בפודקאסט שלנו:כיצד פועלות תחנות כוח גרעיניות?
היסטוריה של זירקוניום
השם זירקוניום נובע כנראה סרגון, מילה מהשפה הסורית המשמשת לתיאור הצבעים של אבני חן המוכרות כיום כזירקוניה. למרות שהמינרלים כבר היו ידועים, לא היה ידוע שהם מכילים יסוד חדש עד מרטין היירינץ' קלפרות', בשנת 1789, הצליח לזהות את היסוד בברלין. המדען הגרמני החליט לתת שם לאלמנט זירקהורן.
שנת 1789 הייתה חשובה מאוד עבור קלפרות', שכן באותה שנה גילה המדען את היסוד אורניום.
פתרו תרגילים על זירקוניום
שאלה 1
(FGV SP/2014 - מותאם) סוג חדש ומבטיח של חומרים מוליכים-על מבוסס על התרכובת ונדיום זירקוניום דיבוריד. תרכובת זו מסונתזת ממלח זירקוניום (IV).
(מגזין חפש Fאפספ, יוני 2013. מְעוּבָּד)
מספר הפרוטונים והאלקטרונים ביון Zr4+ שווה ל, בהתאמה:
א) 36; 40
ב) 40; 40
ג) 40; 44
ד) 40; 36
ה) 36; 36
תשובה
האות ד
כמו שיש לזירקוניום מספר אטומי שווה ל-40, אנו יכולים להסיק שמספרו של פרוטונים הוא גם 40, כי המספר האטומי שווה מספרית למספר הפרוטונים.
הצגת מטען השווה ל-+4, אנו יודעים שלזירקוניום בצורה זו יש ארבעה אלקטרונים אלא אם כן בצורתו הנייטרלית.
כאשר נייטרלי, מספר הפרוטונים שווה למספר האלקטרונים, כלומר, במקור לזירקוניום יש 40 פרוטונים ו-40 אלקטרונים. מאבד ארבעה אלקטרונים, לזירקוניום נשאר רק 36.
שאלה 2
(Uerj 2013 —מְעוּבָּד) זירקוניום דו חמצני דומה ליהלום, צורה אלוטרופית של פחמן, שניתן להחליף בתכשיטים בעלות נמוכה.
סמן את החלופה המכילה את הנוסחה הכימית של זירקוניום דו חמצני, וכן את סוג הקשר הבין-אטומי של חומר זה.
א) זרו4, קוולנטי.
ב) זרו2, יונית.
ג) זרו2, קוולנטי.
ד) זרו4, יונית.
ה) זרו2, מתכתי.
תשובה
אות ב'
זירקוניום דו חמצני, כשמו כן הוא, חייב להכיל רק שני אטומים של חַמצָן. לפיכך, הנוסחה הצפויה היא ZrO2. בנוסף, זירקוניום בדרך כלל מקבל מצב חמצון השווה ל-+4.
סוג הקשר הבין-אטומי הוא יונית, משתי סיבות:
זירקוניום הוא מתכת, וחמצן הוא לא מתכת;
ההבדל של אלקטרושליליות בין שניהם גדול מ-1.7 (3.5 - 1.3 = 2.2).
מאת סטפנו אראוחו נובאיס
מורה לכימיה
