הפונקציות האורגניות העיקריות הן: חומצות, בסיסים, מלחים ותחמוצות.
לתרכובות אורגניות תכונות שונות והן קיימות במצבים רבים בחיי היומיום שלנו. מסיבה זו נושא זה נדון רבות בבחינות הקבלה, באויב ובתחרויות.
כדי לעזור לך להתכונן לבחינות, יצרנו רשימה זו של 15 שאלות עם החלטות שהגישו הערות וגישות שונות לכל פונקציה אורגנית.
מושגים כלליים
1. (FGV) תרכובות מסוימות, כאשר מסולסלות במים, מייצרות תמיסה מימית המוליכה חשמל. מבין התרכובות שלהלן:
| אני. בְּ2רק4 |
| II. או2 |
| III. Ç12ה22או11 |
| IV. KNO3 |
| V. CH3COOH |
| ראה. NaCl |
הם יוצרים פתרון מימי המוליך חשמל:
א) רק אני, IV ו- VI
ב) רק אני, IV, V ו- VI
ג) הכל
ד) רק אני ו- VI
ה) רק ראה
חלופה נכונה: ב) רק אני, IV, V ו- VI.
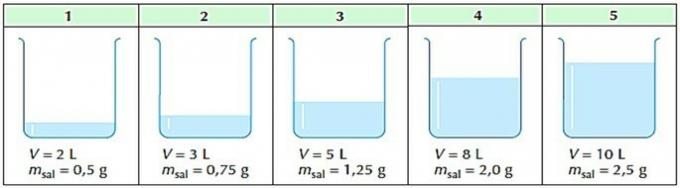
הולכת החשמל בתמיסה מתרחשת עקב היווצרותם של מינים טעונים חשמליים, היונים, כפי שמצא ארניוס בניסויים שלו.
כאשר יונים נוצרים בתמיסה, קטיונים (מטען חיובי) נודדים לקוטב והאניונים השליליים (מטען שלילי) נודדים לקוטב החיובי, סוגרים את המעגל החשמלי ומאפשרים מעבר של שַׁרשֶׁרֶת.
תרכובות המייצרות בתמיסה מינים ניטרליים אינן מוליכות חשמל.
על פי מידע זה עלינו:
אני. נהיגה
בתמיסה, המלח מתנתק ויונים נוצרים.
II. לא נוהג
חמצן דיאטומי בטמפרטורת החדר הוא מולקולה אינרטית.
III. לא נוהג
הנוסחה המוצגת היא לסוכרוז, תרכובת מולקולרית שכאשר היא באה במגע עם מים, המולקולות שלה מתפזרות, אך אינן מאבדות את זהותן.
IV. נהיגה
בתמיסה, המלח מתנתק ויונים נוצרים.
V. נהיגה
חומצה אצטית היא חומצה חלשה שיש לה חלק מיונן קטן בתמיסה.
ראה. נהיגה
בתמיסה, המלח מתנתק ויונים נוצרים.
2. (מקנזי- SP)
המשוואה לעיל מייצגת תגובה
א) של דיסוציאציה יונית.
ב) שיש בו חומצה כמגיב.
ג) של יינון מוחלט, ויוצר את קטיון ההידרוקסוניום.
ד) של יינון, הפקת אניון הפוספיד.
ה) אשר, ביינון מלא, מייצר אניון חד-פעמי.
חלופה נכונה: ג) של יינון מוחלט, ויוצר את הקטיון ההידרוקסוניום.
חומצה זרחתית היא תרכובת כימית המייננת במגע עם מים ומשחררת יוני H+.
יינון מתרחש בשלושה שלבים:
| צעד ראשון | |
| שלב שני | |
| צעד שלישי | |
| סכום הצעדים |
הקטיונים (ח+) המשוחררים מגיבים עם מים ויוצרים את היון ההידרוקסון (H3או+).
על פי הנמקה זו עלינו:
שגוי. ניתוק מתרחש בתרכובות יוניות וחומצה זרחתית היא תרכובת מולקולרית.
ב) לא נכון. חומצה זרחנית היא תלת חומצה מכיוון שיש בה שלושה מימנים מיוננים.
ג) נכון. קטיון ההידרוקסוניום, הנקרא גם הידרוניום, הוא מין שנוצר על ידי צומת מימן מיונן עם מים.
ד) שגוי. האניון המיוצר הוא פוספט (). נוסחת הפוספיד היא:
ה) לא נכון. האניון שנוצר () משולש כי יש לו 3 טעינות.
3. נקשר נכון את התרכובות שלהלן עם הפונקציות האורגניות שלהן.
| אני. HBr, H3אָבָק4 ו- H2שיתוף3 | () חומצות |
| II. שיתוף2, רק2 ואל2או3 | () בסיסים |
| III. אל2(אוה)3, KOH ו- NH4הו | () מלחים |
| IV. NaCℓ, KNO3 ו- BaSO4 | () תחמוצות |
חומצות הן תרכובות שיש בהן מימנים מיוננים.
(אני) חומצות: HBr, H3אָבָק4 ו- H2שיתוף3
בבסיסים יש יון הידרוקסיל.
(III) בסיסים: אל2(אוה)3, KOH ו- NH4הו
מלחים הם תרכובות יוניות הנוצרות על ידי קטיונים ואניונים.
(IVמלחים: NaCℓ, KNO3 ו- BaSO4
תחמוצות הן תרכובות הנוצרות על ידי צומת חמצן עם יסודות אחרים, למעט פלואור.
(II) תחמוצות: CO2, רק2 ואל2או3
חומצות
4. כתוב את שם החומצות הבאות:
א) HCl ו- HBr
חומצה הידרוכלורית וחומצה הידרו-ברומית.
התרכובות לעיל מייצגות הידרטים. לחומצות בכיתה זו נוסחה HאיקסA, כאשר x מייצג את מספר המימנים (H) ו- A תואם את המטלי הקשור.
המינוח של חומרים אלה נעשה באופן הבא:
| ה | קל | |
| חוּמצָה | כְּלוֹר | הידריק |
| חומצה הידרוכלורית |
| ה | br | |
| חוּמצָה | ברום | הידריק |
| חומצה הידרוברומית |
ב) HNO3 ו- HNO2
חומצה חנקתית וחומצה חנקתית.
התרכובות הנ"ל מייצגות חומצות חמצן בעלות שני מספרים של חמצון. לחומצות בכיתה זו נוסחה HאיקסAO, נוצר על ידי מימן, לא מתכתי וחמצן.
המינוח של חומרים אלה נעשה באופן הבא:
| ה | נ | או3 |
| חוּמצָה | ניטר | אני |
| חומצה חנקתית. המקסימום של חנקן במתחם זה הוא +5. |
תרכובת ה- Nox הנמוכה ביותר היא חומצה חנקתית: HNO2.
| ה | נ | או2 |
| חוּמצָה | ניטר | עֶצֶם |
| חומצה חנקתית. המקסימום של חנקן במתחם זה הוא +3. |
ג) HClO, HClO2, HClO3 ו- HClO4
חומצות היפוכלור, כלור, כלור ופרוכלור.
התרכובות לעיל מייצגות חומצות חמצן בעלות ארבעה מספרים של חמצון. לחומצות בכיתה זו נוסחה HאיקסAO, נוצר על ידי מימן, חמצן ולא מתכת ממשפחת 7A.
המינוח של חומרים אלה נעשה באופן הבא:
| Nox +1 | חוּמצָה | היפופוטם | קידומת אלמנט | עֶצֶם |
| Nox +3 | חוּמצָה | - | קידומת אלמנט | עֶצֶם |
| Nox +5 | חוּמצָה | - | קידומת אלמנט | אני |
| Nox +7 | חוּמצָה | לְכָל | קידומת אלמנט | אני |
התרכובות שניתנו בחלופה נקראות כך:
| ה | קל | או | |
| חוּמצָה | היפופוטם | כְּלוֹר | עֶצֶם |
| חומצה היפוכלורית. המקסימום של כלור בתרכובת זו הוא +1. |
| ה | קל | או2 |
| חוּמצָה | כְּלוֹר | עֶצֶם |
| חומצת כלור. המקסימום של כלור בתרכובת זו הוא +3. |
| ה | קל | או3 |
| חוּמצָה | כְּלוֹר | אני |
| חומצה כלורית. המקסימום של כלור בתרכובת זו הוא +5. |
| ה | קל | או4 | |
| חוּמצָה | לְכָל | כְּלוֹר | אני |
| חומצה פרוכלורית. המקסימום של כלור בתרכובת זו הוא +7. |
5. (UVA-CE) חומצות HClO4, ח2MnO4, ח3אָבָק3, ח4יום שבת2או7, לגבי מספר המימנים המיוננים, ניתן לסווג ל:
א) חד-חומצה, חומצה, טרי-חומצה, חומצה-חמוצה.
ב) חד-חומצה, חומצה, טריאציד, טריאציד.
ג) חד-חומצה, חומצה, חומצה, חמצן.
ד) חד-חומצה, חד-חומצית, חומצה, טרי-חומצה.
חלופה נכונה: ג) חד-חומצה, חומצה, חומצה, חמצן.
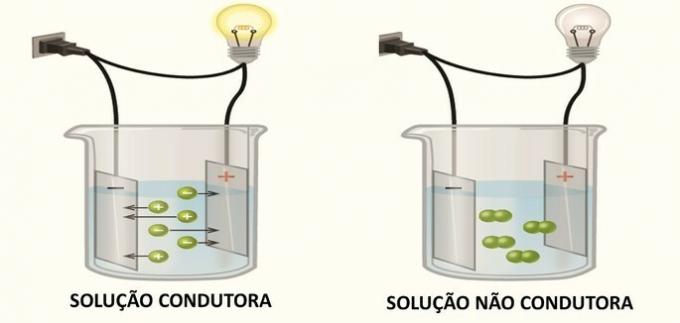
יינון החומצות המוצגות מתרחש באופן הבא:
נוסחאות מבניות מראות לנו כי מימנים מיוננים קשורים לחמצן.
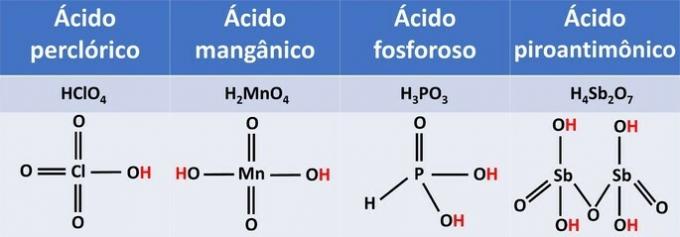
לפי כמות המימנים המיוננים, ניתן לסווג חומצות ל:
| HClO4 | מימן מיונן | חד-חומצה |
| ה2MnO4 | שני מימנים מיוננים | סוכרת |
| ה3אָבָק3 | שני מימנים מיוננים | סוכרת |
| ה4יום שבת2או7 | ארבעה מימנים מיוננים | טטרציד |
עבור חומצות אוקסי, מימנים מיוננים הם אלה המחוברים ישירות לחמצן. לחומצה זרחנית יש אחד משלושת המימנים המחוברים לאלמנט המרכזי, זרחן, ולכן הוא חומצה.
6. (UESPI) תן לחומצות להיות רשומות למטה, עם דרגות היינון בהתאמה שלהן באחוזים (α%):
|
HClO4 (α% = 97%) |
ה2רק4 (α% = 61%) |
ה3BO3 (α% = 0,025%) |
ה3אָבָק4 (α% = 27%) |
HNO3 (α% = 92%) |
בדוק את ההצהרה הנכונה:
א) ח3אָבָק4 חזק מ- H2רק4.
ב) HNO3 זו חומצה קלה.
ג) HClO4 הוא חלש יותר מ- HNO3.
ד) ה3אָבָק4 זו חומצה חזקה.
ה) ה3BO3 זו חומצה חלשה.
חלופה נכונה: ה) ח3BO3 זו חומצה חלשה.
הערך של תואם את מידת היינון ומחושב על ידי:
ככל שהערך גבוה יותר של , ככל שהחומצה חזקה יותר מכיוון שמשמעותה שיותר מינים מיוננים שוחררו לתמיסה.
על פי הנמקה זו עלינו:
שגוי. ככל שהערך גבוה יותר של , החומצה חזקה יותר. ה- H2רק4 בעל דרגת יינון גבוהה יותר מ- H3אָבָק4.
ב) לא נכון. ה- HNO3 יש לו מידת יינון הגדולה מ 90%. זו חומצה חזקה.
ג) לא נכון.4 בעל רמת יינון גבוהה יותר מאשר HNO3 להיות, אם כן, חזק ממנו.
ד) שגוי. ה- H3אָבָק4 זוהי חומצה בינונית, שכן יש לה מידת יינון בין 5% ל -50%.
ה) נכון. ה- H3BO3 יש לו מידת יינון פחות מ 5% ולכן הוא חומצה חלשה.
בסיסים
7. הקלד את שם הבסיסים הבאים:
א) LiOH ו- Be (OH)2
ליתיום הידרוקסיד ובריליום הידרוקסיד.
לבסיסים המוצגים יש תשלום קבוע ולכן המינוח מתבצע כדלקמן:
LiOH: ליתיום הידרוקסיד.
להיות (אוה)2: בריליום הידרוקסיד.
ב) CuOH ו- Cu (OH)2
הידרוקסיד גביעי והידרוקסיד כופרי.
לנחושת שני מספרים של חמצון: +1 ו- +2. אחת הדרכים לקרוא לבסיס nox משתנה היא כדלקמן:
| Nox +1 | CuOH | הידרוקסיד כוס |
| Nox +2 | Cu (OH)2 | הידרוקסיד קופרי |
ג) Sn (OH)2 ו- Sn (OH)4
פח (II) הידרוקסיד ופח (IV) הידרוקסיד.
לפח שני מספרים של חמצון: +2 ו- +4. המינוח של בסיס נוקס משתנה יכול להיעשות גם באופן הבא:
| Nox +2 | Sn (OH)2 | פח הידרוקסיד II |
| Nox +4 | Sn (OH)4 | פח הידרוקסיד IV |
8. (Fiam-SP) כדי להילחם בחומציות הקיבה הנגרמת על ידי עודף חומצה הידרוכלורית, נהוג לבלוע נוגד חומצה. מבין החומרים הבאים, הנמצאים בחיי היומיום של האנשים, המתאימים ביותר למאבק בחומציות הם:
סודה.
ב) מיץ תפוזים.
ג) מים עם לימון.
ד) חומץ.
ה) חלב מגנזיה.
חלופה נכונה: ה) חלב מגנזיה.
נוגדי חומצה הם חומרים המשמשים להעלאת ה- pH של הקיבה, מכיוון שעודף החומצה הידרוכלורית גורם לירידה ב- pH וכתוצאה מכך לעלייה בחומציות.
כדי להילחם בחומציות הקיבה, מומלץ לבלוע א חומר בעל אופי בסיסי, מכיוון שכאשר מגיבים עם חומצת קיבה, היא תייצר תגובה מנטרלת, ויוצרת מלח ומים.
על פי הנמקה זו עלינו:
שגוי. לא ניתן להשתמש בסודה מכיוון שהיא מכילה חומצה פחמנית בהרכבה.
ב) לא נכון. לא ניתן להשתמש בתפוז, מכיוון שהוא מכיל חומצת לימון בהרכבו.
ג) לא נכון. לא ניתן להשתמש בלימון, מכיוון שהוא מכיל חומצת לימון בהרכבו.
ד) שגוי. לא ניתן להשתמש בחומץ מכיוון שהוא מכיל חומצה אצטית בהרכבו.
ה) נכון. יש להשתמש בחלב מגנזיה מכיוון שהוא מכיל בסיס מגנזיום הידרוקסיד בהרכבו.
תגובת הנטרול שנוצרה היא:
9. (Osec) בסיס חזק חייב להיות קשור לקבוצת OH-:
א) יסוד חשמלי מאוד.
ב) אלמנט מאוד אלקטרוני.
ג) חצי מתכת.
ד) מתכת הנותנת 3 אלקטרונים.
ה) שאינו מתכת.
חלופה נכונה: א) אלמנט מאוד-חיובי.
בסיס חזק הוא בסיס שיש לו רמה גבוהה של דיסוציאציה, כלומר יוני הידרוקסיל חופשיים בתמיסה.
ליון ההידרוקסיל יש מטען שלילי, מכיוון שהוא מצליח למשוך את האלקטרון לעברו כאשר הוא מתנתק בגלל האלקטרוני שלילי של חמצן.
לפיכך, לאלמנט מאוד-חיובי יכולת לאבד אלקטרונים ולמסור אותם להידרוקסיל, כשהוא נשאר בצורה קטיונית בתמיסה.
א) נכון. יסודות חשמליים מאוד כמו מתכות אלקליות ומתכות אדמה אלקליין יוצרים בסיסים חזקים.
ב) לא נכון. אלמנט אלקטרוני יותר שלילי מאשר חמצן יביא לתחרות על האלקטרון.
ג) לא נכון. לחצי-מתכת יש אלקטרונגטיביות רבה.
ד) שגוי. ליון ההידרוקסיל יש מטען 1. מתכת שנותנת 3 אלקטרונים תיצור בסיס עם 3 הידרוקסילים.
דוגמא:
ה) לא נכון. הבסיסים החזקים ביותר הם בסיסים שנוצרו עם מתכות.
מלחים
10. כתוב את שם המלחים הבאים:
א-נ-א2שיתוף3
נתרן פחמתי.
זהו סוג של מלח ניטרלי ומינוחו ניתן כדלקמן:
| אניון | קטיון |
| בְּ+ | |
| פַּחמָה | נתרן |
| נתרן פחמתי |
ב) KNaSO4
נתרן ואשלגן גופרתי.
זהו סוג של מלח כפול והמינוח שלו זהה למלח הניטראלי, ושמות שני הקטיונים נכתבים.
| אניון | קטיונים | |
| ק+ | בְּ+ | |
| סולפט | אֶשׁלָגָן | נתרן |
| נתרן ואשלגן גופרתי |
ג) NaHCO3
נתרן חד מימן פחמתי.
זהו סוג של מלח חומצי והמונח שלו ניתן כדלקמן:
| מספר מימנים | אניון | קטיון |
| 1 | בְּ+ | |
| מונו | פַּחמָה | נתרן |
| נתרן חד מימן פחמתי |
השם הפופולרי לתרכובת זו הוא נתרן ביקרבונט.
ד) אל (אוה)2קל
אלומיניום דיהידרוקסי כלוריד.
זהו סוג של מלח בסיסי ומינוחו ניתן כדלקמן:
| מספר הידרוקסילים | אניון | קטיון |
| 2 | קל- | אל3+ |
| די | כלוריד | אֲלוּמִינְיוּם |
| אלומיניום דיהידרוקסי כלוריד |
תרכובת זו ידועה גם בשם אלומיניום כלורי כללי.
ה) CuSO4. 5 שעות2או
נחושת גופרית פנטהידראט.
זהו סוג של מלח מיובש ומינוחו ניתן כדלקמן:
| אניון | קטיון | מספר מולקולות מים |
| תַחַת2+ | 5 | |
| סולפט | נְחוֹשֶׁת | פנטה |
| נחושת גופרית פנטהידראט |
11. (Unirio) מלחים הם גם מוצרים המתקבלים על ידי תגובה של ניטרול מוחלט או חלקי של מימנים מיוננים של חומצות עם בסיסים או הידרוקסידים, על פי התגובה הגנרית:
חומצה + בסיס מלח + מים
על סמך הצהרה זו, מהי החומצה היחידה שאין בה את כל המוצרים האפשריים שלה?
א) חומצה הידרוכלורית מייצרת רק את מלח הכלוריד הנייטרלי.
ב) חנקן מייצר רק את המלח ניטראלי ניטראט.
ג) זרחן מייצר רק את מלח הפוספט הנייטרלי.
ד) גופרתי יכול לייצר מלח גופריתי ניטרלי או מלח חומצה, חומצה גופרית או מימן גופרתי.
ה) גופרית יכולה לייצר מלח גופרית ניטרלי או מלח חומצה, חומצה גופרתית או מימן גופרתי.
חלופה לא נכונה: ג) זרחן מייצר רק את המלח הפוספט הנייטרלי.
א) נכון. בחומצה הידרוכלורית יש רק מימן מיונן אחד, אשר יגיב ליצירת מים. המלח ייווצר אז על ידי האניון של החומצה, במקרה זה הכלוריד, וקטיון הבסיס.
דוגמאות:
ב) נכון. לחומצה החנקתית יש רק מימן מיונן אחד, שיגיב ליצירת מים. המלח ייווצר אז על ידי האניון של החומצה, במקרה זה החנקתי, וקטיון הבסיס.
דוגמאות:
ג) לא נכון. לחומצה הזרחנית שלושה מימנים מיוננים, ולכן היא יכולה לעבור יינון חלקי או מוחלט. במקרה זה, ניתן ליצור שלושה סוגים של מלחים:
- ניטרול מוחלט המייצר א מלח ניטרלי:
- ניטרול חלקי המייצר א מלח חומצה:
- ניטרול חלקי המייצר א מלח בסיסי:
ד) נכון. בנטרול מוחלט נוצר מלח ניטרלי ובנטרול חלקי ניתן ליצור מלח חומצי.
- ניטרול מוחלט:
- ניטרול חלקי:
ה) נכון. בנטרול מוחלט נוצר מלח ניטרלי ובנטרול חלקי ניתן ליצור מלח חומצי.
- ניטרול מוחלט:
- ניטרול חלקי:
| אני. בְּ2ב4או7.10 שעות2או | ה. מלח בסיסי |
| II. מג (OH) Cl | ב. מלח כפול |
| III. נאקסו4 | Ç. מלח חומצה |
| IV. NaHCO3 | ד. מלח מיובש |
הקשר הנכון ביניהם הוא:
א) AI, BIII, CIV, DII
ב) AII, BIV, CIII, DI
ג) AI, BII, CIII, DIV
ד) AII, BIII, CIV, DI
חלופה נכונה: ד) AII, BIII, CIV, DI
| AII. מלח בסיסי: מג (OH) Cl | יש לו הידרוקסיל במבנה שלו. |
| BIII. מלח כפול: NaKSO4 | במבנהו שני קטיונים מתכתיים. |
| CIV. מלח חומצי: NaHCO3 | יש לו מימן במבנה שלו. |
| DI. מלח מיובש: נא2ב4או7.10 שעות2או | במבנה שלה יש מולקולות מים. |
תחמוצות
13. כתוב את שם התחמוצות הבאות:
פְּלָדָה2 ולא2או3
פחמן דו-חמצני ודיאטרוגן דו-חנקני.
תחמוצות אלו הן תחמוצות מולקולריות, מכיוון שחמצן נקשר לא-מתכות. המינוח לשיעור זה נעשה באופן הבא:
| מספר החמצן | מספר פחמנים |
| 2 | 1 |
| חד פחמן דו חמצני או פחמן דו חמצני |
| מספר החמצן | מספר חנקן |
| 3 | 2 |
| דו תחמוצת דיטרוגן |
ב) אל2או3 והמשיך2או
תחמוצת אלומיניום ותחמוצת נתרן.
תחמוצות אלו הינן תחמוצות יוניות, שכן חמצן קשור למתכות. למתכות הקשורות לחמצן יש מטען קבוע. לכן, המינוח לשיעור זה נעשה באופן הבא:
אל2או3: תחמוצת אלומיניום
בְּ2O: תחמוצת נתרן
ב) קו2O ו- CuO
תחמוצת נחושת I ותחמוצת נחושת II.
תחמוצות אלו הן תחמוצות יוניות מכיוון שחמצן נקשר למתכת. למתכת הקשורה לחמצן יש מטען משתנה. אחת הדרכים למנות מחלקה זו היא כדלקמן:
| Nox +1 | תַחַת2או | תחמוצת נחושת I |
| Nox +2 | CuO | תחמוצת נחושת II |
ג) FeO ו- Fe2או3
תחמוצת ברזל ותחמוצת ברזל.
תחמוצות אלו הן תחמוצות יוניות מכיוון שחמצן נקשר למתכת. למתכת הקשורה לחמצן יש מטען משתנה. המינוח של תחמוצת נוקס משתנה יכול להיעשות גם באופן הבא:
| Nox +2 | FeO | תחמוצת ברזל |
| Nox +3 | אֱמוּנָה2או3 | תחמוצת ברזל |
14. (UEMA) אטומים ניטרליים של יסוד מייצג מסוים M כוללים שני אלקטרונים בקליפת הערכיות שלהם. הנוסחאות הנכונות לתחמצן ולברומיד הרגילים שלך הן, בהתאמה:
(נתונים: O = 6A ו- Br = 7A.)
א) מ2O ו- MBr
ב) מו2 ו- MBr2
ג) MO ו- MBr2
ד) מ2או2 ב2br
ב2O ו- MBr2
חלופה נכונה: ג) MO ו- MBr2
לאלמנטים M שני אלקטרונים במעטפת הערכיות. כדי להתקשר עם אלמנטים אחרים הוא יכול לאבד את שני האלקטרונים הללו וליצור את הקטיון M.2+.
חמצן שייך למשפחת 6A וזקוק ל -2 אלקטרונים נוספים כדי לרכוש יציבות עם תצורה אלקטרונית של גז אצילי, כאמור על ידי כלל האוקטט.
כמו כן, ברום, שהוא ממשפחת 7A, זקוק רק לאלקטרון אחד כדי שיהיו לו 8 אלקטרונים במעטפת הערכיות.
על פי מידע זה עלינו:
שגוי. ליצירת תרכובת M2O ו- MBr, אלמנט M אמור ליצור את הקטיון M+.
ב) לא נכון. לחמצן יש מטען 2- ולא 1- כפי שהוא מיוצג בעת יצירת תרכובת MO2.
ג) נכון. על פי הערכיות של היונים החלופה נכונה.
ד) שגוי. לברומיד מטען 1- ולא 2- כפי שמוצג בעת יצירת תרכובת M2בר.
ה) לא נכון. לקטיון האלמנט יש מטען של 2+ ולא מטען של 1+ כפי שמוצג בעת יצירת התרכובת M.2או
15. (PUC-MG) צפה בתגובות הכימיות שלהלן:
| אני. MgO + H2או |
| II. שיתוף2 + H2או |
| III. ק2O + 2HCl |
| IV. רק3 + 2 לא אה |
ההצהרה השגויה היא:
א) בתגובות II ו- IV יש תחמוצות חומצה או אנהידרידים.
ב) התגובות I ו- III כוללות תחמוצות בסיסיות.
ג) המלח המיוצר בתגובה IV נקרא נתרן סולפט.
ד) המלח המיוצר בתגובה III נקרא אשלגן כלורי.
ה) האופי הבסיסי של תחמוצות מודגש כאשר חמצן נקשר ליסודות אלקטרוניים יותר.
חלופה לא נכונה: ה) האופי הבסיסי של תחמוצות מודגש ככל שחמצן נקשר ליסודות אלקטרוניים יותר.
א) נכון. כאשר תחמוצות חומציות כמו פחמן דו חמצני וטריו-חמצני גופרית מגיבות עם מים, הן יוצרות חומצה בתמיסה.
ב) נכון. בתגובה עם מים, תחמוצות בסיסיות כגון תחמוצת מגנזיום ותחמוצת אשלגן מהוות בסיס בתמיסה.
ג) נכון. בְּ2רק4 היא הנוסחה לנתרן סולפט.
ד) נכון. KCl הוא הנוסחה לאשלגן כלורי.
ה) לא נכון. האופי הבסיסי של התחמוצות מודגש ככל שחמצן נקשר ליותר יסודות. אלקטרופוזיטיבי, כמתכות אלקליין אלקליין ואדמה, מכיוון שכאשר הם מגיבים עם מים הם מייצרים בסיסים חזקים וכאשר הם מגיבים עם חומצות הם יוצרים מלח ומים.