בתוך הטקסט איזומרים במולקולות עם פחמנים אסימטריים שונים הוצגו שתי נוסחאות שהוצעו על ידי Van't Hoff ו- Le Bel המסייעות בקביעת כמות האיזומרים האופטיים כאשר למולקולה יש שניים או יותר פחמנים אסימטריים.
אך כאשר למולקולה יש כמה פחמנים אסימטריים שווים לא ניתן להשתמש בנוסחאות אלה. אנו קובעים אם מולקולה היא כזו אם יש בה שני פחמנים או יותר שהליגנדים שלהם שונים זה מזה, אך זהים לחלוטין ליגנדים של פחמן (ים) אחר.
לדוגמא, חומצה טרטרית היא חומר שנוצר בתהליך של תסיסת מיץ ענבים לצורך ייצור יין. למולקולה שלך שני פחמנים אסימטריים שווים, שלשניהם הליגנדים הבאים:
│
HOOC─, ח─HO─ ו- H─C─OH
│
COOH
בתחזיות שלהלן יש לנו שתי אפשרויות: בראשונה הליגנדים של OH נמצאים בצדדים מנוגדים (וגם הליגנדים H); בשנייה, הליגנדים האלה נמצאים באותו צד ובכל אחת מהאפשרויות יש לנו תמונות מראה בהתאמה:

מכיוון ששני הפחמנים הא-סימטריים שווים, זווית α הסטייה ממישור האור המקוטב תהיה זהה. לכן, במקרה הראשון יש לנו את זה, מכיוון שהקונפורמציה של אטומי הפחמן שונה, אחד יעביר את מישור האור מקוטב ימינה (יד ימין) בזווית + α, והשני יעביר את מישור האור המקוטב שמאלה (levorotator) ב זווית –α. זה אומר ש
האחד יבטל את ההשפעה של השני ו החומר יהיה לא פעיל אופטית על ידי פיצוי פנימי, נקרא מתחם מזו.באפשרות השנייה המוצגת לעיל, לשני הפחמנים יש אותה קונפורמציה, כך ששני מקרים של תרכובות פעילות אופטיות:
1) שני הפחמנים הא-סימטריים מעבירים את מישור האור המקוטב ימינה (מפריד): + 2α;
2) שני הפחמנים הא-סימטריים מעבירים את מישור האור המקוטב שמאלה (מוטור מוטור): -2α.
חומצה טרטרית יכולה גם ליצור א תערובת גזענית שיש בו 50% מהאיזומר הקשור לטרור-רוטורציה ו -50% מהאיזומר הלב-מוטורי. איזומר אחד יבטל את הסטייה של מישור האור המקוטב של השני, לכן, תערובת זו נחשבת לא פעיל אופטית על ידי פיצוי חיצוני.
עם זה, אנו מגיעים למסקנה שלמולקולה שיש לה שני אטומי פחמן אסימטריים שווים יש שני איזומרים אופטיים. פעיל (דקסטרוגירוס ולבוגירוס) ושני איזומרים לא פעילים אופטית (תרכובת המסו והתערובת הגזעית), כפי שמוצג בסיכום לִגעוֹת:
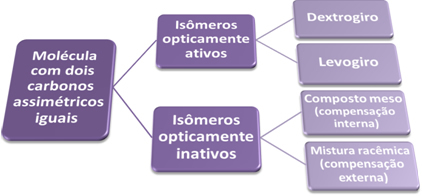
לאיזומרים השונים הללו יש אותה נוסחה מולקולרית, אולם תכונותיהם שונות, ראה:
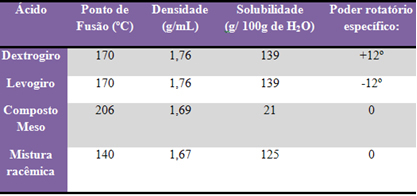
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/molecula-com-carbonos-assimetricos-iguais.htm

