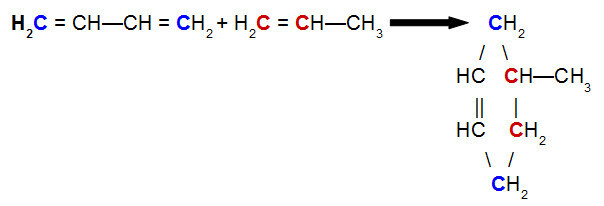ניתוח התכונות הפיזיקליות והכימיות של תרכובות המבצעות קשרים קוולנטיים (על ידי שיתוף אלקטרונים) מראה לנו שיש הבדלים גדולים בין חומרים אלה. אך לפני שנבחן את המאפיינים הללו עצמם, בואו נראה מה ההבדל בין חומרים מולקולריים לקוולנטיים.
בְּ חומרים מולקולריים הם אלה שנוצרים כאשר אטומים מקושרים באמצעות קשרים קוולנטיים, מה שמוליד מולקולות של מספר נקבע.
עם זאת, הקשר הקוולנטי יכול להיווצר גם תרכובות במבנה רשת בעל מספר גדול מאוד ובלתי מוגדר של אטומים, שהם מקרומולקולות. חומרים כאלה נקראים תרכובות קוולנטיות אוֹ מוצקי רשת קוולנטיים. כמה דוגמאות לתרכובות אלה הן: יהלום (C), גרפיט (C), סיליקון דו חמצני (SiO2) וסיליקון קרביד (SiC).
עכשיו, בואו נסתכל על המאפיינים העיקריים שלו:
- מצב גופני בטמפרטורת החדר: בתנאי סביבה, תרכובות מולקולריות וקוולנטיות נמצאות בשלושת המצבים הפיזיים (מוצק, נוזלי וגז).
דוגמאות:
או מוצק: סוכר (סוכרוז), סיליקה (חול), יהלום, גרפיט;
או נוזל: מים, אצטון, אתנול;
או גזי: מימן גופרתי, גז כלור, גז ברום, גז מימן.

- נקודת התכה ורתיחה: באופן כללי, נקודות ההיתוך והרתיחה של חומרים אלה הם קטנים יותר מאלו של חומרים יוניים.
לחומרים קוולנטיים יש טמפרטורות רתיחה גבוהות יותר מאלו המולקולריות, תמיד מעל 1000 מעלות צלזיוס. הסיבה לכך היא שככל שהמולקולות שלהם מחוברות יותר, ויוצרות סריג גבישי, יש צורך לספק יותר אנרגיה כדי לגרום להם לשנות את מצבן.
שני גורמים מפריעים לנקודות הרתיחה וההיתוך של תרכובות קוולנטיות ומולקולריות: א מסה מולארית וה כוח בין מולקולרי.
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
ככל שהמסה הטוחנת גדולה יותר, כך האינרציה של המולקולה גדולה יותר וכתוצאה מכך נקודת הרתיחה וההיתוך גבוהים יותר. אם ההמונים הטוחניים מקורבים, אנו מסתכלים על הכוחות הבין מולקולריים. הכוח הבין-מולקולרי האינטנסיבי ביותר הוא של קשירת מימן, מה שמוביל לנקודת רתיחה והיתוך גבוהה יותר. הביניים הם הדיפול הקבוע והחלש ביותר, המוביל לנקודת רתיחה והתכה נמוכה יותר, הוא הדיפול המושרה.
- זרם חשמלי: בצורתם הטהורה, הן הנוזלים והן המוצקים אינם מוליכים זרם חשמלי.
יוצא מן הכלל הוא גרפיט, המוליך זרם חשמלי בצורה מוצקה, מכיוון שאלקטרוני הקשר הכפול שלו מהדהדים ולכן הם בעלי ניידות מסוימת.
- מְסִיסוּת: קוטבים מתמוססים לקוטבים ולא קוטביים מתמוססים לקוטביים.
- עַקשָׁנוּת: העמידות של חומרים קוולנטיים בפני פגיעה או זעזועים מכניים נמוכה. באופן כללי, הם מוצקים שבירים, כפי שמוצג במקרה של זכוכית, שנוצרת על ידי נתרן וסידן סיליקט.

- קשיחות: באופן כללי, יש להם קשיות גבוהה. למעט גרפיט, מכיוון שאטומי הפחמן שלו קשורים לשלושה אטומי פחמן אחרים, ויוצרים לוחות משושים עם ניידות מסוימת, מה שהופך אותו לרך. בגלל זה, הוא משמש אפילו כחומר סיכה.
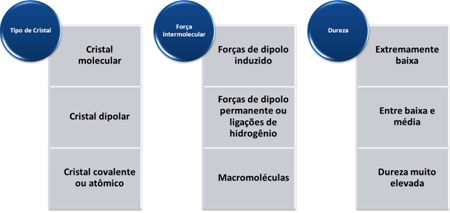
קשיותם של חומרים אלה משתנה בהתאם לסוג הגביש, כפי שמוצג בטבלה שלהלן:
מאת ג'ניפר פוגאצה
בוגר כימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "תכונות של תרכובות קוולנטיות ומולקולריות"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm. גישה אליו ב -28 ביוני 2021.
תרכובות יוניות, מאפיינים עיקריים של תרכובות יוניות, קשר בין יונים, העברה סופית של אלקטרונים, כוחות משיכה אלקטרוסטטיים בין יונים, יונים שליליים וחיוביים, אניונים, קטיונים, קשר יוני, מבנה מולקולרי הוא