Nella pulizia della casa, in diverse situazioni, è possibile utilizzare l'aceto per eliminare i cattivi odori. Ma finisce con tutti i tipi di odori sgradevoli? In quali situazioni può essere utilizzato?
Per capire come l'aceto elimina i cattivi odori, dobbiamo prima capire cosa costituisce questi odori. Gli odori che ci provocano una sensazione sgradevole sono composti da molecole che ne hanno diverse funzioni organiche. Vedi alcuni esempi:
* acidi carbossilici: hanno da 1 a 3 atomi di carbonio e hanno un odore da forte a irritante; gli acidi da 4 a 10 atomi di carbonio hanno un odore estremamente sgradevole, con odori rancidi e pungenti. Alcuni esempi sono:

* composti di zolfo o tiocomposti: Diversi composti contenenti zolfo sono "puzzolenti". Di solito sono derivati da gas di idrogeno solforato, H2S, responsabile dell'odore di uova marce.
Molti composti solforati, soprattutto del gruppo tiolico, detti anche mercaptani, vengono aggiunti al gas di cottura cooking perché hanno un odore estremamente sgradevole e possono essere facilmente rilevati dal consumatore anche a basse concentrazioni. Questo avviso riduce il rischio di incidenti. Generalmente, tra i tioli utilizzati ci sono etantiolo, butan-1-tiolo e 1,1-dimetiletanotiolo di seguito riportati:
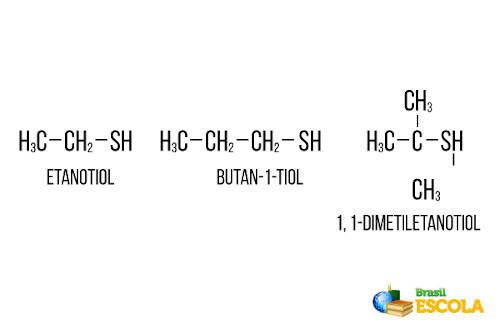
Oltre a questi abbiamo anche il metantiolo (CH3 ─ S ─ H), che è considerato il compost con uno dei peggiori odori al mondo.
* Composti aromatici azotati:
Per darvi un'idea, il scatolo (C9H9N) è un'ammina aromatica responsabile dell'odore delle feci.
Le ammine sono presenti anche negli odori sgradevoli perché molte di esse sono prodotte nella decomposizione degli esseri viventi. L'odore sgradevole caratteristico del pesce marcio, ad esempio, è dovuto alla trimetilammina e anche alla piridina (ammina aromatica):
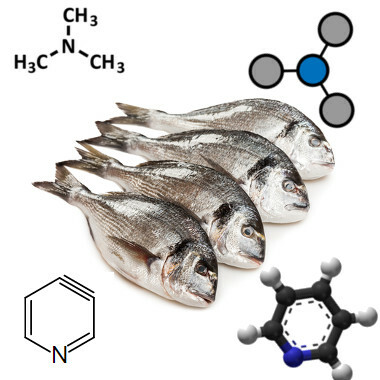
La trimetilammina e la piridina sono responsabili dell'odore del pesce marcio
Ora parliamo di aceto. Consiste in una soluzione acquosa di circa il 4% in volume di Acido acetico. Questo composto organico, chiamato anche acido etanoico, appartiene alla famiglia degli acidi carbossilici e la sua struttura è mostrata di seguito:

Formula di struttura dell'acido etanoico o acetico
Affinché l'aceto elimini i cattivi odori, è necessario che a reazione di neutralizzazione, in cui vengono prodotte sostanze che non hanno il cattivo odore. dal momento che tutto reazione di neutralizzazione avviene tra un acido e una base, l'aceto, che è un acido, elimina efficacemente solo gli odori basici.
I composti azotati citati sono alcalini, cioè hanno un carattere basico (pH > 7). Secondo la teoria acido-base di Lewis, una base è una qualsiasi specie chimica in grado di offrire una coppia di elettroni. Ma secondo la teoria di Bronsted-Lowry, base è ogni specie chimica in grado di ricevere un protone (H+).
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Pertanto, i composti azotati, come le ammine aromatiche, fungono da basi perché l'azoto ha una coppia di elettroni che può fornire ad un'altra specie chimica oppure può ricevere un protone (H+).
L'aceto può quindi essere utilizzato per eliminare l'odore di pesce, poiché si verifica la seguente reazione tra acido acetico e piridina:
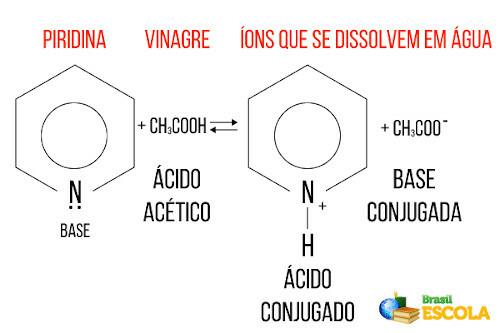
Si noti che la piridina fungeva da base, poiché riceveva un protone dall'acido acetico dall'aceto, formava ioni che aumentavano la sua solubilità in acqua ed eliminava l'odore di pesce marcio.
Quindi, nella vita di tutti i giorni, puoi lavarsi le mani con aceto e poi con acqua per finire il odore di pesce che resta nelle mani. Questo può essere fatto anche per terminare il odore di grasso fetido e con quello odore rancido e sapore di pollo.
Anche l'aceto agisce in modo simile per sbarazzarsi del odore di muffa sui vestiti. Puoi immergere i vestiti in una ciotola di acqua e aceto.
Un'altra applicazione dell'aceto consiste nell'eliminare il odore di urina e feci di cani e gatti. Dopo aver rimosso questi residui, puoi pulire la zona con un panno imbevuto di una soluzione composta da 2/3 di acqua tiepida e 1/3 di aceto. Infine, applica una parte del prodotto puro sulla zona e lascia asciugare naturalmente.
Ma secondo le reazioni viste, l'aceto non è efficace nell'eliminare, ad esempio, l'odore di sudore (bromidrosi), poiché, come detto, questo odore sgradevole è dovuto agli acidi carbossilici.
Il sudore è secreto dalle nostre ghiandole eccrine ed apocrine, costituite essenzialmente da acqua (99%), cloruro di sodio, acidi carbossilici a bassa massa molare, urea, sali di ferro, potassio, ammonio, acido lattico, proteine e altri componenti.
Viene poi eliminato dalle ghiandole sudoripare, inizialmente senza alcun odore sgradevole. Tuttavia, nella nostra pelle, ci sono batteri che metabolizzano le sostanze del sudore e ne producono alcune composti maleodoranti come acido butirrico, acido caproico e altri associati ad ammine e mercaptani.
Quindi, per eliminare l'odore delle ascelle, è più consigliabile utilizzare una sostanza di base come il latte di magnesia (soluzione di idrossido di magnesio, Mg(OH)2), che renderà basico l'ambiente, provocando la morte dei batteri e, di conseguenza, la decomposizione delle sostanze organiche eliminate con il sudore. La maggior parte dei deodoranti funziona anche perché hanno un componente attivo che inibisce la crescita dei batteri, come il triclosan.
di Jennifer Fogaça
Laureato in Chimica


