dissociazione di basi è un processo fisico che si verifica con questo importante gruppo di sostanze inorganiche quando vengono disciolte in acqua, o quando passano attraverso il processo di fusione (passaggio dallo stato solido allo stato liquido attraverso riscaldamento).
In generale, il fenomeno di dissociazione di base è il rilascio dei cationi e degli anioni che formano il composto ionico, che, in questo caso, è la base. Quindi, durante il dissociazione di base, il rilascio di ioni che già esistono nel composto, cioè non si formano nuovi ioni.
La base è formata da un qualsiasi metallo (X), che è il catione del composto, o dal catione ammonio (gruppo NH4+), legato all'anione idrossido (rappresentato dal gruppo OH), come nelle rappresentazioni seguenti:
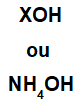
Rappresentazioni generali di una formula base
la forma di rappresentare il dissociazione di base si fa attraverso un'equazione in cui, nel reagente, abbiamo la base e, nei prodotti, abbiamo gli ioni (cationi e anioni). Ciò che fa la differenza è come avviene la dissociazione:
Dissoluzione della base in acqua:
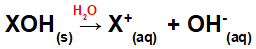
Equazione che rappresenta la dissociazione di una base in un mezzo acquoso
Dissociazione per fusione di base:
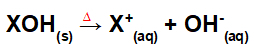
Equazione che rappresenta la dissociazione di una base mediante il processo di fusione
Analizzando le equazioni generali di cui sopra, verifichiamo che in tutte avremo sempre la base, il catione (che è il metallo o gruppo NH4+) e l'anione (OH-). Ma sono tutti così? Non c'è differenza tra loro? Per la prima domanda la risposta è no e per la seconda domanda la risposta è sì.
Quando eseguiamo il dissociazione da una base, è fondamentale prima analizzare la formula base, perché da essa si può determinare il carico del of catione e la quantità in moli di anioni idrossido, poiché la quantità in moli di catione è standard (sempre 1 moli).
Vale la pena ricordare che la quantità di gruppi OH presenti nella formula base determina la carica del catione e la quantità in moli dell'anione idrossido nella dissociazione della base.
Diamo un'occhiata agli esempi di idrossido di alluminio [Al(OH)3] e idrossido d'oro (AuOH). Nella formula della base di alluminio, ci sono tre gruppi OH e nella formula della base dell'oro, solo un gruppo OH. Quindi, nella dissociazione di queste basi, abbiamo:
Al(OH) dissociazioneOH3:
Poiché questa base ha tre gruppi OH nella formula, la carica sul catione sarà +3 e la quantità in moli di anioni è pari a 3 moli, come possiamo vedere nella seguente equazione:
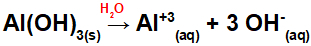
Equazione di dissociazione della base di alluminio in mezzo acquoso
Dissociazione da AuOH:
Poiché questa base ha un gruppo OH nella formula, la carica sul catione sarà +1 e la quantità in moli di anioni è pari a 1 mol, come possiamo vedere nella seguente equazione:
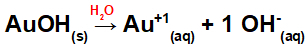
Equazione della dissociazione delle basi con l'oro in mezzo acquoso
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm
