l'elemento chimico fosforo (P) appartiene al terzo periodo della tavola periodica e alla famiglia dell'azoto (VA). Per questo motivo i suoi atomi normalmente formano tre legami chimici per raggiungere il teoria dell'ottetto (stabilità). Tuttavia, ci sono alcune situazioni in cui un atomo di fosforo fa più di tre legami, un fatto che è possibile solo attraverso il fenomeno di ibridazione.
Per capire il ibridazione del fosforo, dobbiamo prima capire perché l'atomo di questo elemento fa tre legami. Per fare ciò, dobbiamo solo monitorare la tua distribuzione elettronica:

Distribuzione elettronica del fosforo
Possiamo osservare che, nello strato di valenza, l'atomo di fosforo ha il sottolivello 3s completo (con due elettroni) e il sottolivello 3p incompleto (ciascuno dei tre orbitali di sottolivello p ha a elettrone). Di seguito abbiamo la distribuzione degli elettroni negli orbitali dei sottolivelli del Strato di valenza del fosforo:
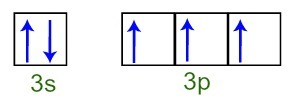
Rappresentazione degli elettroni del guscio di valenza dell'atomo di fosforo
Poiché ciascuno degli orbitali di sottolivello 3p è incompleto, l'atomo di fosforo è in grado di creare tre legami chimici, ottenendo così stabilità.
Ora, quando guardiamo alla sostanza PCl5, ad esempio, siamo certi che, in questa molecola, il fosforo abbia subito ibridazione, in quanto ha realizzato cinque connessioni. Poiché il cloro, che appartiene alla famiglia VIIA, ha bisogno di un legame per essere stabile e la molecola ha cinque atomi di questo elemento, ciascuno di essi deve formare un legame, il che fa sì che l'atomo di fosforo, a sua volta, debba fare anche cinque Connessioni. Questo evento è possibile solo attraverso il ibridazione (unione di orbitali atomici incompleti) del fosforo.
Quando riceve energia dall'ambiente esterno, gli elettroni dell'atomo di fosforo si eccitano. Subito dopo, uno dei due elettroni appartenenti al sottolivello 3s si sposta su un orbitale vuoto presente nel sottolivello d, che fino ad allora non ha elettroni. Vedi lo schema qui sotto:
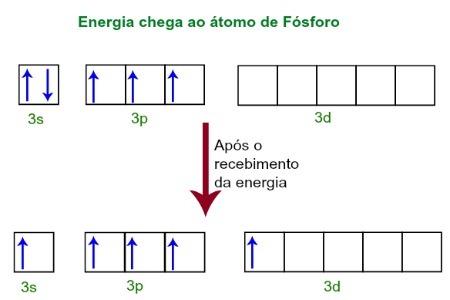
Dopo aver ricevuto energia, gli elettroni del fosforo vengono eccitati e uno occupa un orbitale del sottolivello d.
In questo momento, abbiamo nello strato di valenza del fosforo un orbitale s, tre orbitali p e un orbitale d incompleto.Alla fine, questi cinque orbitali si ibridano, cioè si fondono, risultando in cinque orbitali atomici incompleti, che ora sono in grado di creare cinque legami chimici.

Ibridazione di orbitali atomici incompleti del fosforo
Poiché un orbitale s, tre orbitali p e un orbitale d sono stati uniti, l'ibridazione del fosforo è del tipo sp3d.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm
