Al funzione dell'ossigeno sono un gruppo di composti organici che hanno atomi di ossigeno attaccati alla catena di carbonio. Sono loro:
alcool;
chetone;
aldeide;
acido carbossilico;
estere;
etere.
Leggi anche:Idrocarburi: composti formati da carbonio e idrogeno
Riassunto sulla funzione dell'ossigeno
Le funzioni dell'ossigeno sono un gruppo di composti che contengono un atomo di ossigeno. ossigeno attaccato direttamente alla catena di carbonio.
Le diverse funzioni dell'ossigeno sono caratterizzate da una specifica disposizione strutturale di atomi, detto gruppo funzionale.
I gruppi funzionali sono responsabili delle proprietà di ciascuna funzione organica.
Le funzioni dell'ossigeno sono: alcool, chetone, aldeide, acido carbossilico, estere ed etere.
Video lezione sulla funzione dell'ossigeno
Quali sono le funzioni dell'ossigeno?
Le funzioni corporee ossigenate sono quelle che avere un atomo di ossigeno legato a un atomo di ossigeno carbonio della catena di carbonio.
Le funzioni dell'ossigeno sono:
alcool;
chetone;
aldeide;
acido carbossilico;
estere;
etere.
Le funzioni organiche sono identificati dal loro gruppo funzionale, che è una disposizione strutturale di atomi o legami, responsabile delle proprietà caratteristiche di quell'insieme di composti.
Importanza delle funzioni dell'ossigeno
La presenza di funzioni dell'ossigeno nei composti organici è in grado di modificare le proprietà dei composti, rispetto al rispettivo idrocarburo, con un numero uguale di atomi di carbonio.
Le funzioni dell'ossigeno sono caratterizzate dalla presenza di gruppi idrossilici, carbonilici o carbossilici. UN la presenza dell'atomo di ossigeno aumenta il carattere polare composti, rendendoli più idrofili, cioè aumentando la loro affinità per acqua.
Presenza di funzioni dell'ossigeno è anche responsabile del tipo di forza intermolecolareagendo tra le molecole. La natura e l'intensità delle forze intermolecolari influenzano il solubilità e le temperature di fusione e di ebollizione.
La tabella sottostante mette a confronto alcune proprietà di tre composti che hanno lo stesso numero di atomi di carbonio, ma differiscono per la presenza di gruppi funzionali ossigenati.
Composto organico | |||
Butano (c4H10) |
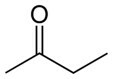
butanone (c4H8O) |
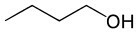
Butanolo (C4H10O) |
|
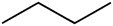 |
 |
 |
|
funzione organica |
Idrocarburo |
chetone (funzione dell'ossigeno) |
Alcol (funzione dell'ossigeno) |
Polarità |
apolare |
Polare |
Polare |
temperatura di fusione |
-138,3°C |
-86°C |
-89°C |
temperatura di ebollizione |
-0,5°C |
80°C |
118°C |
Forza intermolecolare predominante |
Dipolo indotto |
dipolo permanente |
legami di idrogeno |
Alcol
La funzione organica dell'alcool ha un gruppo idrossile (-OH) legato direttamente al carbonio saturo, cioè quell'atomo di carbonio che stabilisce solo legami singoli.
Gruppo funzionale degli alcoli: R-OH (idrossile).
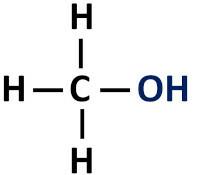
gli alcoli lo sono classificati in base al tipo di carbonio a cui è legato l'ossidrile. Gli alcoli primari hanno l'idrossile attaccato al carbonio primario. Gli alcoli secondari hanno il gruppo idrossile attaccato a un carbonio secondario e gli alcoli terziari hanno il loro gruppo -OH attaccato a carboni terziari.
Un composto organico che ha un solo ossidrile è chiamato monoalcol. Se ha due gruppi idrossilici, si chiama dialcool. Inoltre, le molecole sono chiamate polialcoli.
UN nomenclatura degli alcoli segue la raccomandazione di Iupac (International Union of Pure and Applied Chemistry), considerando l'assemblaggio del nome delle strutture chimiche in tre parti:
Prefisso - relativo al numero di atomi di carbonio.
Infix - si riferisce al tipo di legame chimico stabilito tra gli atomi di carbonio.
Suffisso - relativo al gruppo funzionale. Nel caso degli alcoli, il suffisso utilizzato è -Ciao.
Vedi esempi:
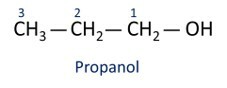
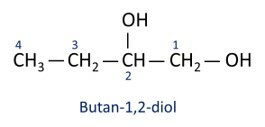
O l'alcol principale è etanol (CH3CH2OH), utilizzato come combustibile, nelle bevande alcoliche, come solvente chimico, detergente e disinfettante.
chetone
La funzione chetonica organica corrisponde a gruppo funzionale carbonilico (C=O), situato tra due atomi di carbonio della catena di carbonio.
Gruppo funzionale dei chetoni: R1–(C=O)–R2.

I chetoni lo sono classificati in base al numero di gruppi carbonilici:
Monochetoni: hanno un solo gruppo carbonilico.
Dichetoni: hanno due gruppi carbonilici.
Politoni: hanno più di due gruppi carbonilici.
UN nomenclatura dei chetoni segue le regole Iupac, ma con una differenza nell'ortografia del suffisso. I chetoni sono identificati dal suffisso -ona.
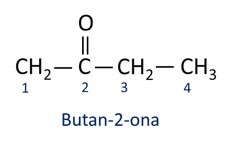
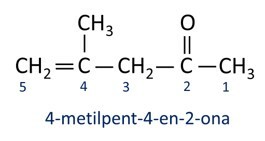
In generale, i chetoni trovano applicazione nella produzione di altri prodotti chimici e farmaceutici. Nell'industria, i chetoni sono usati come solventi per pitture, coloranti e vernici. Uno dei chetoni più noti è propanone, che è popolarmente noto come acetone. Le soluzioni di acetone vengono utilizzate per rimuovere lo smalto per unghie.
Leggi anche:Ammidi: composti che hanno un azoto attaccato al carbonile
Aldeide
La funzione organica dell'aldeide è caratterizzato dalla presenza del gruppo funzionale carbonilico, il cui atomo di carbonio ha un legame idrogeno.
Gruppo funzionale delle aldeidi: H–C=O (formile).
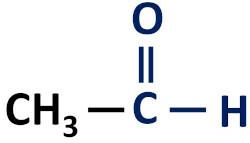
Le aldeidi si trovano sempre all'estremità delle catene di carbonio perché il loro atomo di carbonio deve essere legato ad almeno un atomo di idrogeno.
UN nomenclatura dei composti aldeidici segue le regole IUPAC, differenziandosi per il suffisso. Le aldeidi sono identificate dal suffisso -al.
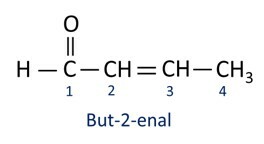
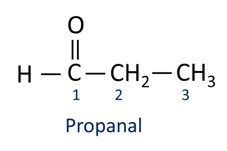
Le aldeidi sono utilizzate industrialmente nella produzione di profumi e aromatizzante, poiché il suo odore e sapore variano a seconda della lunghezza della catena di carbonio. I composti aldeidici sono utilizzati anche nella produzione di prodotti per la pulizia, medicinali, polimeri, tra gli altri. Le aldeidi a catena di carbonio corta possono essere utilizzate come agenti di conservazione, come il famoso formalina, che è un'aldeide chiamata metanale.

acido carbossilico
La funzione dell'acido carbossilico organico è identificata dalla presenza del gruppo funzionale carbossilico (-COOH).
Gruppo funzionale degli acidi carbossilici: –(C=O)OH o –COOH.

I composti appartenenti a questa funzione organica sono acidi deboli, in quanto rilasciano facilmente ioni H+ in soluzione acquosa.
UN nomenclatura degli acidi carbossilici segue le regole Iupac, tuttavia il termine “acido” compare prima del prefisso che indica il numero di carbonio, e il suffisso utilizzato è -oic.
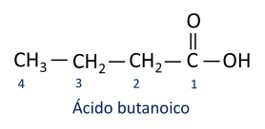
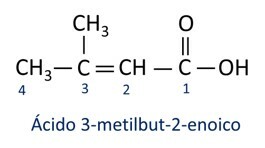
O acido carbossilico più comune nella vita di tutti i giorni è il Acido acetico, sostanza presente nell'aceto. La vitamina C, abbondante in molti agrumi, è una molecola organica chiamata acido ascorbico.
Estere
La funzione dell'estere organico è identificato dalla presenza del gruppo funzionale carbonilico, il cui atomo di carbonio ha un legante di ossigeno.
Gruppo funzionale degli esteri: –R–(C=O)O–R'.
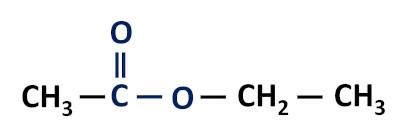
Gli esteri lo sono derivati degli acidi carbossilici, differendo da questi in quanto hanno un radicale alchilico attaccato all'atomo di ossigeno invece che all'atomo di idrogeno.
Le molecole appartenenti alla funzione estere sono formate dalla reazione tra un acido carbossilico e un alcol, reazione nota come esterificazione.
Le regole per nomenclatura degli esteri definito da Iupac considera che la molecola è formata da due parti:
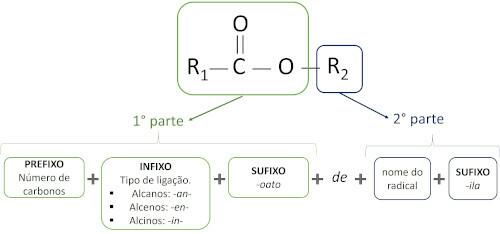
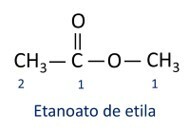
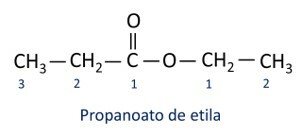
La caratteristica principale degli esteri è la loro capacità di simulare gusto e aroma degli alimenti naturali, secondo la lunghezza delle catene di carbonio (R1 e r2). Per questo motivo, gli esteri sono ampiamente utilizzati come agenti aromatizzanti nell'industria alimentare, nella produzione di prodotti farmaceutici, profumi e cosmetici.
Etere
La funzione organica dell'etere è caratterizzato dall'avere un atomo di ossigeno tra due catene di carbonio.
Gruppo funzionale degli eteri: R–O–R.

Gli eteri sono sostanze altamente infiammabili, con un odore caratteristico e forte.
UN nomenclatura ufficiale Iupac per gli eteri segue l'ordine prefisso + infisso + suffisso. Tuttavia, al lato della molecola che ha meno atomi di carbonio viene assegnato il suffisso -oxy mentre la catena di carbonio più lunga viene denominata come se fosse un idrocarburo, ricevendo il suffisso -o.
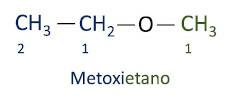
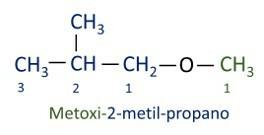
Gli eteri lo sono utilizzati come solventi per vernici, resine, oli e grassi. Di conseguenza, vengono utilizzati in diversi processi industriali e farmaceutici. L'etere una volta era usato come anestetico, oggi sostituito da altre sostanze più sicure.
Leggi anche:Composti nitro — composti che contengono gruppi nitro (NO2) nella loro molecola
Esercizi risolti sulle funzioni dell'ossigeno
domanda 1
(Uece) In Chimica Organica, un gruppo funzionale è definito come una struttura molecolare che conferisce alle sostanze un comportamento chimico simile. L'insieme dei composti che hanno lo stesso gruppo funzionale è chiamato funzione organica. Segna l'opzione che presenta correttamente il composto e la funzione organica a cui appartiene.

Risoluzione:
Lettera C
Tra le alternative, l'unica che esprime correttamente il gruppo funzionale al nome della funzione chimica è l'item C. La funzione dell'estere organico è definita dal gruppo funzionale carbonilico, il cui atomo di carbonio ha anche un ligando di ossigeno.
Al punto A è espresso il gruppo funzionale etere.
Nel punto B è espresso il gruppo funzionale chetonico.
Alla voce D è espresso il gruppo funzionale ammidico. ammine È ammidi appartengono alle funzioni dell'azoto.
Domanda 2
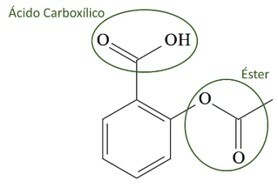
(UCS-RS) Nel V secolo a.C. C., Ippocrate, medico greco, scrisse che un prodotto di corteccia di salice alleviava il dolore e abbassava la febbre. Questo stesso prodotto, una polvere acida, è persino citato nei testi delle antiche civiltà del Medio Oriente, Sumer, Egitto e Assiria. I nativi americani lo usavano anche contro mal di testa, febbre, reumatismi e tremori. Questo farmaco è un precursore dell'aspirina, la cui struttura chimica è mostrata di seguito.
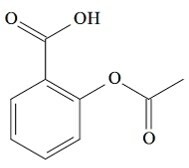
Le funzioni organiche presenti nella struttura dell'aspirina, sopra rappresentate, sono:
a) acido carbossilico ed estere.
b) alcool ed etere.
c) ammina e ammide.
d) ammina ed etere.
e) aminoacidi e alcol.
Risoluzione:
Lettera a
Di Ana Luiza Lorenzen Lima
Insegnante di chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/funcoes-oxigenadas.htm
