IL concentrazione comune, detta anche concentrazione in g/L, è il rapporto tra la massa di soluto in un volume di soluzione.
Matematicamente, la concentrazione comune è espressa attraverso la formula:
C = m/v
Dove,
C: concentrazione comune;
m: massa del soluto;
V: volume della soluzione.
L'unità più comunemente usata per la concentrazione comune è g/L, poiché la massa del soluto è calcolata in grammi (g) e il volume della soluzione in litri (L).
Ad esempio, l'acqua di mare ha una grande quantità di sali disciolti e il cloruro di sodio (NaCl), popolarmente noto come sale da cucina, è uno di questi.
La concentrazione di cloruro di sodio nell'acqua di mare è, in media, di 2,5 g/L. Quindi, ci sono 2,5 grammi di sale, che è il soluto, in ogni litro di acqua di mare, che è la soluzione.
Come calcolare la concentrazione comune?
Una soluzione è una miscela omogenea formata da una sostanza in quantità minore, chiamata soluto, disciolta in un solvente, che è in quantità maggiore.
Quindi, concentrazione comune si riferisce alla quantità di soluto in un dato volume di soluzione. Più soluto è disciolto nella soluzione, più è concentrato. Altrimenti, cioè un basso soluto indica che la soluzione è diluita.
Esempio 1: Qual è la concentrazione in g/L di una soluzione di ioduro d'argento (AgI) contenente 2,6 g in 1L di soluzione?
Quando viene data la quantità di soluto e il volume della soluzione, inseriamo semplicemente i valori nella formula di concentrazione comune per trovarne il valore.
Pertanto, in una soluzione di 2,6 g/L di ioduro d'argento ci sono 2,6 g di soluto in ogni 1 litro di soluzione.
Esempio 2: Quando si evapora il solvente da 500 mL di soluzione salina con una concentrazione di 6 g/L, qual è la massa di soluto ottenuta?
Si noti che in alcuni calcoli possiamo trovare la concentrazione comune descritta in modo da poter calcolare la massa del soluto.
È inoltre necessario prestare attenzione alle unità. Poiché la concentrazione comune è espressa in g/L, in questo caso è necessario convertire l'unità di volume prima di applicare la formula.
Poiché 1 litro contiene 1000 ml, 500 ml corrispondono a 0,5 litri.
Pertanto, evaporando il solvente dalla soluzione con una concentrazione di 6 g/L, si ottengono 12 g di soluto.
Acquisisci maggiori conoscenze con i contenuti:
- Concentrazione della soluzione
- concentrazione molare
- Diluizione di soluzioni
Risolti esercizi di concentrazione comuni
Utilizzare le seguenti domande per verificare le conoscenze acquisite in precedenza.
domanda 1
(Unicamp) Il solvente viene completamente evaporato da 250 mL di una soluzione acquosa di MgCl2 di concentrazione 8,0 g/L. Quanti grammi di soluto si ottengono?
a) 8.0
b) 6.0
c) 4.0
d) 2.0
e) 1.0
Alternativa corretta: d) 2.0.
Domanda 2
Vedi l'immagine qui sotto.
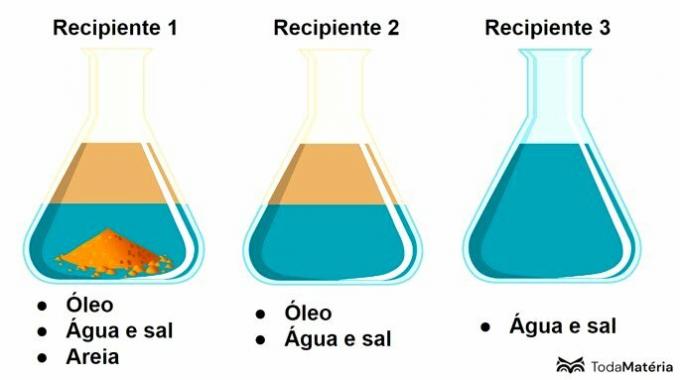
In questo schema, il contenitore 3 contiene a
a) miscela eterogenea
b) pura sostanza
c) Soluzione
d) miscela colloidale
Alternativa corretta: c) Soluzione.
Il contenitore 3 contiene una soluzione, che è una miscela omogenea formata da soluto e solvente, dove il sale è il soluto e l'acqua è il solvente.
In generale si può dire che il soluto è il componente in minor quantità e il solvente è presente in maggiore quantità.
Il contenitore 1 presenta una miscela eterogenea a 3 fasi e il contenitore 2 corrisponde a una miscela eterogenea a 2 fasi.
Domanda 3
Una soluzione è stata preparata sciogliendo 4,0 g di cloruro di magnesio MgCl2 fino a raggiungere una concentrazione di 2,0 g/L. Quale volume di soluzione è stato preparato?
a) 1 litro
b) 2 l
c) 4 L
d) 6 L
Alternativa corretta: b) 2 L.
Scopri altri problemi con la risoluzione commentata all'indirizzo esercizi di concentrazione comuni.
Riferimenti bibliografici
FONSECA, M. R. M. Chimica, 1. 1. ed. San Paolo: Attica, 2013.
SANTOS, WLP; MOL, GS Chimica dei cittadini, 1. 2. ed. San Paolo: Editora AJS, 2013.
USBERCO, J. Collegare la chimica, 1. 2. ed. San Paolo: Saraiva, 2014.
- Esercizi sulla concentrazione comune con feedback commentato
- soluzioni chimiche
- Soluto e Solvente: cosa sono, differenze ed esempi
- Concentrazione della soluzione
- Solubilità
- Molarità o Concentrazione Molare: cos'è, formula e come calcolarla
- Diluizione di soluzioni
- Esercizi sulle proprietà della materia