o tecnezio è un elemento di numero atomico 43 appartenenti al gruppo 7 della Tavola Periodica. È un metallo di transizione ed è stato il primo elemento ad essere prodotto artificialmente nella storia umana. È ancora dibattuto se il metallo possa essere trovato naturalmente in la crosta terrestre.
Questo elemento trova grande utilità in medicina nucleare, poiché possiede un isotopo in grado di produrre immagini utilizzate per la diagnosi di tumori in vari organi del Corpo umano. Sebbene la sua chimica non sia così sviluppata, l'interesse per esso è dovuto alla medicina nucleare.
Leggi anche:Niobio: un altro metallo di transizione
Riepilogo sul tecnezio
- Il tecnezio è stato il primo elemento ad essere prodotto artificialmente.
- Chimicamente, questo metallo è molto simile a renio, anche dal gruppo 7.
- Si ipotizza la presenza di tecnezio nella crosta terrestre, ma la sua produzione è ancora totalmente artificiale.
- L'elemento è ampiamente utilizzato in medicina nucleare per la diagnosi di tumori e l'imaging di vari organi.
- La sua scoperta avvenne nel 1937, ad opera del gruppo dello scienziato italiano Emilio Segrè.
Proprietà del tecnezio
- Simbolo: Tc.
- Numero atomico: 43.
- Massa atomica: 98 c.u.
- Configurazione elettronica: [Kr] 5s2 4d5.
- Punto di fusione: 2157°C.
- Punto di ebollizione: 4265°C.
- Densità: 11,50 g.cm-3.
- Serie chimica: Metallo di transizione; gruppo 7.
Non fermarti ora... C'è altro dopo l'annuncio ;)
Caratteristiche del tecnezio
Il tecnezio è un elemento originariamente artificiale, il primo prodotto dall'uomo. Il tecnezio metallico nella fascia del chilogrammo è già stato prodotto, inizialmente attraverso la riduzione del Tc2S7 a 1100 °C con gas idrogeno. Attualmente, la riduzione del pertecnetato di ammonio (NH4TcO4), anche con gas idrogeno.
Nella sua forma metallica, il tecnezio è grigio argenteo e si scurisce lentamente a contatto con l'aria. E 'degno di nota il tuo chimica è simile al renio, elemento situato appena sotto nel gruppo 7. Ad esempio, una volta divisi, entrambi possono bruciare a contatto con l'aria ad una temperatura di circa 370 °C. Hanno anche in comune il capacità di reagire con alogeni.
Il tecnezio non si dissolve acido cloridrico in nessuna concentrazione, ma si dissolve in:
- acido nitrico;
- aqua regia (miscela di acido nitrico e acido cloridrico ad alta concentrazione);
- acido solforico.
gli stati di ossidazione I valori più comuni per il tecnezio vanno da 0 a +7, ma la maggior parte della chimica del tecnezio ha l'anione pertecnetato (TcO4-) come precursore.
Attualmente sono catalogati 43 isotopi di tecnezio, le cui masse vanno da 86 a 113. Tra alcuni esempi di questi isotopi ci sono il 97Tc, con metà vita di 2,6 x 106 anni, e il 98Tc, con un'emivita di 4,2 x 106 Anni. L'isotopo più sfruttato chimicamente è il 99Tc, con un'emivita di 2,1 x 105 Anni.
Vedi anche: Bario — un altro elemento color argento
Presenza di tecnezio
È comune affermare che il tecnezio non si trova naturalmente sul nostro pianeta, è solo preparato sinteticamente. Tuttavia, nel 1956, il chimico giapponese Paul Kuroda predisse che una specie di potrebbe essere esistito un reattore nucleare naturale nel profondo di pianeta.
Cinque anni dopo, nel 1961, Kuroda riferì a presenza di 99Tc in un campione di pechblenda (minerale ricco di uranio), il cui contenuto sarebbe dell'ordine di 2 x 10-10 grammi di isotopo per chilogrammo di minerale.

Successivamente, nel 1962, i ricercatori francesi confermarono le teorie di Kuroda valutando campioni di roccia nel Gabon e anche indicato la presenza di tracce di tecnezio nei campioni. Così il L'idea che non ci sia tecnezio naturale è contraddittoria, oggetto di grande discussione all'interno della comunità scientifica.
Per quanto riguarda lo spazio, tecnezio è stato rilevato nelle chiamate stelle rosso gigante, negli anni '50, ma non nel sole, qualcosa che aiuta a dimostrare che il Sole è una stella relativamente nuova. Il rilevamento del tecnezio in queste stelle è stato molto importante, poiché l'emivita dell'elemento è molto più breve. rispetto all'età di queste stelle, suggerendo che il tecnezio viene effettivamente prodotto in questi corpi celeste.
Ottenere il tecnezio
Sebbene ci sia un dibattito sulla presenza naturale o meno del tecnezio sul nostro pianeta, è un dato di fatto che il La produzione di tecnezio avviene con mezzi artificiali nelle centrali nucleari. Corrisponde a circa il 6% dei prodotti di fissione del uranio, recuperato molti anni dopo.
Il suo recupero avviene in modo da dare tempo ai prodotti di fissione breve emivita e altamente radioattivi sono decaduti. In generale, il tecnezio viene separato dagli altri prodotti di fissione mediante resine a scambio ionico o estrazione con solvente.
Sappi anche che: Dubnio — elemento artificiale altamente radioattivo
Applicazioni del tecnezio
L'uso principale del tecnezio è in medicina nucleare, in particolare nella diagnosi dei tumori.Per questo viene utilizzato il decadimento isotopico 99 mTc, che corrisponde all'isotopo metastabile di 99Tc. La forma metastabile è la forma eccitata dell'isotopo tradizionale, cioè più energetica, con proprietà nucleari distinte.

Per scopi medicinali, il 99 mTc nel paziente sotto forma di a soluzione soluzione salina che sarà assorbita dal organo da valutare. Questo isotopo è prodotto dal molibdeno-99 (99Mo), anche sintetico, formando l'anione [99Muggire4]2-, che decade, emanando particelle β e produce il [99 mTcO4]-, forma chimica usata per essere iniettata nel paziente.
Questo isotopo metastabile è molto adatto a questo scopo in quanto, dopo essere stato iniettato, normalmente decade nell'isotopo 99Tc, emettendo radiazione abbastanza gamma (energia) per ottenere il risultato se viene utilizzato pochissimo dell'isotopo metastabile, qualcosa intorno a 1 x 10-9 a 1 x 10-12 talpe
Qualcosa di altrettanto vantaggioso è l'emivita del 99 mTc — nell'intervallo di sei ore. Questa emivita è abbastanza lunga perché il campione venga iniettato nel paziente prima di ogni altra decadimento, ma sufficientemente piccolo perché le emissioni siano misurabili a piccole concentrazioni di isotopo.
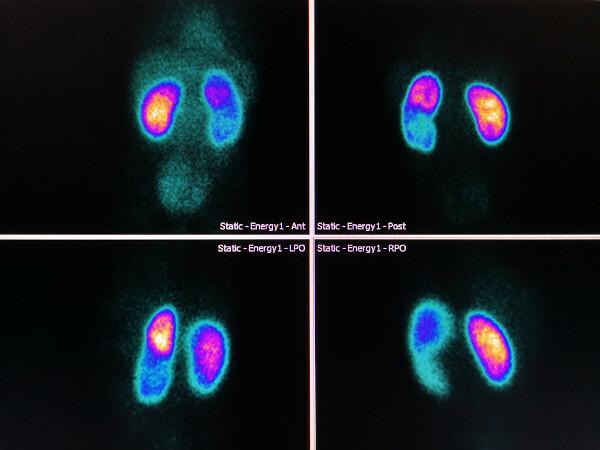
Tutta la radiazione gamma rilasciata viene utilizzata per generare un'immagine, che può essere:
- bidimensionale (da valutare tumori e metastasi);
- tridimensionale (per creare immagini del cuore, ossatura, fegato, reni e cervello).
Precauzioni con tecnezio

È necessario prestare attenzione radioattività di tecnezio, principalmente in modo che la sua manipolazione sia adeguata. In piccole quantità, come meno di 0,05 grammi, i rischi presentati non sono così gravi, sebbene siano necessarie precauzioni. Ad esempio, la radiazione gamma più pericolosa è quasi inesistente, ma la le emissioni beta sono facilmente contenute dal vetro.
Va anche ricordato che gli isotopi del tecnezio hanno una lunga emivita. Pertanto, la quantità di radiazione generata è piccola in un breve intervallo di tempo, il che rafforza ulteriormente la necessità di lavorare in piccole quantità.
Uno dei modi per manipolare il tecnezio implica uso di un cappuccio a guanti, in modo che il campione sia isolato e l'operatore non sia esposto ai rischi associati alle radiazioni.
Saperne di più: Quali elementi della tavola periodica sono radioattivi?
storia del tecnezio
gruppo 7 di Tavola periodica ha attirato l'attenzione per molto tempo, poiché nello sviluppo del tavolo originale di Dmitri Mendeleev, solo uno elemento chimico in esso contenuto: il manganese. Così, nel 20° secolo, sono stati fatti molti tentativi per scoprire gli elementi del gruppo 7, la maggior parte ovviamente inefficace.
Nel 1925, tuttavia, Otto Berg, Walter Noddack e Ida Tacke (poi Ida Noddack) affermarono di aver scoperto non uno, ma due nuovi elementi del gruppo 7, che chiamarono masurio (Z = 43) e renio (Z = 75). Il secondo è stato accolto, ma l'elemento 43 non ha avuto lo stesso rispetto, essendo oggetto di numerose controversie.
Di fronte a molte impasse, il la scoperta ufficiale dell'elemento 43 è attribuita all'italiano Emilio Segrè, che ha avuto l'aiuto del suo gruppo di ricercatori, nel 1937. Segrè e il suo team sono riusciti a manipolare un campione di molibdeno, che è stato bombardato dal deuterio per diversi mesi.
Dopo diverse analisi, il team italiano è riuscito a identificare questo nuovo elemento, che potrebbe essere separato per bollitura idrossido di sodio e una piccola quantità di perossido di idrogeno.
Il nome tecnezio deriva dal greco tecneto e significa "artificiale". |
Esercizi risolti su tecnezio
domanda 1
(ESCS-DF 2011) In medicina nucleare, i radiofarmaci sono utilizzati nella diagnosi e nel trattamento di varie malattie. Alcuni radiofarmaci utilizzano il tecnezio-99m (Tc-99m), che ha proprietà utili come marcatore. nuclide gamma-emettitore e può essere utilizzato negli esami del cervello, miocardio, tiroide, polmoni e altri.
L'uso di un radioisotopo dipende dalle sue proprietà chimiche e biologiche, inclusa la sua emivita. L'isotopo 99mTc ha un'emivita di sei ore, sufficiente perché si accumuli nell'organo da studiare e non permanga nell'organismo per lungo tempo.
La massa di 99mTc, necessaria per eseguire un determinato test, corrisponde a 500 mg. Considerando che un paziente si sottoporrà a tale esame 12 ore dopo la somministrazione del radionuclide, la quantità minima di radiofarmaco che il paziente deve assumere è pari a:
A) 2 g
B) 1 g
C) 500 mg
D) 250 mg
E) 125 mg
Risoluzione:
Alternativa A
L'emivita è il tempo necessario affinché la quantità di un campione radioattivo diminuisca della metà. Il paziente eseguirà l'esame 12 ore dopo la somministrazione del 99 mTc, che ha un'emivita di sei ore.
Se sono necessari 500 mg, significa che dopo 12 ore solo 500 mg del 99 mTc sarà disponibile. Entro 12 ore erano trascorsi due tempi di emivita, il che significa che il campione è stato dimezzato due volte, ovvero la quantità originale è stata divisa per quattro.
Pertanto, la quantità iniziale di radiofarmaco che il paziente deve ricevere è di almeno 2 grammi, poiché dopo 12 ore rimarranno solo 500 mg di campione.
Domanda 2
(Fameca-SP 2014) La figura mostra un generatore da 99mTc (tecnezio metastabile-99) prodotto in Brasile da Ipen. Questo radionuclide, utilizzato in medicina nucleare, è continuamente prodotto dal decadimento del radionuclide “genitore”, che è 99Mo (molibdeno-99). Il grafico mostra una tipica attività 99Mo di questi generatori in funzione del tempo in giorni.

Nell'equazione nucleare riferita al decadimento di 99Mo, il nuclide "genitore", a 99mTc, il nuclide "figlia", c'è un rilascio di
A) particelle alfa.
B) particelle beta negative.
C) particelle beta positive.
D) neutroni.
E) protoni.
Risoluzione:
Alternativa C
entrambi i 99Quanto il 99 mTc hanno la stessa massa. Loro dentro 99 mTc significa semplicemente che è un isotopo metastabile, cioè si trova a un livello di energia più alto dell'isotopo 99Tc convenzionale, ma senza alcuna interferenza nella massa.
Il molibdeno ha un numero atomico di 42, mentre il tecnezio ha un numero atomico di 43.
Pertanto, si può vedere che nel decadimento del 99Mo per la produzione di 99 mTc si è verificato il mantenimento della massa e l'aumento di un'unità del numero atomico. Questo è caratteristico dell'emissione di particelle beta negative, poiché queste particelle hanno massa trascurabile e numero atomico pari a -1, proprio come il elettrone.
Di Stefano Araújo Novais
Insegnante di chimica



