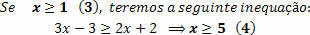IL francio, simbolo Fr, numero atomico 87, è un elemento appartenente al Gruppo 1 di Tavola periodica, i metalli alcalini. Tuttavia, a differenza degli altri elementi del gruppo, il francio non ha isotopi stabili, il che ha persino reso difficile la sua scoperta. In effetti, il francio era il ultimo elemento da scoprire e isolati in campioni naturali.
La sua grande instabilità atomica non consente di ottenere campioni visibili e pesanti, pertanto le sue proprietà fisico-chimiche sono estrapolate dai dati di altri metalli alcalini. Si stima che ci siano solo 30 grammi di francio nella crosta terrestre, il che lo rende il secondo elemento più raro del pianeta, dietro solo l'astato.
Leggi anche: Rubidio — elemento utilizzato nella fabbricazione di occhiali speciali e orologi atomici
riassunto francio
Il francio è un metallo alcalino situato nel settimo periodo della tavola periodica, simbolo Fr, Z = 87.
Non ha isotopi stabili ed è il secondo elemento più raro del pianeta.
Il suo isotopo più stabile ha un tempo di metà vita 22 minuti.
È l'elemento con il più grande raggio atomico della tavola periodica, oltre ad essere il più elettropositivo.
Può essere ottenuto solo mediante processi nucleari, essendo difficile da isolare.
Non ci sono ancora applicazioni pratiche relative al francio.
Proprietà del francio
Simbolo: FR.
massa atomica: 223.02 u.
Punto di fusione: 22°C (stimato).
Punto di ebollizione: 665 °C (stimato).
Densità: 2,5 g/cm³ (stimato).
elettronegatività: 0,79.
Distribuzione elettronica: [Rn] 7s1.
→ Video lezione sulle proprietà periodiche e aperiodiche degli elementi chimici
Caratteristiche del francio
il francio ha diversi isotopi, ma l'isotopo 233 è il più stabile, raggiungendo un'emivita di 22 minuti. Solo l'isotopo 212 ha un'emivita simile di 21 minuti, mentre gli altri non si avvicinano nemmeno a quella, e possono anche avere emivite dell'ordine dei secondi.

tutto questo instabilità atomica ostacola la determinazione di importanti caratteristiche fisiche e proprietà. Infatti le proprietà note sono state ottenute in condizioni estreme. diluizione (concentrazione dell'ordine di 10-15 moli/l).
Essendo un metallo alcalino, il suo numero di ossidazione è noto per essere +1. Gli esperimenti hanno anche dimostrato che francium è l'elemento più elettropositivo della tavola periodica. Un'altra posizione di primo piano che questo elemento ha nella tabella è quella con il diametro maggiore, con 2,7 angström (10-10 m).
Come altri metalli alcalini, il francio rimane in soluzione mentre altri elementi precipitano sotto forma di idrossidi, carbonati, fluoruri, solfuri, cromati, ecc.
Leggi anche: Cosa sono gli elementi radioattivi?
Ottenere il francio
Francium-223, l'isotopo più stabile di Fr, era rilevato per la prima volta attraverso l'emissione alfa di actina-227. È anche possibile produrre francio (isotopo 212) bombardando oro (197Au) con ossigeno-18 (18O) in un reattore nucleare.
Il frantium può essere ottenuto in diversi modi. Per esempio, c'è la possibilità di precipitarlo con il cesio, attraverso sali elementi poco solubili come il perclorato (ClO4-), esacloroplatinato (PtCl62-), iodato (IO4-), tra gli altri. Tuttavia, si prevede che la separazione di cesio e francio sarà molto difficile.
Altri metodi sviluppati negli anni '60 e '70 hanno permesso di separazione del francio da soluzioni di cesio e rubidio tramite resine scambiatrici di cationi. Il frantium-223, che è stato scoperto dall'emissione alfa dell'attinio-227, può anche essere separato dall'attinio e da altri prodotti di degradazione mediante tecniche di precipitazione selettiva. Esiste anche un'altra tecnica utilizzata con relativo successo: la sublimazione del cloruro di francio (FrCl) a temperature intorno ai 300 °C.
Applicazioni di francio
I test sui ratti hanno concluso che il francio si accumula nei reni, nel fegato e nelle ghiandole salivari. Inoltre, c'è stato un tentativo di applicarlo nella medicina nucleare, nella diagnosi del cancro, ma la difficoltà nel prepararlo e nell'isolarlo ha reso il progetto irrealizzabile. Questa caratteristica, sommata alla sua bassa emivita, rende il francium uno dei pochi elementi nessuna applicazione pratica.
Tuttavia, il fatto di avere il raggio atomico più grande della tavola periodica e avendo un solo elettrone nel strato di valenza mantiene alcuni ricercatori curiosi sulla sua natura. Nel 2002, un gruppo di ricercatori negli Stati Uniti è riuscito a intrappolare 300.000 atomi di francio per saperne di più sull'elemento.
Guarda il nostro podcast: Duro come un diamante: cosa significa?
storia del francio
Ciò che spicca nella storia del francio è il numero di volte in cui le persone hanno affermato di averlo scoperto dopo Mendeleev predisse l'esistenza di questo elemento nel 1871, sotto il nome di eka-cesio.
È noto da tempo che dopo l'elemento 83, bismuto, la tavola periodica mostra solo elementi radioattivi e instabili, con eccezioni come l'uranio e il torio. Anche così, questo non ha scoraggiato molti scienziati dal cercare l'elemento 87 nelle fonti naturali e, il più delle volte, affermare la sua scoperta.

Per esempio, nel 1925, il chimico russo Dobroserdov osservò un debole radioattività in un campione di potassio, concludendo che questo sarebbe l'elemento 87 e nominandolo russo, in onore del suo paese natale. Tuttavia, la migliore spiegazione per il fatto è stata che, in effetti, è stata rilevata la radioattività dall'isotopo. 40K, un beta emettitore che costituisce circa lo 0,012% del potassio naturale.
Nel 1926, i chimici inglesi Druce e Loring, analizzando le righe spettrali del solfato di manganese (II), presumevano anche di osservare alcune righe relative all'elemento 87, per le quali successivamente proposero il nome di alcalinio. Tuttavia, la debolezza delle prove ha scoraggiato i ricercatori dall'andare avanti.
Poi, nel 1930, Fred Allison rivendicò la scoperta dell'elemento 87 dopo alcuni esperimenti con campioni di polucite (un minerale ricco di cesio) e lepidolite (un minerale con litio nella sua composizione). Allison ha proposto il nome virginium in onore dello stato americano della Virginia. Tuttavia, nel 1934, MacPherson dimostrò imprecisioni nella scoperta di Allison.
Due anni dopo, Jean Perrin, un fisico francese noto per aver confermato la teoria del moto browniano di Einstein, fornendo, così, prove sufficienti dell'esistenza degli atomi, si unirono al fisico romano Horia Hulubei in una serie di esperimenti con i raggi X. Hanno quindi ottenuto i risultati attesi per l'elemento 87, che hanno prontamente chiamato moldavium, in riferimento alla regione della Moldova, luogo di nascita di Hulubei. Tuttavia, ancora una volta, il lavoro è stato criticato alla luce delle interpretazioni.
Nessuno dei ricercatori è riuscito a capire, ma quello che è successo è che il francio ha isotopi molto instabili, con un'emivita molto breve. La sfortuna è stata tale che è stata addirittura considerata l'inesistenza dell'elemento 87.
Tuttavia, nel 1939, la scoperta dell'elemento 87 è avvenuta da qualcuno che ha iniziato come assistente di laboratorio nientemeno che Marie Curie, a Parigi: Il Margherita francese Perey. Con una buona esperienza nella manipolazione e purificazione di campioni radioattivi, Perey è stato incaricato di analizzare un campione radioattivo di attinio, elemento 89.
lo scienziato è stato il primo ad osservare le emissioni alfa e beta prodotte dall'attinio, rivelando un nuovo elemento con un'emivita di 21 minuti. La francese annunciò poi con cautela la sua scoperta e, nel 1946, difese la sua tesi di dottorato Elemento 87: Attinio-K.
Il nuovo elemento fu poi chiamato francium, in onore del suo paese natale, inizialmente con il simbolo della Fa. Nel 1949, il International Union of Pure and Applied Chemistry (Iupac) ha confermato l'elemento con il nome dato da Perey, ma nel 1951 cambiò il simbolo in p.
Esercizi risolti sul francio
domanda 1
Il frantium (Fr, Z = 87) è un metallo alcalino con una breve emivita ed è instabile. Tuttavia, è noto per avere alcune proprietà simili ad altri metalli alcalini.
Sulla base delle informazioni di cui sopra, qual è il probabile composto formato tra francio e bromo (Br, Z = 35)?
A) FrBr2
B) Fr2fratello
C) FrBr
D) FrBr3
Rispondere
Il frantium, come metallo alcalino, ha NOX pari a +1. Già il bromo, a alogena, in assenza di ossigeno ha NOX pari a -1. Pertanto, il composto più probabile tra loro è la lettera C, FrBr.
Domanda 2
Il raggio atomico è una proprietà periodica estremamente importante, poiché non solo differenzia gli atomi in termini di dimensioni, ma aiuta anche a comprendere la reattività e altre proprietà degli atomi.
Tra gli elementi della Tavola Periodica, l'elemento che ha il raggio atomico maggiore è:
A) F
B) Cs
C) H
D) Fr
E) Og
Rispondere
È noto che il raggio atomico è tanto maggiore quanto maggiore è il periodo dell'elemento e quanto minore è il numero di elettroni nello strato di valenza. Quindi, l'elemento con il raggio più grande è il francio, Fr, poiché è nel settimo periodo della tavola periodica e ha un solo elettrone di valenza.
di Stéfano Araújo Novais
Insegnante di chimica