Gli alcoli possono subire ossidazione se esposti ad un agente ossidante, come una soluzione acquosa di dicromato di potassio (K2Cr2oh7) o permanganato di potassio (KMnO4) in ambiente acido.
Un ossigeno nascente [O] nel mezzo attaccherà il carbonio legato al gruppo funzionale dell'alcol (idrossile - OH), formando un composto molto instabile, detto diolo gemello, che ha due ossidrili legati allo stesso carbonio. Essendo instabile, questo composto rilascia acqua e dà origine ad un nuovo prodotto.
Questo prodotto dipenderà dal tipo di alcol che è stato ossidato, sia esso primario, secondario, terziario o metanolo.
In breve, abbiamo:
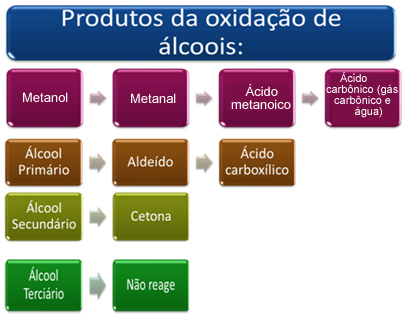
Vedi ogni caso di seguito:
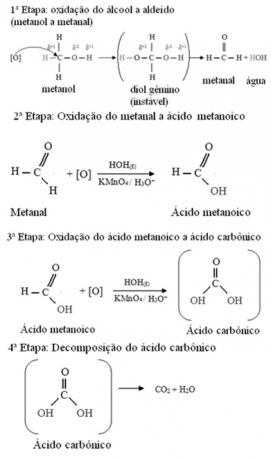
- Metanolo (H3C─OH):
Il metanolo è l'unico alcol che ha tre idrogeni legati al carbonio che subirà ossidazione. In questo caso, poiché ci sono tre punti sulla molecola che un ossigeno nascente può attaccare, si verificheranno tre ossidazioni successive, come mostrato nel diagramma sottostante:
- Alcoli primari:
In questi composti, il carbonio idrossile è legato a un solo atomo di carbonio, cioè gli altri due ligandi sono idrogeni e ci sono due punti in cui l'ossigeno nascente può attaccare.
Innanzitutto, ci sarà la formazione di un'aldeide, come mostrato di seguito:
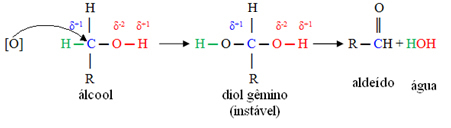
Ma l'ossidazione continua, perché i reagenti usati per ossidare l'alcol sono più forti di quelli usati per ossidare un'aldeide. Quindi, un altro ossigeno nascente attacca il carbonio carbonilico e produce un acido carbossilico.
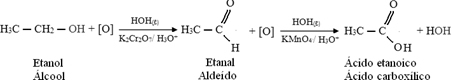
Quello che segue è un esempio, l'ossidazione dell'etanolo, prima ad etanale e poi ad acido etanoico (acido acetico). Questa reazione totale è la trasformazione del vino in aceto.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
L'ossidazione parziale dell'etanolo in etanale si verifica quando una persona alcolizzata esegue un test con etilometro usa e getta. All'interno di questo dispositivo è presente una miscela solida di dicromato di potassio e silice in ambiente acido, con la seguente reazione:
K2Cr2oh7 (ac) + 4H2SOLTANTO4(ac) + 3 CH3CH2Oh(G) → Cr2(SOLTANTO4)3(ac) + 7:002oh(1) + 3 CH3CHO(G) + K2SOLTANTO4(ac)
aranciaetanolo (incolore)verdeetanale (incolore)
Si noti che, oltre all'ossidazione dell'etanolo (alcool) ad etanale (aldeide), si ha una contemporanea riduzione del dicromato, che è arancione, a cromo (III), o anche cromo (II), che è verde. Il cambiamento di colore indicherà che la persona ha più alcol nel sangue di quanto consentito.
- Alcoli secondari:
Si tratta di composti in cui il carbonio idrossile è legato ad altri due atomi di carbonio e ad un solo atomo di idrogeno. Pertanto, ci sarà un solo punto nella molecola dove l'ossigeno nascente può attaccare e si formerà un solo tipo di prodotto, che sarà sempre un chetone:
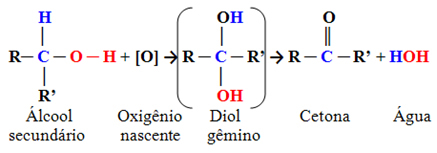
Poiché il carbonio carbonilico di un chetone non ha alcun idrogeno legato direttamente ad esso, non c'è più alcuna possibilità di ulteriore ossidazione. Pertanto, la reazione si ferma al chetone.
- Alcoli terziari:
Gli alcoli terziari sono quelli in cui il carbonio che ha il gruppo -OH forma tre legami con altri atomi di carbonio. Poiché non si legano con gli idrogeni, non c'è punto sulla molecola che possa essere attaccato dall'ossigeno nascente. Per questo motivo, gli alcoli terziari non subiscono ossidazione.
* Fonte e autore dell'immagine: CostaPPPR.
di Jennifer Fogaça
Laureato in Chimica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Aspetto:
FOGAÇA, Jennifer Rocha Vargas. "Ossidazione degli alcoli"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm. Consultato il 27 luglio 2021.
Chimica

Come funziona l'etilometro, concentrazione di alcol, etilometro, reazioni che coinvolgono l'alcol etilico, tipi di etilometro, dicromato di potassio, cella a combustibile, catalizzatore, rilascio di elettroni, acido acetico, idrogeno, concetto